
科目: 来源: 题型:
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,向1L0.5mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓H2SO4;③稀硝酸,恰好完全反应的热效应△H1、△H2、△H3的关系正确的是( )
A.△H1>△H2>△H3 B.△H1<△H3<△H2
C.△H1=△H3>△H2 D.△H1>△H3>△H2
查看答案和解析>>
科目: 来源: 题型:
下列各组热化学方程式中,△H1>△H2的是( )
①C(s)+O2(g)===CO2(g) △H1 C(s)+1/2O2(g)===CO(g) △H2
②S(s)+O2(g)===SO2(g) △H1 S(g)+O2(g)===SO2(g) △H2
③H2(g)+1/2O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
④CaCO3(s)===CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)===Ca(OH)2(s) △H2
A.① B.④ C.②③④ D.①②③
查看答案和解析>>
科目: 来源: 题型:
下列选项中说明乙醇作为燃料的优点的是①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境 ③乙醇是一种再生能源 ④燃烧时放出大量热量( )
A.①②③ B.①②④ C.①③④ D.②③④
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是( )
A.化学反应除了生成新物质外,还伴随着能量的变化
B.放热反应都不需要加热就能发生
C.吸热反应在一定条件(如常温、加热等)也能发生
D.化学反应是放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量
查看答案和解析>>
科目: 来源: 题型:
某有机物B是芳香烃的含氧衍生物,其相对分子质量不超过120,B中含氧的质量分数为14.8%,B与NaOH溶液不发生反应。有机物A在一定条件下可发生反应A+H2O![]() B+C。有关C的转化关系如下图所示:
B+C。有关C的转化关系如下图所示:
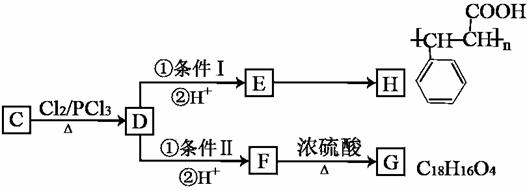
已知: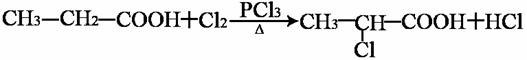
根据以上信息,回答下列问题:
(1)B的结构简式为 ,条件I、II中均需要的试剂为 。
(2)有关C的转化关系图中所发生的反应中属于取代反应的有 个。
(3)C的同分异构体中,同时符合下列要求的物质有 种。
a.苯环上有两个侧链 b.能发生银镜反应 c.能发生消去反应
(4)写出下列转化的化学方程式
F→E ;
F→G
查看答案和解析>>
科目: 来源: 题型:
中国石油天然气勘探开发公司位于尼日尔的分支机构CNPC—尼日尔石油公司,日前在该国东部最新发现了2900万桶的石油储量,勘探小组在石油样品中发现一种烃的含氧衍生物。可用下图所示装置确定其分子式和其组成。(不考虑空气进入装置)
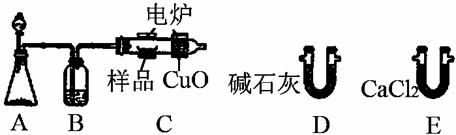
回答下列问题:
(1)A中发生反应的化学方程式为 。
(2)B装置的作用是 ,燃烧管C中CuO的作用是 。
(3)产生氧气按从左向右流向,燃烧管C与装置D、E连接。现甲、乙两位同学提出了两种连接方案。
方案1 甲同学认为连接顺序是:C→E→D
方案2 乙同学认为连接顺序是:C→D→E
请你评价两种连接方案,判断哪种方案正确并说明理由。
, 。
(4)准确称取1.8g烃的含氧衍生物X的样品,经充分燃烧后,D管质量增加2.64g,E管质量增加1.08g,实验测得X的蒸气密度是同温同压下氢气密度的45倍,则X的分子式为 ,1molX分别与足量Na、NaHCO3反应放出的气体在相同条件下的体积比为1∶1,X可能的结构简式为 。
查看答案和解析>>
科目: 来源: 题型:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1mol·L-1的四种溶液;
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列的顺序是_______________(用编号填写)。
(2)常温下,0.1mol·L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
D.c(OH-)/c(H+) E.c(H+)·c(CH3COO-)/c(CH3COOH)
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数_____(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是_____________________。

(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中
c(CH3COO-)-c(Na+)= mol·L-1(填精确值)。
(5)标准状况下,将1.12L CO2通入100mL 1mol·L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:
①c (OH-)=2c(H2CO3)+ ;
②c(H+)+c(Na+)= 。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F为原子序数依次增大的短周期元素,B、C相邻且同周期,A、D同主族。A、C能形成两种化合物甲和乙,原子个数比分别为2∶1和1∶1,甲为常见的溶剂。E是地壳中含量最多的金属元素。F元素为同周期电负性最大的元素。D和F可形成化合物丙,E和F可形成化合物丁。G为第四周期未成对电子数最多的元素
请回答下列问题:
(1)写出G基态原子的外围电子排布式 。
(2)B和C比较,第一电离能较大的元素是 (填元素符号),其原因为 。
(3)甲、乙两分子中含有非极性共价键的是 (填分子式)。
(4)已知化合物丁熔点190℃,沸点183℃,结构如图所示。

①丙和丁比较,熔点较低的化合物是 (填化学式),其原因为 。
②则丁晶体中含有的作用力有 (填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力
(5)G3+与元素A、C、F构成配合物戊,在含有0.001mol戊的溶液中加入过量AgNO3溶液,经过滤、洗涤、干燥后,得到287mg白色沉淀。已知该配合物的配位数为6,则戊的化学式为 。
(6)三聚氰胺(结构如图)由于其含氮量高被不法奶农添加到牛奶中来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石。三聚氰胺中N原子的杂化形式是 。

查看答案和解析>>
科目: 来源: 题型:
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有2个未成对电子。元素Z 的原子最外层电子数是其内层的3倍。
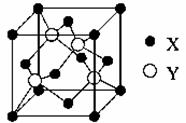
(1)X与Y所形成化合物晶体的晶胞如右图所示。
①在1个晶胞中,X离子的数目为 。
②该化合物的化学式为 。
(2)在Y的氢化物分子中,Y原子轨道的杂化类型是 。
(3)Z的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是 。
(4)Y 与Z 可形成YZ42-
①YZ42-的空间构型为 。
②写出一种与YZ42-互为等电子体的分子的化学式: 。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com