
科目: 来源: 题型:阅读理解
利用光能和光催化剂,可将CO2和H2O转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如下左图所示。


(1)在0-30小时内,CH4的平均生成速率vI、vII和vIII从大到小的顺序为 ;反应开始后的12小时内,在第 种催化剂的作用下,收集的CH4最多。
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,一定温度下发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g) K=27mol2·L-2。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,在上述温度下发生反应达到平衡,测得CO的物质的量为0.10mol,CH4的平衡转化率为 (保留两位有效数字)。
CO(g)+3H2(g) K=27mol2·L-2。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,在上述温度下发生反应达到平衡,测得CO的物质的量为0.10mol,CH4的平衡转化率为 (保留两位有效数字)。
(3)甲烷燃料电池是利用CH4跟氧气或空气反应将化学能转化成电能的装置,电解质溶液是强碱。下面有关说法正确的是 (填编号)。
A.负极反应为:O2+2H2O+4e- -→4OH-;
B.负极反应为:CH4+10OH- - 8e--→CO32-+7H2O
C.放电时溶液中的阴离子向负极移动
D.随放电的进行,溶液的pH值不变
(4)如上右图是一个电化学装置示意图,甲烷燃料电池作其电源。
①如果A为含有铁、银、金、碳杂质的粗铜,B为纯铜,C为CuSO4溶液,通电后,Cu2+的浓度将 (填“增大”、“减小”或“不变”)。
②如果A是铂电极,B是石墨电极,C是KBr溶液,通电时阳极的电极反应式是__________________________。
③特定条件下,该装置使用惰性电极电解Na2SO4浓溶液可制得少量过氧化氢:在阳极上SO![]() 被氧化成S2O
被氧化成S2O![]() (过二硫酸根离子),S2O
(过二硫酸根离子),S2O![]() 与H2O反应即可生成H2O2,
与H2O反应即可生成H2O2,
S2O![]() +2H2O === 2SO
+2H2O === 2SO![]() +H2O2+2H+。若各反应物质的转化率均为100%,则要制取1 mol H2O2,理论上燃料电池需消耗CH4的物质的量为 。
+H2O2+2H+。若各反应物质的转化率均为100%,则要制取1 mol H2O2,理论上燃料电池需消耗CH4的物质的量为 。
查看答案和解析>>
科目: 来源: 题型:
在化学反应中,只有极少数能量比平均能量高得多的分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。


(1)若上面左图表示的是H2(g)+ ![]() O2(g) === H2O(g)的反应过程,则该反应是 (填“吸热”或“放热”)反应,该反应的ΔH= (用含E1、E2的代数式表示)。
O2(g) === H2O(g)的反应过程,则该反应是 (填“吸热”或“放热”)反应,该反应的ΔH= (用含E1、E2的代数式表示)。
(2)若上面左图表示的是A2(g)+B2(g) == 2AB(g) ΔH=akJ·mol-1,已知其正反应的活化能为b kJ·mol-1,则其逆反应的活化能为 。
(3)已知CH4(g) +H2O(g)== CO(g) + 3H2(g) △H=+206.2kJ·mol-1
CH4(g) +CO2(g) == 2CO(g) + 2H2(g) △H=+247.4 kJ·mol-1
工业上常用的制氢方法是:CH4(g)与H2O(g)反应生成CO2(g)和H2(g),其热化学方程式为: 。
(4)电解尿素[CO(NH2)2]的碱性溶液也可以制氢,装置示意图见上面右图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为 。
(5)Mg2Cu是储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。
该反应的化学方程式为: 。
查看答案和解析>>
科目: 来源: 题型:
关于下图的说法正确的是 ( )
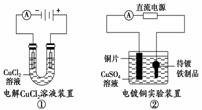
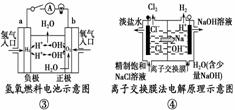
A.①装置中阴极处产生的气体能够使湿润淀粉KI试纸变蓝
B.②装置中待镀铁制品应与电源正极相连
C.③装置中电子由b极流向a极
D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
科目: 来源: 题型:
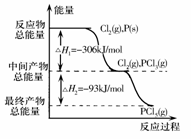
如图是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程和能量关系图。其中PCl5(g)分解成PCl3(g)和Cl2(g)的反应是一个可逆反应,温度T℃时,在密闭容器中加入0.6 mol PCl5,达平衡时PCl5还剩0.45mol,其分解率为α,则下列推断不正确的是 ( )
A.α等于25%
B.若升高温度,平衡时PCl5的分解率小于α
C.若起始时加入0.6 mol PCl3和0.6 mol Cl2,
以相同条件进行反应,则平衡时PCl3转化率为3α
D.PCl5分解的热化学方程式为
PCl5(g)![]() PCl3(g)+Cl2(g) △H=-93 kJ.mol-1
PCl3(g)+Cl2(g) △H=-93 kJ.mol-1
查看答案和解析>>
科目: 来源: 题型:
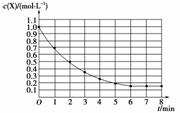
右图表示反应X(g)![]() 4Y(g)+Z(g),ΔH<0,在某温度时X的浓度随时间变化的曲线:下列有关该反应的描述正确的是 ( )
4Y(g)+Z(g),ΔH<0,在某温度时X的浓度随时间变化的曲线:下列有关该反应的描述正确的是 ( )
A.X的平衡转化率为85%
B.第6 min后,反应就终止了
C.若升高温度,X的平衡转化率将大于85%
D.若降低温度,v正和v逆将以同样倍数减小
查看答案和解析>>
科目: 来源: 题型:
用惰性电极电解含有一定量下列溶质的溶液,一段时间后,再加入一定质量的另一种物质(中括号内),溶液可能与原来溶液完全一样的是 ( )
A.CuCl2[CuSO4] B.NaOH[NaOH] C.NaCl[HCl] D.CuSO4[Cu(OH)2]
查看答案和解析>>
科目: 来源: 题型:
将NaCl溶液滴在光亮清洁的铁板上,一段时间后发现液滴覆盖的中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是 ( )
A.液滴中的Cl-由a区向b区迁移
B.液滴边缘是正极区,发生的电极反应为:
O2 + 2H2O + 4e- === 4OH-
C.液滴下的Fe因发生还原反应被腐蚀,生成的Fe2+由a区向b区迁移,与OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e- === Cu2+

查看答案和解析>>
科目: 来源: 题型:
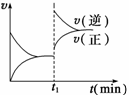
如图为某化学反应的速率与时间的关系示意图。在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是 ( )
A.2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0
2SO3(g) ΔH<0
B.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
C.H2(g)+I2(g)![]() 2HI(g) ΔH>0
2HI(g) ΔH>0
D.2A(g)+B(g)![]() 2C(g) ΔH>0
2C(g) ΔH>0
查看答案和解析>>
科目: 来源: 题型:
电镀废液中Cr2O72-可通过反应转化成铬黄(PbCrO4):
Cr2O72-(aq)+2Pb2+(aq)+H2O(l)![]() 2 PbCrO4(s)+2H+(aq)ΔH<0
2 PbCrO4(s)+2H+(aq)ΔH<0
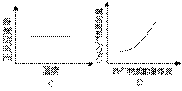
反应达平衡后,改变横坐标表示的条件,下列图示正确的是 ( )

查看答案和解析>>
科目: 来源: 题型:
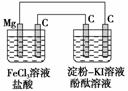
某电化学实验研究装置如图所示。有关说法不正确的是( )
A.镁为负极 B.原电池碳极上反应为Fe3++e-―→Fe2+
C.电解池中阳极处变红,阴极处变蓝
D.电解池阴极的反应为2H++2e-―→H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com