
科目: 来源: 题型:
在25mL 0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1CH3COOH溶液,溶液pH变化曲线 如右图所示,下列有关离子浓度的关系正确的是
A.在A、B间,溶液中可能有c(Na+)>c(OH-) >c(CH3COO-)>c(H+)
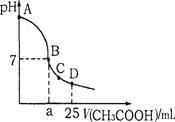 B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.在D点,c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,将64 g SO2气体和32g氧气通入密闭容器中生成SO3气体,达到平衡时,共放出热量78.64KJ,已知SO2在此条件下转化率为80%,则下列热化学方程式正确的是
A.SO2(g)+1/2O2(g)![]() SO3(g);△H=-78.64KJ·mol-1
SO3(g);△H=-78.64KJ·mol-1
B.2SO2(g)+O2(g)![]() 2SO3(g);△H=-196.6KJ·mol-1
2SO3(g);△H=-196.6KJ·mol-1
C.SO2(g)+1/2O2(g)![]() SO3(l);△H=-98.3KJ·mol-1
SO3(l);△H=-98.3KJ·mol-1
D.2SO2(g)+O2(g)![]() 2SO3(g); △H=+196.6KJ·mol-1
2SO3(g); △H=+196.6KJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
下列关于离子交换膜法电解食盐水的说法错误的是
A.阴极产物为NaOH和H2 B.所用离子交换膜只允许阴离子通过
C.阳极反应式为2Cl-―2e-= Cl2↑ D.阳极室注入精制的较浓食盐水
查看答案和解析>>
科目: 来源: 题型:
在一定条件下发生下列反应,其中属于盐类水解反应的是
A.NH4++2H2O![]() NH3·H2O+H3O+ B.HCO3–+ H2O
NH3·H2O+H3O+ B.HCO3–+ H2O![]() H3O+ + CO32–
H3O+ + CO32–
C.NH3 +H2O![]() NH4+ +OH– D.Cl2+H2O
NH4+ +OH– D.Cl2+H2O![]() H++Cl–+HclO
H++Cl–+HclO
查看答案和解析>>
科目: 来源: 题型:
恒容密闭容器中进行的可逆反应2NO2![]() 2NO+O2,达到平衡状态的是
2NO+O2,达到平衡状态的是
①单位时间内生成a mo1 O2的同时生成2a mol NO2
②单位时间内生成a mol O2的同时生成2a molNO
③混合气体的颜色不再改变
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
A.①③④ B.②④⑤ C.①③⑤ D.①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
下列反应中,熵显著减少的反应是
A、CO(g)+2H2(g)= CH3OH(g)
B、CaCO3(s)+2HCl(aq)= CaCl2(aq)+CO2(g)+H2O(l)
C、(NH4)2CO3(s)= NH4HCO3(s)+NH3(g)
D、2HgO(s)= 2Hg(l)+O2(g)
查看答案和解析>>
科目: 来源: 题型:
下列与平衡移动无关的是
A.向0.1 mol/L的CH3COOH中加入少量CH3COONa固体,溶液pH增大
B.向水中投入金属Na,最终溶液呈碱性
C.在密闭容器中充入一定量NO2建立2NO2(g)![]() N2O4(g)平衡后,增大压强,体系颜色加深
N2O4(g)平衡后,增大压强,体系颜色加深
D.在滴有酚酞的Na2CO3溶液中,慢慢滴入BaCl2溶液,溶液的红色逐渐褪去
查看答案和解析>>
科目: 来源: 题型:
右图是探究铁发生腐蚀的装置图。发现开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水柱又上升。下列说法不正确的是
A.开始时发生的是析氢腐蚀
B.一段时间后发生的是吸氧腐蚀
C.两种腐蚀负极的电极反应均为:Fe - 2e-== Fe2+
D.析氢腐蚀的总反应为:2Fe + O2 + 2H2O == 2Fe(OH)2

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com