
科目: 来源:2013届浙江省嘉兴市高三上学期基础测试化学试卷(带解析) 题型:填空题
某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入l~2滴溴水,振荡后溶液呈黄色。
(1)提出问题: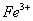 、
、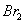 哪一个的氧化性更强?
哪一个的氧化性更强?
(2)猜想
①甲同学认为氧化性: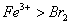 ,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性: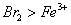 ,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(3)设计实验并验证
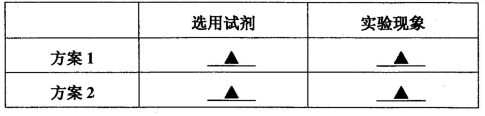
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。供选用的试剂:
| A.酚酞试液 | B.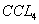 | C.无水酒精 | D.KSCN溶液 |
查看答案和解析>>
科目: 来源:2012-2013学年黑龙江省哈尔滨四中高一下学期期中考试化学理科试卷(带解析) 题型:填空题
硫酸在下列用途或反应中所表现的性质(用字母填在横线上)。
| A.难挥发性 | B.强酸性 | C.吸水性 | D.脱水性 E.强氧化性 |
查看答案和解析>>
科目: 来源:2012-2013学年辽宁省丹东市宽甸二中高二4月月考(一)化学试卷(带解析) 题型:填空题
氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO3-+4H++3e→NO+2H2O
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:
。
查看答案和解析>>
科目: 来源:2012-2013学年吉林省吉林一中高二4月月考化学试卷(带解析) 题型:填空题
将W g木炭与 同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为
同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为 ,高温下容器中木炭与
,高温下容器中木炭与 均完全反应后恢复到原温度,压力表的示数为
均完全反应后恢复到原温度,压力表的示数为 ,试求:
,试求:
(1)当W取值发生变化时,反应后压强P也发生变化,P的最大值(以 表示)是______。
表示)是______。
(2)以W表示满足题设条件的a的取值范围__________。
(3)在题设条件下,W、a、P、 之间必须满足函数系W=f(a、
之间必须满足函数系W=f(a、 、P),写出该函数表达式:__________________。
、P),写出该函数表达式:__________________。
查看答案和解析>>
科目: 来源:2013届辽宁省沈阳市第二十中学高三高考领航考试(三)化学试卷(带解析) 题型:填空题
【化学——选修化学与技术】(15分)现有一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2[CuCl2]-+S
请回答下列问题:
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是 _____________________ ________、___________________________________ 。
(2)反应Ⅰ的产物为(填化学式) ___________________ 。
(3)反应Ⅲ的离子方程式为 ____________________________________________________ 。
(4)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是 ___________
(5)黄铜矿中Fe的化合价为+2,对于反应:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是 ___________________ (填字母)。
8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是 ___________________ (填字母)。
| A.反应中被还原的元素只有氧 | B.反应生成的SO2直接排放会污染环境 |
| C.SO2既是氧化产物又是还原产物 | D.当有8mol铜生成时,转移电子数目为100NA |
查看答案和解析>>
科目: 来源:2012届福建省莆田二中高三上学期期中考试化学试卷(带解析) 题型:填空题
金属钛被称为铁和铝之后崛起的“第三金属”,常见化合价为+4。它是空间技术、航海、化工、医疗上不可缺少的材料。
工业上用钛铁矿(主要成分FeTiO3)制备金属钛的一种工艺流程如下图(部分产物略去):
(1)步骤①反应的化学方程式为:2FeTiO3 + 6C + 7Cl2 2FeCl3 + 2TiCl4 + 6CO,还 原剂是 ,每生成1mol TiCl4转移 mol电子。
2FeCl3 + 2TiCl4 + 6CO,还 原剂是 ,每生成1mol TiCl4转移 mol电子。
(2)步骤②分离出TiCl4的方法,利用了TiCl4与FeCl3 的不同。
(3)步骤④反应的化学方程式为______________ __________,该反应在氩气中进行的理由是_________ _____________________。
(4)绿色化学提倡物料循环。以上流程中,可用于循环的物质除Cl2、Mg外,还有___。
查看答案和解析>>
科目: 来源:2013学年江西省德兴一中、横峰中学、铅山一中、弋阳一中高一第三次月考化学试卷(带解析) 题型:填空题
(8分)已知将盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
(1)该反应中,化合价升高的反应物是________,化合价没有发生变化的反应物是________。
(2)写出一个包含上述七种物质的氧化还原反应方程式(不需配平)_________________。
(3)上述反应中,氧化剂是________,1 mol氧化剂在反应中________(填“得到”或“失去”)________mol电子。
(4)如果在反应后的溶液中加入NaBiO3,溶液又变紫红色。说出NaBiO3的一个性质:
________________________________________________________________________。
查看答案和解析>>
科目: 来源:2012-2013学年浙江省宁海县正学中学高一下学期第一次阶段性测试化学试卷(带解析) 题型:填空题
(1)在试管里放入一小块铜片,注入一定体积的浓硫酸,给试管加热,使之反应。若铜片还有剩余硫酸是否消耗完毕?
①结论及理由是:_________________________________________。
②向100毫升18 mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量
A.小于0·9 mol B.等于0·9 mol C.在0·9 mol与1.8 mol之间 D.大于1·8 mol
③50g的胆矾加热到100℃失去部分结晶水后,质量变为35.6g,则失去水后的硫酸铜晶体的化学式是
A.CuSO4·H2O B.CuSO4·2H2O C.CuSO4·3H2O D.CuSO4
(2)足量的锌投入到一定量的浓硫酸中,充分反应后共收集到SO2和H222.4L(标准状况)。
①简述能产生H2的原因是____________ __________________
②上述变化中体现浓硫酸强氧化性的反应方程式是:
③反应共消耗金属锌的质量为_________g。
④以上数据能否计算出消耗的硫酸的物质的量? _ (填“能”或“不能”)
查看答案和解析>>
科目: 来源:2012-2013学年湖南省怀化市高一上学期期末考试化学试卷(带解析) 题型:填空题
工业上常利用反应 3Cl2+8NH3 =6NH4Cl+N2 检查氯气管道是否漏气。回答下列问题:
(1)该反应中,氧化剂是 ,发生氧化反应的物质是 。
(2)该反应中氧化剂与还原剂的物质的量之比为 。
(3)若标准状况下有6.72L N2生成,则转移电子的物质的量为 mol。
查看答案和解析>>
科目: 来源:2012-2013学年山西省忻州一中高二上学期期末联考化学(文)试卷(带解析) 题型:填空题
(8分)我国从1994年起在食盐中添加碘酸钾(KIO3)作为营养强化剂。请回答:
(1)成人如果长期缺碘,会引起的病症是 (填字母)。
A.佝偻病 B.甲状腺肿大 C.夜盲症
(2)在瘦肉、胡萝卜、海带中,富含碘元素的是 。
(3)依据化学方程式为:5KI+KIO3+6HCl = 6KCl+3I2 +3H2O可检验加碘盐中是否含有碘。此反应中的还原剂是 (填化学式),生成的含I2的溶液遇淀粉可变为 色。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com