
科目: 来源:2010—2011学年福建省罗源一中高一3月月考化学试卷 题型:填空题
(4分)利用氧化还原反应原理配平
⑴ NH3 + O2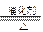 NO + H2O
NO + H2O
⑵ FeSO4 + KNO3 + H2SO4 = K2SO4 + Fe2(SO4)3 + NO↑+ H2O
查看答案和解析>>
科目: 来源:2010—2011学年广东省揭阳一中高一上学期期末考试化学试卷 题型:填空题
(6分)有人在研究硫酸亚铁受热分解反应时,作了两种假设:
⑴假设它按氯酸钾受热分解的方式来分解,反应的化学方程式为:
⑵假设它按碳酸钙受热分解的方式来分解,反应的化学方程式为:
⑶事实上,硫酸亚铁分解为氧化铁,二氧化硫,三氧化硫(分解温度为500℃左右),则反应化学方程式为:
查看答案和解析>>
科目: 来源:2011届上海市十校高三下学期第二次联考化学试卷 题型:填空题
某反应体系中有物质:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4。
(1)请将NaBiO3之外的反应物与生成物分别填入以下空格内。
(2)反应中,被氧化的元素是____________,氧化剂是___________。
(3)将氧化剂与还原剂及其已配平的化学计量数填入 下列空格中,并标出电子转移的方向和数目。
下列空格中,并标出电子转移的方向和数目。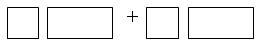
查看答案和解析>>
科目: 来源:2010—2011学年西藏拉萨中学高二第一次月考化学试卷 题型:填空题
(Ⅰ)(6分)配平下列氧化还原反应方程 式:
式: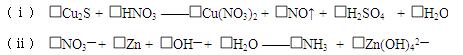
(Ⅱ)(10分)某温度时,在容积为2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答: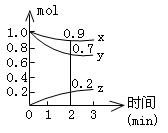
(1)计算反应开始2min内的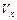 = ,
= , 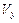 = ,
= , = ,
= ,
(2)容器内的反应物是 。
(3)写出该反应的化学方程式 。
查看答案和解析>>
科目: 来源:2011届浙江省杭州师范大学附属中学高三上学期第一次月考化学卷 题型:填空题
请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式:
(1)_________+__________→__________+__________+__________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)请将反应物的化学式及配平系数填入下列相应的位置中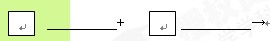
查看答案和解析>>
科目: 来源:2011届广西河池高级中学高三第六次月考理综化学部分 题型:填空题
交警常用“司机饮酒检测仪”检查司机是否酒后驾车,其原理是硫酸酸化的重铬酸盐(Cr2O72-橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等。重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬。方法如下:
将铬铁矿[主要成分Fe(CrO2)2]与纯碱、氧气高温焙烧,除杂、酸化,得到重铬酸钠,碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,Cr2O3再经铝热法还原,即可制得金属铬。请回答:
(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式是 。
(2)写出碳和重铬酸钠高温反应的化学方程式 。
Cr2O3经铝热法还原制得金属铬的化学方程式是 。
(3)硫酸酸化的Na2Cr2O7和FeSO4反应,生成Cr3+等,该反应的离子方程式是 。
(4)某Na2Cr2O7样品2.00g恰好和4.56gFeSO4完全反应,该样品的纯度为 。
查看答案和解析>>
科目: 来源:2011届上海市卢湾区高三上学期期末考试化学试卷 题型:填空题
亚硫酸 钠和碘酸钾在酸性溶液中发生以下发应:
钠和碘酸钾在酸性溶液中发生以下发应:
Na2SO3+ KIO3+ H2SO4 → __Na2SO4 + K2SO4+ I2 + 
(1)配平上面的方程式,在横线上填入系数,在方框填上反应产物
(2)其中氧化剂是 ,若反应中有2.5mol电子转移,则生成的碘是 mol;氧化产物为 mol。
(3)该反应的过程和机理较复杂,一般认为发生以下四步反应:
① IO3- +SO32 -  IO2- + SO42 - (反应速率慢)
IO2- + SO42 - (反应速率慢)
② IO2- + 2SO32 -  I- + 2SO42 - (反应速率快)
I- + 2SO42 - (反应速率快)
③ 5I- +6H+ +IO3- 3I2 +3H2O (反应速率快)
3I2 +3H2O (反应速率快)
④ I2 +SO32 - +H2O  I- + SO42 -+2H+ (反应速率快)
I- + SO42 -+2H+ (反应速率快)
根据上述步骤推测该反应总的反应速率由_____(填反应编号)步反应决定。
(4)预先加入淀粉溶液,由上述四步反应可以看出必须在_____离子消耗完后,才会使淀粉变蓝的现象产生。
查看答案和解析>>
科目: 来源:2011届上海市嘉定区高三上学期第一次质量调研化学试卷 题型:填空题
XeO3是一种不稳定的物质,具有强氧化性。
(1)配平反应的离子方程式:
_____XeO3+____Mn2+ +_____H2O → MnO4-+____Xe↑+___H+
(2)反应现象为:①有气泡产生,②______________________。
(3)发生氧化反应的物质(或微粒)是_______________。
①此时转移电子_____________mol。
②将反应后的溶液稀释至90mL,所得溶液的pH=________。
查看答案和解析>>
科目: 来源:2011届浙江省杭州二中高三10月月考化学试卷 题型:填空题
在有机化学工业中常用的一种钠盐是NaBH4,即硼氢化钠。它具有很强的还原性,也是一种高贮氢密度材料,是最有可能作为氢燃料电池的即时供应氢源。但它不能与水和酸共存。
⑴将其投入水中可生成偏硼酸钠(NaBO2)和氢气,写出该反应的化学方程式 ,反应中的还原剂是 ,每摩NaBH4反应时电子转移数为 mol。
⑵若将NaBH4投入酸溶液中其反应速率与其放入水中相比,应快还是慢 ,理由是 。
⑶NaBH4还用于将含Au3+的碱性废液中回收黄金,其离子方程式为: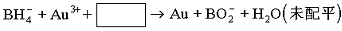
请写出配平的离子方程式 。
查看答案和解析>>
科目: 来源:2010年青海省青海师大附中高二上学期期中考试化学试卷 题型:填空题
实验室制取氯气时,若没有MnO2则用KMnO4代替,据此回答下列问题:
(1)配平该反应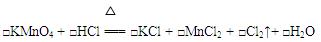
(2)被氧化的HCl与未被氧化的HCl的物质的量之比为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com