
科目: 来源:2012届河南省卫辉市第一中学高三第一次月考化学试卷 题型:填空题
(13分)铝土矿的主要成分是A12O3,含有Fe2O3、
SiO2等杂质,按下列操作从铝土矿中提取A12O3。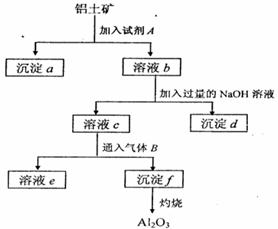
回答下列问题:
(1)沉淀物的化学式分别是:
 ;d ;
;d ;
f ;
(2)写出加入过量NaOH溶液时所发生主要
反应的离子方程式 、
(3)写出通入气体B(过量)时溶液C中发生反应
的离子方程式 、 。
(4)气体B能否改用试剂A代替?为什么? ,  。
。
查看答案和解析>>
科目: 来源:2011-2012年安徽省六校教育研究会高二素质测试化学卷 题型:填空题
(12分)从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下: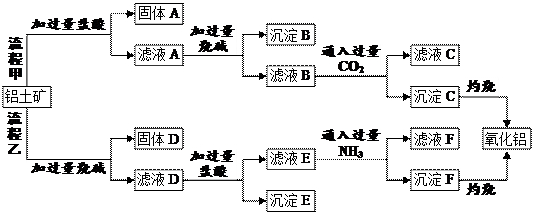
请回答下列问题:
⑴流程甲中,固体A的主要成分是______(填化学式,下同),沉淀B的主要成分是_______,生成沉淀C的离子方程式为__________________。
⑵流程乙中,加过量烧碱时发生反应的离子方程式为________________,沉淀E的主要成分是_________。
⑶生成沉淀F的离子方程式为____________________________________。
查看答案和解析>>
科目: 来源:2011届浙江省绍兴一中高三期中考试化学试卷 题型:填空题
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下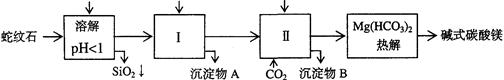
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
科目: 来源:2010-2011学年福建省厦门六中高二下学期期中考试化学试卷 题型:填空题
(9分)胃舒平主要成分是氢氧化铝,同时含有三硅镁(Mg2Si3O8`H2O)等化合物。
(1)比较铝离子和镁离子半径大小(用离子符号表示)______________________。
(2)比较铝和镁的第一电离能大小__________________(用元素符号表示)
(3)下列事实不能说明镁比铝的金属性强的是____________
A.Al(OH)3可溶于强碱溶液中,M g(OH)2不能 g(OH)2不能 |
| B.Mg能从铝盐溶液中置换出铝 |
| C.Mg 原子最外层只有2个电子, 而Al原子最外层有3个电子 |
| D.Mg与盐酸反应比铝与盐酸反应更剧烈 |
 点,都可以制耐火材料,其原因是_____________________
点,都可以制耐火材料,其原因是_____________________查看答案和解析>>
科目: 来源:2010—2011学年浙江省杭州十四中高二下学期期中考试化学试卷 题型:填空题
(10分)从某铝镁合 金片上剪下一小块(质量为1.0g),立即投入到盛有10mL10mol/LNaOH溶液的小烧杯中。
金片上剪下一小块(质量为1.0g),立即投入到盛有10mL10mol/LNaOH溶液的小烧杯中。
(1)自反应开始到反应结束,从小烧杯中可观察到的主要现象。(请依次写出)
(2)开始时产生气泡的速率较慢的原因是 。
后来的反应速率相当快的原因是 。
(3)写出所形成的原电池的负极材料名称:
电 极反应式:
极反应式:
(4)欲利用该反应来测定合金中铝的含量,还应测定的数据。(请逐一写出)
查看答案和解析>>
科目: 来源:2010—2011学年江西省德兴一中高一下学期第一次月考化学试卷 题型:填空题
(4分)取等物质的量的MgO和Fe2O3的混合物进行铝热反应,反应的化学方程式为 , 引发铝热反应的实验操作是
。 (各2分)
查看答案和解析>>
科目: 来源:2010—2011学年广东省汕头金山中学高一下学期第一次月考化学试卷 题型:填空题
(4分)室温下,将铁片、铜片、铝片(表面用砂纸打磨过)分别投入浓盐酸、浓硫酸、浓硝酸、浓氢氧化钠溶液四种试剂中,做了12个实验,实验的编号如下表所示。
| | 浓盐酸 | 浓硫酸 | 浓硝酸 | 浓氢氧化钠溶液 |
| 铝 | 实验1 | 实验2 | 实验3 | 实验4 |
| 铁 | 实验5 | 实验6 | 实验7 | 实验8 |
| 铜 | 实验9 | 实验1O | 实验11 | 实验12 |
 。
。查看答案和解析>>
科目: 来源:2010—2011学年黑龙江省大庆中学高一上学期期末考试化学试卷 题型:填空题
(6分)向20mL某物质的量浓度的AlCl3溶液中滴入2mol/LNaOH溶液时,得到的Al(OH)3沉淀质量与所加NaOH溶液体积(mL)的关系如图所示,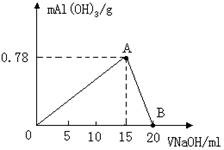
试回答下列问题:
(1)图中A点表示的意义是 ___________
(2)图中B点表示的意义是___________
(3)上述两步总反应用总的离子方程式可表示为:___________
(4)若溶液中有Al(OH)3沉淀0.39g,则此时用去NaOH溶液的体积为___________(写出计算过程)
查看答案和解析>>
科目: 来源:2011届四川省南充市高三第二次诊断性考试(理综)化学部分 题型:填空题
铝是国民经济发展的重要材料,铝在地壳中的含量约占8% ,目前我国铝消费量超过430万吨,在众多的金属中仅次于铁。请回答下问题:
(I )实验室中用金属铝制备少量氢氧化铝,有以下3种方案:
方案1: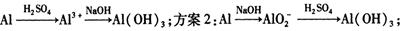
方案3: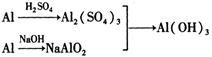 o
o
制备相同物质的量的氢氧化铝消耗酸和碱最少的是方案_____________________。
(II)工业上冶炼铝的流程图如图16所示: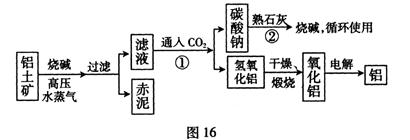
在制取氧化铝的过程中,分析铝土矿和赤泥中所含Al2O3、Fe203质量分数的数据如下:
| | Al2O3 | Fe2O3 | 其他杂质 |
| 铝土矿 | 55% | 16% | — |
| 赤泥 | 15% | 48% | 一 |
查看答案和解析>>
科目: 来源:2011届福建省莆田市高三教学质量检查化学试卷 题型:填空题
(9分)铝和铁及其化合物在生产、生活中有广泛应用。请回答下列问题:
(1)“和谐号”动车组是由中国自主研发制造的世界上运营速度最高的动车组列车之一,列车采用轻量化铝合金车体,主要利用铝 的性质。
(2)明矾可用作净水剂,在使用时发现并不能使酸性废水中的悬浮物沉降除去,其原因是 。
(3)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO 3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移电子的物质的量是 。
3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移电子的物质的量是 。
(4)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为: 。
(5)某高效净水剂可由Fe(OH)SO4聚合得到。工业上以FeSO4、NaNO2和稀硫酸为原料来制备Fe(OH)SO4,反应中有NO生成,化学方程式为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com