
科目: 来源:2011-2012学年广东省汕头金山中学高一第一学期期末考试化学试卷 题型:填空题
(11分)铝土矿的主要成分是Al2O3,含有Fe2O3、SiO2等杂质,按下列操作从铝土矿中提取Al2O3。回答下列问题:
(1)沉淀物的化学式分别是:a ;d ;f 。
(2)溶液b中所含的金属阳离子是 ;溶液c中所含的酸根离子是 。
(3)加入的试剂A是 ,通入的气体B是 ,能否将B换成A?其理由是 。
查看答案和解析>>
科目: 来源:2011-2012学年北京市四中高一上学期期末考试化学试卷 题型:填空题
(9分)铝土矿的主要成分是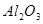 ,含有杂质
,含有杂质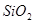 、
、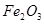 、
、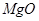 。工业上从铝土矿中提取铝可采用如下工艺流程:
。工业上从铝土矿中提取铝可采用如下工艺流程: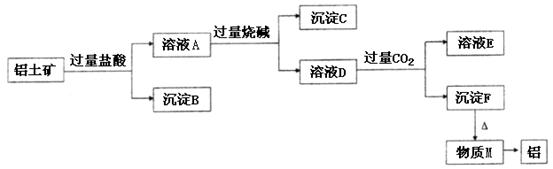
请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是____________(填操作名称)。
(2)沉淀B的成分是____________(填化学式,下同),B可以用来制作普通玻璃,化学方程式是____________________,____________________;沉淀C的成分是____________;溶液D中存在较多的阴离子是____________。
(3)沉淀F转化为物质M的化学方程式为________________________;由物质M制取铝的化学方程式为________________________;溶液D中通入过量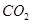 生成沉淀F的离子方程式为________________________。
生成沉淀F的离子方程式为________________________。
查看答案和解析>>
科目: 来源:2011-2012学年云南省芒市中学高一上学期期末考试化学试卷 题型:填空题
(8分)甲、乙、丙三种物质之间有如下转化关系: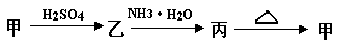
(1)若甲是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是
________ ;写出 乙→丙转化的化学方程式 :___________________________ 。
(2)若乙溶液中加入KSCN溶液,有红色出现,则甲物质是___________;写出 甲→乙转化的离子方程式_________________________________________。
查看答案和解析>>
科目: 来源:2011—2012学年海南省洋浦中学高一第一学期期末考试化学试卷 题型:填空题
(12分)由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转换关系,A是地壳中含量最多的金属元素。请回答: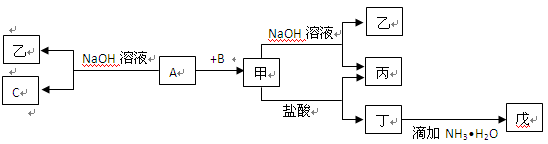
(1)写出下列物质的化学式:乙 、丁 、戊 。
(2)写出甲物质在工业上的一种主要用途: 。
(3)写出甲→乙+丙反应的离子方程式: ;
A→乙+C反应的化学方程式:
查看答案和解析>>
科目: 来源:2012届浙江省杭州市高三第一次高考教学质量检测化学试卷 题型:填空题
(6分)高纯氧化铝可用于制高压钠灯的陶瓷管,实验室制取高纯氧化铝的流程如下: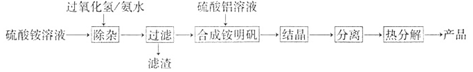
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。检验Fe2+是否除尽的实验操作是 。
(2)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
(3)上述流程图里,“结晶”这步操作中,母液经 得到铵明矾(含结晶水)。
(4)上述流程图里,“分离”这个步骤应包含的是 (填字母代号)
| A.蒸馏 | B.分液 | C.过滤 | D.洗涤晶体 |
查看答案和解析>>
科目: 来源:2012届浙江省杭州市高三第一次高考教学质量检测化学试卷 题型:填空题
(7分)2011年8月12日,《云南信息报》首度披露了云南曲靖铬污染事件,引起全国广泛关注。工业上将制取重铬酸钾(K2Cr2O7)和铬酸酐(CrO3)的剩余废渣称为铬渣,其成分为:SiO2、Al2O3、MgO、Fe2O3、CrO3、K2Cr2O7等。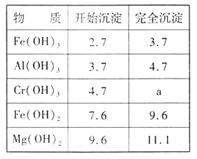
已知:①重铬酸钾和铬酸酐都易溶于水,这是造成铬污染的主要原因,它们都是强氧化剂,铬酸酐溶于水呈酸性;
②+6价铬易被人体吸收,可致癌:+3价铬不易被人体吸收,毒性小。
③右表为一些金属氢氧化物沉淀的pH参照数据。
回答下列处理铬渣、消除铬污染的有关问题:
(1)将铬渣用稀硫酸浸取、过滤,在浸出液中加入适量的绿矾(FeSO4·7H2O),加入绿矾的目的是 。
(2)再向浸出液中缓慢加入烧碱,至pH刚好达到4.7,过滤,所得沉淀的化学式是 ;常温下,Cr(OH)3的溶度积Ksp=10-32,要使Cr3+完全沉淀[c(Cr3+)降至10-5mol·L-1视为沉淀完全],溶液的pH应调于a= 。
(3)向(2)中得到的滤液中加入硫酸,调节至呈强酸性,所得的溶液是含 溶质的溶液。
查看答案和解析>>
科目: 来源:2011-2012学年云南省保山曙光中学高一上学期期末考试化学试卷 题型:填空题
铝是一种重要的金属。
(1)铝在元素周期表中的位置是________。
(2)生产中曾用铝热反应焊接钢轨,铝与氧化铁发生反应的化学方程式为__________________________。
(3)铝与NaOH溶液反应的离子方程式为:__________________________;
同温同压下,在浓度和体积均为100 mL 2 mol/L的盐酸及NaOH溶液中各加入等质量的Al,产生气体的体积比为5:6,则所加Al的质量为________。
查看答案和解析>>
科目: 来源:2011—2012学年度黑龙江大庆实验中学高一上学期期末考试化学试卷 题型:填空题
(8分)
某研究型学习小组为测定镁和铝的混合物中铝的质量分数,称取该混合物a g,溶于200 mL 5 mol/L HCl溶液中,共收集到标准状况下的氢气3.36 L。
(1)a 的取值范围是 。
(2)向反应后所得溶液中逐渐加入4 mol/L的NaOH溶液,当沉淀质量达到最大值时,加入的NaOH溶液的体积是 mL,沉淀的最大质量是 g。(用含a 的代数式表示)
(3)继续加入NaOH溶液至沉淀不再发生变化时,过滤、洗涤并灼烧沉淀至恒重,所得残余固体的质量仍为a g,原混合物中铝的质量分数 。(写出计算过程)
查看答案和解析>>
科目: 来源:2011-2012学年内蒙古包头三十三中高一上学期期末考试化学试卷 题型:填空题
(8分)在50mL bmol·L-1的AlCl3溶液中加入50mL amol·L-1 NaOH溶液。
(1)当a≤3b时,生成Al(OH)3沉淀的物质的量为__________mol。
(2)当a、b满足_________条件时,无沉淀产生。
(3)当a、b满足_________条件时,先有沉淀生成,后又有部分沉淀溶解,此时Al(OH)3的质量为_______克。
查看答案和解析>>
科目: 来源:2011-2012学年广东省增城市高一上学期期末化学试卷 题型:填空题
(本题共20分)混合物A中含有KAl(SO4)2·12H2O、Al2O3和Fe2O3,通过下图所示方法可分离回收Al2O3和Fe2O3:
回答下列问题:
(1)滤渣Ⅰ的主要成分是(填化学式) 。
(2)为了使滤渣Ⅰ中某些成分溶解,便于分离出Fe2O3,所加入的试剂Ⅰ是(填化学式) ,发生反应的离子方程式是: 。
(3)向滤液Ⅰ中加入过量氨水可得到白色沉淀,反应的离子方程式是
。
(4)滤渣Ⅲ的主要成分是(填化学式) ;滤渣Ⅲ在一定条件下反应生成 Al2O3,反应的化学方程式是 。
(5)以Fe2O3为原料,可制备FeCl2溶液,请写出有关的化学反应方程式,试剂任选。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com