
科目: 来源:2008年高考北京理综化学 题型:填空题
由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去):

 (1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填化学式)________________。
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填化学式)________________。 (2)Z为一种或两种气体:
(2)Z为一种或两种气体: ①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是_____________________________。
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是_____________________________。 ②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是______。
②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是______。 (3)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)________________。
(3)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)________________。 (4)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是_______________。
(4)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是_______________。  (5)另取原样品,加入足量稀硫酸充分反应,若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中物质用化学式表示)_________________。
(5)另取原样品,加入足量稀硫酸充分反应,若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中物质用化学式表示)_________________。
查看答案和解析>>
科目: 来源:2008年普通高等学校招生统一考试理综试题化学部分(山东卷) 题型:填空题
钢铁工业对促进经济和社会发展起了重要作用。



 (1)炼铁高炉分为五部分,铁矿石与高温煤气主要在 部分发生反应,在 部分开始生成铁和炉渣。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在 部分发生反应,在 部分开始生成铁和炉渣。 (2)炼钢时,除磷的化学方程式为 ;
(2)炼钢时,除磷的化学方程式为 ; 加入硅、锰和铝的目的是 。
加入硅、锰和铝的目的是 。 (3)不锈钢含有的Cr元素是在炼钢过程的氧吹 (填“前”或“后”)加入,原因是 。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹 (填“前”或“后”)加入,原因是 。 (4)炼铁和炼钢生产中,尾气均含有的主要污染物是 。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是 。 从环保和经济角度考虑,上述尾气经处理可用作 。
从环保和经济角度考虑,上述尾气经处理可用作 。
查看答案和解析>>
科目: 来源:2007年普通高等学校招生全国统一考试(广东卷)化学试题 题型:填空题
已知某混合金属粉末中,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。 仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol·L-1硫酸、2mol·L-2硝酸、2mol·NaOH溶液、20%KSCN溶液。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol·L-1硫酸、2mol·L-2硝酸、2mol·NaOH溶液、20%KSCN溶液。 完成以下实验探究过程:
完成以下实验探究过程: (1)提出假设:
(1)提出假设: 假设1:该混合金属粉末中除铝外还含有 元素;
假设1:该混合金属粉末中除铝外还含有 元素; 假设2:该混合金属粉末中除铝外还含有 元素;
假设2:该混合金属粉末中除铝外还含有 元素; 假设3:该混合金属粉末中除铝外还含有Fe、Cu元素;
假设3:该混合金属粉末中除铝外还含有Fe、Cu元素; (2)设计实验方案基于假设3,设计出实验方案(不要在答题卡上作答)。
(2)设计实验方案基于假设3,设计出实验方案(不要在答题卡上作答)。 (3)实验过程
(3)实验过程 根据(2)的实验方案,叙述实验操作、预期现象和结论。
根据(2)的实验方案,叙述实验操作、预期现象和结论。 【提示】Ⅰ.在答题卡上按以下方式作答,注意前后内容对应;
【提示】Ⅰ.在答题卡上按以下方式作答,注意前后内容对应; Ⅱ.注意文字简洁,确保不超过答题卡空间。
Ⅱ.注意文字简洁,确保不超过答题卡空间。
查看答案和解析>>
科目: 来源:2012-2013学年浙江省宁波万里国际学校高一下期末考试文科化学试卷(带解析) 题型:填空题
(1)写出工业上用过量CO2与偏铝酸钠溶液反应制氢氧化铝的离子方程式 。
(2)写出乙醇、乙酸与浓硫酸加热反应的方程式 。
查看答案和解析>>
科目: 来源:2013年全国普通高等学校招生统一考试理科综合能力测试化学(大纲卷带解析) 题型:填空题
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下: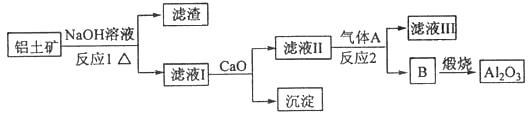
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下: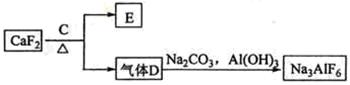
回答下列问题:
(1)写出反应1的化学方程式 , ;
(2)滤液Ⅰ中加入CaO生成的沉淀是 ,反应2的离子方程式为 ;
(3)E可作为建筑材料,化合物C是 ,写出由D制备冰晶石的化学方程式 ;
(4)电解制铝的化学方程式是 ,以石墨为电极,阳极产生的混合气体的成分是 。
查看答案和解析>>
科目: 来源:2013年全国普通高等学校招生统一考试理科综合能力测试化学(北京卷带解析) 题型:填空题
用含有A1203、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是
(2)KMnO4 - 氧化Fe2+的离子方程式补充完整: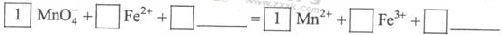
(3)已知:
生成氢氧化物沉淀的pH
| | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目: 来源:2013年全国普通高等学校招生统一考试化学(上海卷带解析) 题型:填空题
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。完成下列填空:
(1)铝原子核外电子云有 种不同的伸展方向,有 种不同运动状态的电子。
(2)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式。
(3)硅与铝同周期。SiO2是硅酸盐玻璃(Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成Na2O·CaO·6SiO2。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 。
长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为
(4)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:
2Al+4BaO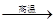 3Ba↑+BaO·Al2O3
3Ba↑+BaO·Al2O3
常温下Al的金属性比Ba的金属性 (选填“强”“弱”)。利用上述方法可制取Ba的主要原因是 。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
查看答案和解析>>
科目: 来源:2013届上海市金山区高三上学期期末考试化学试卷(带解析) 题型:填空题
证明Al2O3具有两性的反应事实是______________________(用离子方程式表示)。
查看答案和解析>>
科目: 来源:2013届山东省聊城市某重点中学高三下学期期初考试化学试卷(带解析) 题型:填空题
铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下图所示,请回答有关问题: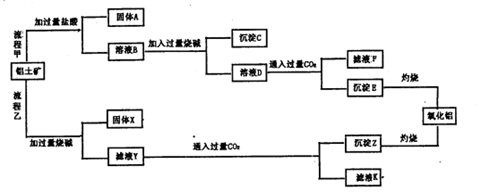
(1)流程乙加入烧碱后发生反应的离子方程式: .
(2)溶液D到沉淀E发生的离子方程式: 。
(3)验证滤液B含Fe3+,可取少量滤液并加入 。
(4)滤液K中溶质的主要成份是 (填化学式)。
查看答案和解析>>
科目: 来源:2012-2013学年山东省威海市高一上学期期末考试化学试卷(带解析) 题型:填空题
现有100mL AlCl3与MgSO4的混合溶液,分成两等份。
(1)向其中一份中加入10mL 4mol/L的氨水,恰好完全反应,其中AlCl3与氨水反应的离子方程式是 。继续加入l mol/L NaOH溶液至10mL时,沉淀不再减少,沉淀减少的离子方程式是 ,剩余的沉淀的物质的量是 。
(2)向另一份中加入a mL 0.1mol/LBaCl2溶液能使SO42-沉淀完全,a= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com