
科目: 来源:2010年沙河一中考前预测卷化学试题 题型:填空题
(12分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2 6SO2+Fe3O4,氧化产物为 ,若有3 mol FeS2参加反应,转移 mol电子。
6SO2+Fe3O4,氧化产物为 ,若有3 mol FeS2参加反应,转移 mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
。
(3)与明矾相似,硫酸铁也可用作净水剂,其原理为 (用离子方程表示)
(4)①钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。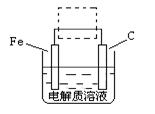
②写出修改前的钢铁吸氧腐蚀石墨电极的电极反应式 。
(5)铁红是一种红色颜料,其成分是Fe2O.3将一定量的铁红溶于160ml5 mol·L—1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为 。
查看答案和解析>>
科目: 来源:2010年普通高等学校招生全国统一考试理综化学部分(新课标全国I卷) 题型:填空题
[化学——选修化学与生活](15分)
(Ⅰ)合金是生活中常用的材料,请回答下列问题:
(1)生铁和钢是含碳量不同的铁碳合金,含碳量在2%~4.3%的称为 。不锈钢在空气中比较稳定,不易生锈,有强的抗腐蚀能力,其合金元素主要是 ; (2)钢铁的腐蚀给社会造成的损失是巨大的,所以采取各种措施防止钢铁的腐蚀是十分必要的,请列举三种防止钢铁腐蚀的方法 ;
(3)青铜的主要合金元素为 ,黄铜的主要合金元素为 :
(4)储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料。如镧镍合金,它吸收氢气可结合成金属氢化物,其化学式可近似地表示为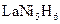 (
(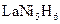 中各元素化合价均可看作是零),它跟
中各元素化合价均可看作是零),它跟 可组成镍氢可充电电池:
可组成镍氢可充电电池: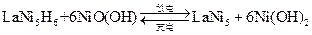
该电池放电时,负极反应是 。市面上出售的标称容量为2000 mA h的1节镍氢电池至少应含有镧镍合金 g(已知1法拉第电量为96500库仑或安培·秒)。
(Ⅱ)有机化合物与生活息息相关。请回答下列有关问题:
(1)棉花、蚕丝、小麦主要成分分别为 、 、 ,它们蕃都属于天然有机高分子化合物;
(2)味精是烹饪常用的调味品,其主要成分的化学名称为 ;
(3)解热镇痛药阿司匹林主要成分的结构简式为 。
查看答案和解析>>
科目: 来源:2009-2010学年度唐山二中高二第二学期期中化学试卷 题型:填空题
(共12分)FeCl3可通过多种途径转化为FeCl2。
(1)在FeCl3溶液中加入适量氢碘酸,发生反应的离子方程式为
(2)工业上常将无水FeCl3在氮气做保护气下加热至300℃―350℃,通入干燥H2,而制得FeCl2。该反应的化学反应方程式为
(3)工业上另一种制备FeCl2的方法是:将无水FeCl3与适量氯苯(C6H5Cl)混合,在130℃持续加热约3小时,可发生如下反应:
依据有机反应规律,该反应中氯苯发生的是 (填有机反应类型)。
(4)分析上述三个反应,下列有关说法正确的是 (填序号)。
①反应(1)中,氢碘酸既表现了酸性,又表现了还原性
②反应(3)中,HCl为氧化产物
③上述三个反应中,FeCl2均为还原产物
(5)请另写出一个FeCl3转化成FeCl2的化学方程式:
查看答案和解析>>
科目: 来源:2012-2013学年北京市西城区(北区)高一上学期期末考试化学试卷(带解析) 题型:填空题
经精选后的铝土矿A(主要成份为Al2O3,含有一定量的Fe2O3、SiO2杂质),可用A来制备电解铝原料——氧化铝,某课外小组同学模拟该过程,设计了如下方案: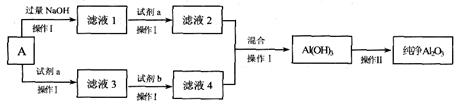
请回答:
(1)A中Al2O3与过量氢氧化钠溶液反应的化学方程式是________________
(2)操作I的名称是________________。
(3)下列说法中正确的是________(填选项)。
a 操作Ⅱ是灼烧 b. 滤液3所含阳离子是Fe3+、Al3+
c. 试剂b可用氢氧化钠 d. 为保证转化完全,所加试剂a和试剂b均应过量
(4)写出滤液2、4混合后生成Al(OH)3的离子方程式是______________________ __
查看答案和解析>>
科目: 来源:2012-2013学年新疆兵团农二师华山中学高一上学期期末考试化学试卷(带解析) 题型:填空题
将一定质量的镁铝合金样品全部溶于100mL某浓度的盐酸中。向所得溶液中滴加5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如右图所示。求: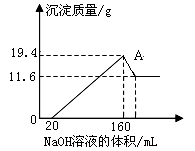
(1)A点沉淀物的化学式为 _ 。
(2)原合金中的Mg 、Al质量各多少克?
(3)盐酸的物质的量浓度。
查看答案和解析>>
科目: 来源:江苏省南通市2010届高三第一次模拟考试化学试 题型:填空题
(12分)实验室制备甲酸铜晶体[Cu(HCOO)2·4H2O]的流程如下: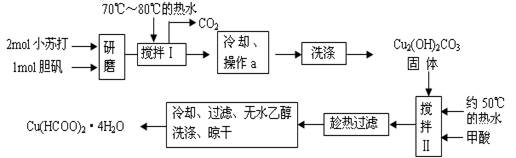
回答下列问题:
(1)生成碱式碳酸铜[Cu2(OH)2CO3]的离子方程式为 。
(2)操作a的名称是 ,该操作使用的玻璃仪器有 。
(3)证明碱式碳酸铜沉淀已经洗涤充分的实验操作是 ;“趁热过滤”的原因是 ;
(4)用无水乙醇洗涤晶体的目的是 。
查看答案和解析>>
科目: 来源:北京市朝阳区2010年高三一模(理科综合)化学部分 题型:填空题
(14分)铜及其化合物在生产、生活中有广泛的应用。
(1)铜可采用如下方法制备:
火法炼铜:Cu2S+O2 2Cu+SO2
2Cu+SO2
湿法炼铜:CuSO4+Fe=====FeSO4+Cu
上述两种方法中,铜元素均被 (填“氧化”或“还原”)成铜单质。
(2)印刷电路板上使用的铜需要回收利用。
方法一:用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如下: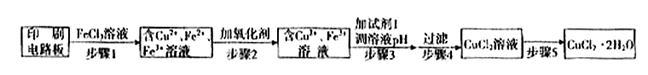 ①证明步骤I所加FeCl3溶液过量的方法是 。
①证明步骤I所加FeCl3溶液过量的方法是 。
②步骤2中所加的氧化剂最适宜的是 。
A.HNO3 B.H2O2 C.KMnO4
③步骤3的目的是使溶液的pH升高到4.2,此时Fe3+完全沉淀,可选用的“试剂1”是 。(写出一种即可)
④蒸发农缩CuCl2溶液时,要滴加浓盐酸,目的是 (用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl2·2H2O。
方法二:用H2O2和稀硫酸共同浸泡印刷电路板制备硫酸铜时,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(nq)===CuSO4(aq)+2H2O(l)△H1=-320kJ/mol
又知:2H2O2(l)==2H2O(l)+O2(g) △H2=-196kJ/mol
H2(g)+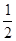 O2(g)==H2O(l) △H3=-286kJ/mol
O2(g)==H2O(l) △H3=-286kJ/mol
则反应Cu(s)+H2SO4(aq)==CuSO4(aq)+H2(g)的△H= 。
(3)欲实现反应Cu+H2SO2==CuSO4+H2,在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”)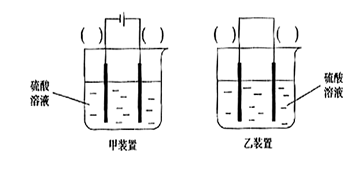
查看答案和解析>>
科目: 来源:杭高2010届高三第二次月考化学试卷 题型:填空题
(9分)铜在自然界存在于多种矿石中,如:
| 矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3·Cu(OH)2 |
 6Cu+SO2↑,反应的氧化剂是 。
6Cu+SO2↑,反应的氧化剂是 。| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铜绿的主成分是碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
| B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
| C | 铁比铜活泼 | 例在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
| D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
查看答案和解析>>
科目: 来源:2009高考真题汇编-几种重要的金属 题型:填空题
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。

 (1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
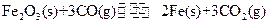
 ①该反应的平衡常数表达式为:K=
①该反应的平衡常数表达式为:K=  ②该温度下,在2L盛有
②该温度下,在2L盛有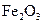 粉末的密闭容器中通入CO气体,10min后,生成了单
粉末的密闭容器中通入CO气体,10min后,生成了单 质铁11.2g。则10min内CO的平均反应速率为
质铁11.2g。则10min内CO的平均反应速率为  (2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态: ① ②
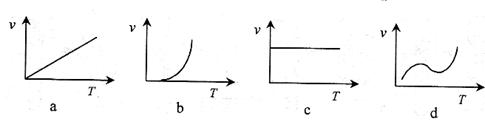
① ②  (3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v) 和温度(T)的关系示意图中与铝热反应最接近的是 。
和温度(T)的关系示意图中与铝热反应最接近的是 。
 (4)写出氢氧化铝在水中发生酸式电离的电离方程式:
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:  欲使上述体系中
欲使上述体系中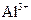 浓度增加,可加入的物质是 。
浓度增加,可加入的物质是 。
查看答案和解析>>
科目: 来源:2008年普通高等学校招生统一考试理综试题化学部分(宁夏卷) 题型:填空题
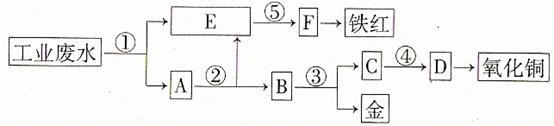
某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。




 填写下面空白。
填写下面空白。 (1)图中标号处需加入的相应物质分别是① 、② 、③ 、④ 、⑤ ;
(1)图中标号处需加入的相应物质分别是① 、② 、③ 、④ 、⑤ ; (2)写出①处发生反应的离子方程式 ;写出③处发生反应的化学方程式 ;
(2)写出①处发生反应的离子方程式 ;写出③处发生反应的化学方程式 ; (3)铁红的化学式为 ;分别写出铁红和氧化铜在工业上的一种主要用途:铁红 ;氧化铜 。
(3)铁红的化学式为 ;分别写出铁红和氧化铜在工业上的一种主要用途:铁红 ;氧化铜 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com