
科目: 来源:2011-2012学年江苏省泰州中学高三化学期中化学试卷 题型:填空题
(16分)三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)是一 种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
(1)铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250ml溶液。
步骤二:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02ml,滴定中MnO4-,被还原成Mn2+ 。
重复步骤二、步骤三操作,滴定消耗0.010mol/L KMnO4溶液19.98ml
请回答下列问题:
① 配制三草酸合铁酸钾溶液的操作步骤依次是: 称量、__▲_____、转移、洗涤并转移、____▲____摇匀。
称量、__▲_____、转移、洗涤并转移、____▲____摇匀。
② 加入锌粉的目的是___▲_____。
③ 写出步骤三中发生反应的离子方程式___▲_____。
④ 实验测得该晶体中铁的质量分数为_____▲____。在步骤二中,若加入的KMnO4的溶液的量不够,则测得的铁含量___▲____。(选填“偏低 ”“偏高”“不变”)
”“偏高”“不变”)
(2)结晶水的测定
将坩埚洗净,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至110℃,恒温一段时间,置于空气中冷却,称量并记录 质量;计算结晶水含量。请纠正实验过程中的两处错误;___▲_____;_____▲____。
质量;计算结晶水含量。请纠正实验过程中的两处错误;___▲_____;_____▲____。
查看答案和解析>>
科目: 来源:2012届河北省衡水中学高三第三次调研考试化学试卷 题型:填空题
(13分)(Ⅰ)W、X、Y、Z是周期表前36号元素中的四种常见元 素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的
素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的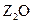 和黑色的ZO两种氧化物。
和黑色的ZO两种氧化物。
(1)W位于元素周期表第_________周期第_________族。
W的气态氢化物稳定性比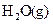 __________(填“强”或“弱”)。
__________(填“强”或“弱”)。
(2)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
_________________________________________________________________________。
(3) 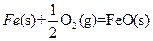
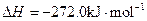
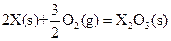
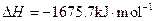
X的单质和FeO反应的热化学方程式是_________________________________________。
(Ⅱ)已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为____________ __
(2)Y元素原子的价层电子的轨道表示式为____________ _
(3)X与Z可形成化合物XZ3,该化合物的空间构型为_____ ___
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是________________________________________。
查看答案和解析>>
科目: 来源:2012届黑龙江省大庆铁人中学高三上学期期中考试化学试卷 题型:填空题
(8分)请回答下列各问:
(1)酸雨的pH范围是 ,在空气质量报告的各项指标中有可吸入颗粒物,还有 。
(2)石灰法是目前应用最广泛的工业废气脱硫方法,过程如下:通过煅烧石灰石得到生石灰,以生石灰为脱硫剂在吸收塔中与废气中的SO2反应而将硫固定,写出反应的化学方程式 。
(3)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是 (填序号)。
① Cu + HNO3(浓)→ Cu(NO3)2
② Cu + HNO3(稀)→ Cu(NO3)2
③ Cu  CuO
CuO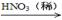 Cu(NO3)2
Cu(NO3)2
(4)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是 。
| A.40.32L | B.30.24L | C.20.16L | D.13.44L |
查看答案和解析>>
科目: 来源:2012届黑龙江省伊春市马永顺中学高三11月月考化学试卷 题型:填空题
现有铁和铜组成的合金共a mol,其中铜的物质的量分数为x。将此合金研成粉末状后全部投入含b mol硝酸的稀溶液中,微热使其充分反应,硝酸的还原产物只有NO。
(1)用粒子符号填写下列空白(列举出全部可能出现的情况):
| 组序 成 分 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 残留固体成分 | | | | | | [ |
| 溶液中金属离子 | | | | | | |
查看答案和解析>>
科目: 来源:2012届黑龙江省伊春市马永顺中学高三11月月考化学试卷 题型:填空题
现有浓度各为2 mol/L的FeCl3、FeCl2、CuCl2混合溶液100 mL,加入一定量的铁粉,按下列情况填空。
(1)充分反应后,无固体存在,则溶液中一定含有的金属阳离子是 。
(2)反应完毕后,铁粉有剩余,过滤所得的固体物质为 ,溶液中一定含有的金属离子的物质的量为 mol。
(3)反应完毕,有固体剩余,则反应后的溶液中一定有的金属阳离子为 ,其物质的量取值范围是 。
查看答案和解析>>
科目: 来源:2011-2012学年江西省赣州市(十一县市)高三第一学期期中联考化学试卷 题型:填空题
(10分) 根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):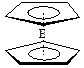

⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
⑵某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 、 。
⑶写出Cl2将Z氧化为K2EO4的化学方程式: 。
⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为: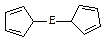 。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
查看答案和解析>>
科目: 来源:2011-2012学年湖北省黄冈中学高一上学期期中考试化学试卷 题型:填空题
(6分) 铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是 ________(用字母代号填)。
| A.Fe | B.FeCl3 | C.FeSO4  | D.Fe2O3 |
查看答案和解析>>
科目: 来源:2011-2012年学山东省莱州一中高三上学期模块检测化学试卷 题型:填空题
铁及铁的化合物应用广泛,如 可用作印刷电路铜板腐蚀剂。
可用作印刷电路铜板腐蚀剂。
(1)写出 溶液腐蚀印刷电路铜板的离子方程式 。
溶液腐蚀印刷电路铜板的离子方程式 。
腐蚀铜板后的混合溶液中,若 、
、 的浓度均为
的浓度均为 ,不考虑溶液体积的变化,则原
,不考虑溶液体积的变化,则原 溶液的浓度为 。
溶液的浓度为 。
(2)某化学小组在实验室按照下列操作分离腐蚀铜板后的混合液并制取有关物质,图示如下:
请回答下列问题:
①试剂X为 ;试剂Y为 ;操作M为
。
②固体c的化学式为 。
③检验混合溶液B中是否存 的操作是
的操作是
。
查看答案和解析>>
科目: 来源:2011-2012年云南省建水一中高二上学期期中考试化学(文)试题 题型:填空题
(6分)某化学兴趣小组用铁矿石(主要成分为Fe2O3,还有SiO2、A12O 3等杂质)提取。操作讨程如下: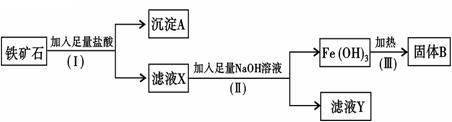
(1)(I)和(Ⅱ)步骤中分离溶液和沉淀的操作名称是 ;
(2)沉淀A中主要含有 ,固体B是 ;
(3)滤液Y中的阴离子除OH-、Cl-外,还有 ;
(4)写出(III)步骤中生成B的化学方程式 。
查看答案和解析>>
科目: 来源:2012届黑龙江省哈师大附中高三上学期期中考试化学试卷 题型:填空题
(10分)化学研究性学习小组拟通过实验探究“新制的还原性铁粉和过量盐酸反应生成FeCl2还是FeCl3”。请你参与探究并回答有关问题:
(1)一位同学用向反应后的溶液中滴加NaOH溶液的方法来验证溶液中含有Fe2+。①可观察到的实现现象是___________,②反应过程中发生反应的化学方程式是______________。
(2)另一位同学向反应后的溶液中先滴加KSCN溶液,再向其中滴加新制氯水,溶液呈现红色,但当滴加过量新制氯水时,却发现红色褪去。为了弄清溶液红色褪去的原因,同学们查到如下资料:
Ⅰ.铁有一种化合物 称为铁酸盐(含有FeO42-)。
称为铁酸盐(含有FeO42-)。
Ⅱ.SCN-的电子式为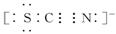
Ⅲ.氯水具有很强的氧化性。
于是同学们提出两种假设:
①第一种假设是:Cl2可将Fe 3+氧化为FeO42-,请写出该离子反应方程式__________。
3+氧化为FeO42-,请写出该离子反应方程式__________。
②第二种假设是:____________,提出该假设的理论依据是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com