
科目: 来源:2013届安徽省望江二中高三第三次月考化学试卷(带解析) 题型:填空题
(10分)向含有0.8 mol的稀硝酸中慢慢加入22.4 g的铁粉,假设反应分为两个阶段。
第一阶段为:Fe+HNO3(稀)―→Fe(NO3)3+NO↑+H2O
(1)写出这两个阶段发生反应的离子方程式:
第一阶段: 。
第二阶段: 。
(2)正确表达这两个阶段反应中,加入铁粉的物质的量与溶液中铁元素存在的形式的关系
。
(3)在图中画出溶液中Fe2+、Fe3+、NO的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量)。
查看答案和解析>>
科目: 来源:2013届山东省新泰市汶城中学高三12月月考化学试卷(带解析) 题型:填空题
(6分)铁及其化合物之间的相互转化可用下式表示: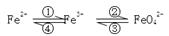
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净。可选用的试剂是 (选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S(CuFeS2中S为-2价)。
则下列说法正确的是 (选填序号);
a.从物质的组成来看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1 mol e- 时,有46 g CuFeS2参加反应
(3)高铁酸钾是一种新型、高效的绿色净水剂,其净水原理是 。
查看答案和解析>>
科目: 来源:2012-2013学年河北省邢台一中高一上学期第三次月考化学试卷(带解析) 题型:填空题
(12分)FeCl3溶液棕黄色,对此溶液,分别做如下实验,请填表:
| 编号 | 实践操作 | 实验主要现象 | 离子方程式 |
| ① | 加入过量 铁粉 | | |
| ② | 加入少量Na2O2粉末 | | |
| ③ | 加入少量AgNO3溶液 | | |
查看答案和解析>>
科目: 来源:2012-2013学年甘肃省武威第五中学高一11月月考化学试卷(带解析) 题型:填空题
(8分)已知有以下物质相互转化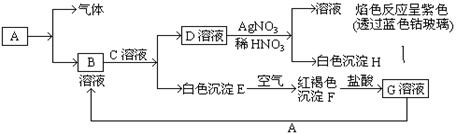
试回答:(1)写出B的化学式 ,D的化学式 。
(2)写出由E转变成F的化学方程式 。
(3)写出F转化成G的离子方程式 ;
查看答案和解析>>
科目: 来源:2012-2013学年山东省日照市某高中高一上学期期中考试化学试卷(带解析) 题型:填空题
(14分)(1)在盛有2mLFeCl3溶液的试管中加入足量铁粉,充分反应后,溶液由________色变为_________色,化学反应方程式为____________________________。
(2)再滴入2滴KSCN溶液,溶液颜色_______________;再加入几滴氯水,观察溶液颜色变为_________,说明_____________________,反应方程式为 ____________________
查看答案和解析>>
科目: 来源:2013届江苏省泰州中学高三上学期期中考试化学试卷(带解析) 题型:填空题
(12分)工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下: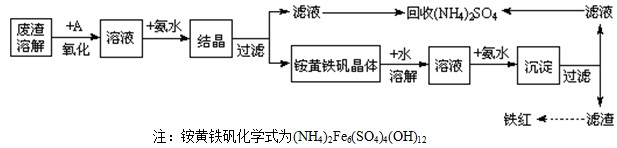
(1)在废渣溶解时需要使用酸,应选用__________,为了提高废渣的浸取率,可采用的措施有哪些?
_____________________________________________________________(至少写出两点)。
(2)物质A是一种氧化剂,工业上最好选用_____________(供选择使用的有:空气、Cl2、MnO2),其理由是 (至少写出两点)。
(3)“结晶”反应的化学方程式为__________________________________________________。
(4)上述生产流程中多处采用了过滤操作,实验室中完成相应的操作需要用到的玻璃仪器有烧杯及____________________________________________。
查看答案和解析>>
科目: 来源:2012-2013学年甘肃省甘谷一中高一第二次月考化学试卷(带解析) 题型:填空题
(12分)已知有以下物质相互转化
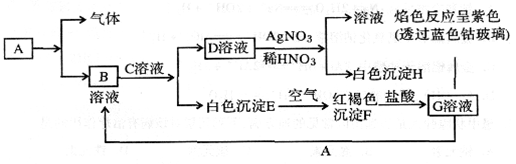
试回答:
(1)写出B的化学式__________;D的化学式__________。
(2)写出由E转变成F的化学方程式_______________________________。
(3)写出用KSCN鉴别G溶液的现象_________;向G溶液加入A的有关离子反应方程式_________________________________________。
查看答案和解析>>
科目: 来源:2013届福建安溪一中、养正中学高三上学期期中联考化学试卷(带解析) 题型:填空题
(12分)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式。可用离子交换和滴定的方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预防处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量为________mol,并求出FeClx中X值为__________。
(2)现有一含有FeCl2和FeCl3的混合样品,采用上述方法测得n(Fe): n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为____________。在实验室中,FeCl2可用铁粉和__________反应制备,FeCl3可用铁粉和_______反应制备
(3)铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。
①写出制取铁酸钠的化学方程式: 。
②铁酸钠之所以有净水作用,除杀菌外,另一个原因是 。
查看答案和解析>>
科目: 来源:2013届甘肃天水市一中高三第一次学段考试化学试卷(带解析) 题型:填空题
(10分) A、B、C、D、E、F、G七种物质间存在如图所示转化关系,其中A、B、D、G含有同种元素。已知:A为金属单质,C为黄绿色气体;D能将某种非金属氧化物氧化为F,F是含有三种元素的化合物。请回答下列问题: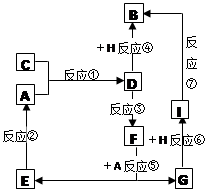
(1) 以上反应中属于化合反应的是___________________ (填序号)
(2) G生成B的过程中所出现的现象
(3)反应⑦的化学方程式为_________________________________
(4)反应③的离子方程式
(5)D的水溶液显_____性,请用离子方程式解释原因 ____________________
查看答案和解析>>
科目: 来源:2013届甘肃天水市一中高三第一次学段考试化学试卷(带解析) 题型:填空题
(9分) 高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上可以通过NaClO氧化法制备Na2FeO4,生产过程如下:
回答下列问题:
(1)经过步骤①后,加入NaOH固体的原因是____ _____________________________
(2)步骤②反应的离子方程式是_____ _____
(3)从溶液Ⅰ中分离出Na2FeO4后,还有副产品Na2SO4、NaCl,则步骤③中反应的离子方程式为___
(4)将一定量的Na2FeO4投入到pH不同的污水中(污水中其余成分均相同),溶液中Na2FeO4浓度变化如图曲线Ⅰ、Ⅱ所示,试推测曲线I比曲线II对应的污水pH____(填“高”或“低”)。
(5)通过计算得知Na2FeO4的消毒效率(以单位质量得到的电子数表示)比Cl2的_____(“高”或“低”),用Na2FeO4代替Cl2作净水消毒剂的优点是____ (答出两点即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com