
科目: 来源:西南师大附中2010届高三第五次月考(理综)试题化学部分 题型:填空题
钛(Ti)被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。请填写下列空白: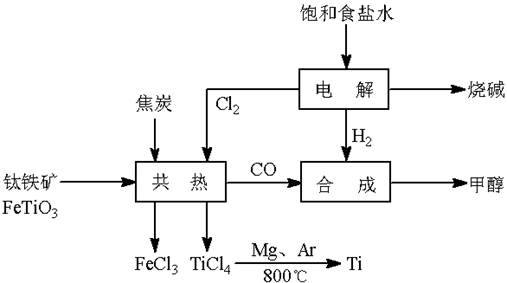
(1)电解饱和食盐水时,阳极的电极反应为 。
(2)写出钛铁矿与焦炭、Cl2共热制得四氯化钛的化学方程式________________________。
(3)已知:①Mg(s) + Cl2(g)=MgCl2(s);△H =" –" 641 kJ/mol ②Ti(s) + 2Cl2(g)=TiCl4(s);△H =" –770" kJ/mol
②Ti(s) + 2Cl2(g)=TiCl4(s);△H =" –770" kJ/mol
则2Mg(s) + TiCl4(s)=2MgCl2(s) + Ti(s);△H= 。 反应2Mg(s) + TiCl4(s)
反应2Mg(s) + TiCl4(s) 2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是 。
2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是 。
(4)在上述产业链中,合成96 t 甲醇理论上消耗H2 t (不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH + 3O2 + 4OH-=2CO32-+ 6H2O。该燃料电池发生反应时正极区溶液的pH (填“增大”、“减小”或“不变”),该电池中负极上的电极反应是________________________________________________。
查看答案和解析>>
科目: 来源:鲁版必修1第04章第3节复合材料 题型:填空题
根据某种分类标准,材料大体可以分为天然材料、烧炼材料、合成材料等。下面是一个分类的实例。
| 类型 | 天然材料 | 烧炼材料 | 合成材料 |
| 名称 | 木材、大理石、皮革 | 钢铁、陶瓷、铝 | 合成纤维、合成橡胶、合成塑料 |
| 类型 | |
| 名称 | |
查看答案和解析>>
科目: 来源:鲁版必修1第04章第3节复合材料 题型:填空题
普通玻璃、钢铁和玻璃钢是三种不同的材料,它们在性能方面差别很大。请根据学过的知识,回答下面问题。
(1)普通玻璃的成分是 ;
(2)铁在人类的生产和生活中有着十分重要的应用。铁的应用,经历了 到 到 的演变过程。
(3)某种复合材料具有耐高温,强度高,导电性好,导热性好的特点,估计该复合材料的基体和增强体材料可能分别是
| A.金属;C |
| B.陶瓷;SiO2 |
| C.合成树脂;SiO2、Al2O3、MgO |
| D.合成树脂;C |
查看答案和解析>>
科目: 来源:2012-2013学年山西省山大附中高一下学期期中考试化学试卷(带解析) 题型:填空题
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。指出电解质溶液是__________,正极电极反应式为__________________。
(3)写出甲醇(CH3OH)—空气碱性燃料电池(KOH作为电解质溶液)的负极反应式:_______________________________。
查看答案和解析>>
科目: 来源:2012-2013学年天津市天津一中高一上学期期末考试化学试卷(带解析) 题型:填空题
把等物质的量的Cu、Fe粉投入一定量的FeCl3溶液中充分反应后取出部分溶液,
(1)若滴加一滴KSCN溶液,溶液显红色,则溶液中存在的离子有_________。
(2)若加一滴KSCN溶液,溶液不显红色,则溶液中一定存在的离子有_________,可能存在的金属粉末有_________。
(3)若加入的金属全部溶解,则溶液中n(Cu2+):n(Fe2+)是_________。
(4)若(3)反应后的溶液中有3种金属离子,欲从中回收Cu和FeCl3,需要用到的试剂有(按反应顺序填写)___________________________________。
查看答案和解析>>
科目: 来源:2013届福建省清流一中高三第三阶段考试化学试卷(带解析) 题型:填空题
铜、铜的氧化物及铜的氢氧化物都是常用的化学试剂。已知红色的氧化亚铜Cu2O在酸性溶液中发生自身氧化还原反应生成Cu2+和Cu,Cu2O在空气中灼烧生成CuO。含有醛基的有机物与新制的氢氧化铜共热会出现Cu2O红色沉淀,某化学兴趣小组对此提出质疑,认为红色沉淀还可能是Cu2O和Cu的混合物,为了验证上述猜测,他们设计了如下三个方案:
| 方案甲 | 取该红色沉淀溶于稀硫酸中,观察是否有残渣。 |
| 方案乙 | 取该红色沉淀溶于稀硝酸中,观察溶液颜色。 |
| 方案丙 | 称取红色沉淀a g,在空气中充分灼烧至完全变黑,并在干燥器中冷却,再称重,反复多次直到固体恒重称的固体质量为b g,比较a和b的关系。 |
查看答案和解析>>
科目: 来源:2012-2013学年福建省清流一中高一第三阶段试化学试卷(带解析) 题型:填空题
已知氯化铁溶液跟铜反应生成氯化铜和氯化亚铁。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是 ,证明Fe3+存在的现象是 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式(1分):
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤: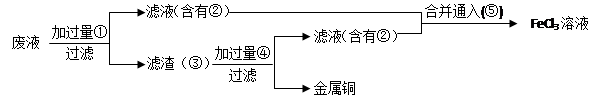
A.请写出上述实验中加入或生成的有关物质的化学式:
① ,② ,④ ,
B.请写出含有②的滤液与⑤反应的离子方程式(1分):
该反应中氧化剂为 还原剂为 。
查看答案和解析>>
科目: 来源:2012-2013学年福建省三明一中、二中高一上学期期末联考化学试卷(带解析) 题型:填空题
已知A、B、C为中学化学中常见的单质, A为是生产、生活中用量最大、用途最广的金属单质,室温下B是黄绿色气体,C为无色气体。在一定条件下相互转化的关系如图所示。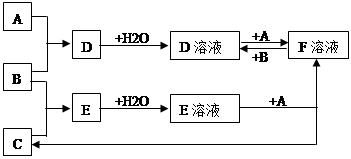
请回答以下问题:
(1)A、B、C分别是什么物质:A是 ,B是 ,C是 ,F是 (填化学式)
(2)写出A和B生成D的化学方程式: ,向D溶液中加
入 溶液可看到溶液变血红色。
(3)写出F溶液中加入B的离子方程式:
查看答案和解析>>
科目: 来源:2011-2012学年云南景洪第一中学高一上期末考试化学试卷(带解析) 题型:填空题
金属铁在空气中缓慢氧化生成的产物是 (化学式),在O2中燃烧生成的产物是 (化学式),铁与水蒸气发生反应的化学方程式是
查看答案和解析>>
科目: 来源:2012-2013学年山东省济南市高一上学期期末考试化学试卷(带解析) 题型:填空题
(8分)将过量的铜置入一定量的浓硝酸中,微热,充分反应后,放出1.12 L气体(标准状况下),试回答下列问题:
(1)反应放出的气体中,含有 和 (写化学式)。
(2)完全反应后,所得溶液中的溶质是 。
(3)写出反应过程其中1个化学反应的化学方程式: 。
(4)整个反应过程中,被还原的HNO3总的物质的量是 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com