
科目: 来源:2012-2013学年北京市东城区(南片)高一上学期期末考试化学试卷(带解析) 题型:问答题
(5分)使生产不同产品的部分生产过程形成联产,不仅有利于降低产品的生产成本,有时也有利于某些废弃物的综合利用。故人们常把具有这种关系的工厂尽可能地建在相邻区域。请对以下两个实例进行解释:
(1)石灰石采石场和炼铁厂建在相邻区域;
(2)海水制盐场和氯碱化工厂建在相邻区域。(信息:氯碱化工厂主要化学反应为电解饱和食盐水:2NaCl+2H O
O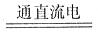 2NaOH+Cl
2NaOH+Cl
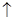 +H
+H
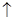 )
)
查看答案和解析>>
科目: 来源:2012-2013学年四川省雅安中学高一上学期入学模拟考试化学试卷(带解析) 题型:问答题
(6分)“物质的组成和结构决定物质性质,物质的性质决定了物质的用途”。请分析:
(1)金刚石很硬,而石墨却很软。原因是
。
(2)氢氧化钠和氢氧化钡溶液都能使无色酚酞试液变红。原因是
。
(3)CO具有可燃性,可以做燃料;CO具有还原性,可以用来 。
(答一点即可)
查看答案和解析>>
科目: 来源:2012届四川省成都树德中学高考适应考试(一)理科综合化学试卷(带解析) 题型:问答题
(15分)铁及其化合物在日常生活、生产中应用广泛。研究铁及其化合物的应用意义重大。
I.水体的净化和污水的处理与铁及其化合物密切相关。
(1)自来水厂常用高铁酸钠(Na2FeO4)改善水质。简述高铁酸钠用于杀菌消毒同时又起到净水作用的原理___________。
(2)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
①写出反应I中发生的氧化还原反应的离子方程式___________。
②加入少量NaHCO3的目的是调节溶液pH,应控制pH的范围为____________。
③在实际生产中,反应II常同时通入O2以减少NaNO2的用量,若通入5.6L O2(标准状况),则相当于节约NaNO2的质量为____________g。
④碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成[Fe2(OH)4]2+聚合离子。该水解反应的离子方程式为___________。
II铁的化合物也是制备高能锂电池的重要原料。已知磷酸亚铁锂电池总反应为:
FePO4+Li LiFePO4,电池中的固体电解质可传导Li+。试写出该电池充电时的阳极反应式____________。常温下以该电池为电源电解200mL饱和食盐水,当消耗1.4g Li时,溶液的pH为____________。(忽略溶液的体积变化)。
LiFePO4,电池中的固体电解质可传导Li+。试写出该电池充电时的阳极反应式____________。常温下以该电池为电源电解200mL饱和食盐水,当消耗1.4g Li时,溶液的pH为____________。(忽略溶液的体积变化)。
查看答案和解析>>
科目: 来源:2012届新疆乌鲁木齐一中高三第二次月考化学试卷 题型:问答题
常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。
(1)铁粉与水蒸气反应的化学方程式是:
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法:
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(结合化学方程式说明):
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是:
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如下图所示的装置:
请简述实验操作及原理:
查看答案和解析>>
科目: 来源:2011-2012学年浙江省宁波市八校高二下学期期末联考化学试卷(带解析) 题型:填空题
(12分)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢。K2Cr2O7和CrO3大量用于鞣革、印染、颜料、电镀等工业中,是工业上造成铬污染的主要原因。近期暴光的“毒胶囊”事件中,就是因为用工业皮革的下脚料或破皮鞋等为原料制成的工业明胶被冒充成食用明胶制成胶囊,造成胶囊内的铬严重超标。
(1)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。 
①A 点时剩余固体的成分是 (填化学式)。
②从开始加热到 750K 时总反应方程式为 。
(2)Cr(Ⅵ)主要以CrO42-和Cr2O72-形态存在,在酸性条件下具有很强的氧化性,它们在溶液中存在如下转化:CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O;K=4.2×1014。若要使溶液由黄色变橙色,则应采取的措施是 。
Cr2O72-(橙色)+H2O;K=4.2×1014。若要使溶液由黄色变橙色,则应采取的措施是 。
| A.加NaOH | B.加盐酸 | C.加硫酸 | D.加AgNO3 |
查看答案和解析>>
科目: 来源:2012届江苏省扬州中学高三下学期质量检测(三)化学试卷(带解析) 题型:填空题
(11分)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。
(1)CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为:
____________ 。
(2)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示。
①A 点时剩余固体的成分是_________ (填化学式)。
②从开始加热到 750K 时总反应方程式为______________________ _。
(3)CrO3和 K2Cr2O7均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6价 Cr 的废水放入电解槽内,用铁作阳极,加入适量的NaCl进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成 Fe(OH)3和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6.0×10-31]。
①电解过程中 NaCl 的作用是__________________________。
②已知电解后的溶液中c(Fe3+)为2.0×10-13 mol·L-1,则溶液中c(Cr3+)为 mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com