
ПЦФПЃК РДдДЃК2012НьКгФЯЪЁжЃжнЪаЫФЪЎЦпжаИпШ§ЩЯбЇЦкЕквЛДЮдТПМЛЏбЇЪдОэ ЬтаЭЃКЪЕбщЬт
ФГЮоЩЋШмвКЃЌгЩNaЃЋЁЂAgЃЋЁЂBa2ЃЋЁЂAl3ЃЋЁЂAlOЁЂMnOЁЂCOЁЂSOжаЕФШєИЩжжзщГЩЃЌШЁИУШмвКНјааШчЯТЪЕбщЃК
ЂйШЁЪЪСПЪдвКЃЌМгШыЙ§СПбЮЫсЃЌгаЦјЬхЩњГЩЃЌВЂЕУЕНШмвКЃЛ
ЂкдкЂйЫљЕУШмвКжадйМгШыЙ§СПЬМЫсЧтяЇШмвКЃЌгаЦјЬхЩњГЩЃЌЭЌЪБЮіГіАзЩЋГСЕэМзЃЛ
ЂлдкЂкЫљЕУШмвКжаМгШыЙ§СПBa(OH)2ШмвКЃЌвВгаЦјЬхЩњГЩЃЌВЂгаАзЩЋГСЕэввЮіГіЁЃ
ИљОнЩЯЪіЪЕ бщЭъГЩЯТСаЮЪЬтЃК
бщЭъГЩЯТСаЮЪЬтЃК
(1)ШмвКжавЛЖЈВЛДцдкЕФРызгЪЧ______________________ЁЃ
(2)вЛЖЈДцдкЕФРызгЪЧ______________________ЁЃ
(3)ХаЖЯГСЕэввГЩЗжЕФЗНЗЈЪЧ________________________ЁЃ
(4)аДГігаЙиРызгЗНГЬЪН
ЪЕбщЂй_________________________________ЁЃ
ЪЕбщЂк________________________________ЁЃ
(5)ЪЕбщЂлЩњГЩЕФЦјЬхЪЧ_________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2012НьЩНЮїЪЁПЕНмжабЇИпШ§9дТЗндТПМЛЏбЇЪдОэ ЬтаЭЃКЪЕбщЬт
ЃЈ16ЗжЃЉбЇЯАаЁзщЖдФГЦЗХЦбРИржаФІВСМСГЩЗжМАЦфКЌСПНјаавдЯТЬНОПЃК
ВщЕУзЪСЯЃКИУбРИрФІВСМСгЩЬМЫсИЦЁЂЧтбѕЛЏТСзщГЩЃЛбРИржаЦфЫќГЩЗжгіЕНбЮЫсЪБЮоЦјЬхЩњГЩЁЃ
ЂёЃЎФІВСМСжаЧтбѕЛЏТСЕФЖЈадМьбщЃК ШЁЪЪСПбРИрбљЦЗЃЌМгЫЎНСАшЁЂЙ§ТЫЁЃ
ЃЈ1ЃЉЭљТЫдќжаМгШыЙ§СПNaOHШмвКЃЌЙ§ТЫЁЃЧтбѕЛЏТСгыNaOHШмвКЗДгІЕФРызгЗНГЬЪНЪЧ____
____________________________________ЁЃ
ЃЈ2ЃЉЭљЃЈ1ЃЉЫљЕУТЫвКжаЯШЭЈШыЙ§СПЖўбѕЛЏЬМЃЌдйМгШыЙ§СПЯЁбЮЫсЁЃЙлВьЕНЕФЯжЯѓЪЧ_____
_____________________________________________________________________ЁЃ
ЂђЃЎбРИрбљЦЗжаЬМЫсИЦЕФЖЈСПВтЖЈЃКРћгУЯТЭМЫљЪОзАжУЃЈЭМжаМаГжвЧЦїТдШЅЃЉНјааЪЕбщЃЌГфЗжЗДгІКѓЃЌВтЖЈCжаЩњГЩЕФBaCO3ГСЕэжЪСПЃЌвдШЗЖЈЬМЫсИЦЕФжЪСПЗжЪ§ЁЃ
вРОнЪЕбщЙ§ГЬЛиД№ЯТСаЮЪЬтЃК
ЃЈ3ЃЉЪЕбщЙ§ГЬжаашГжајЛКЛКЭЈШыПеЦјЁЃЦфзїгУГ§СЫПЩНСАшBЁЂCжаЕФЗДгІЮяЭтЃЌЛЙга______
ЃЈ4ЃЉCжаЗДгІЩњГЩBaCO3ЕФЛЏбЇЗНГЬЪНЪЧ__________________________
ЃЈ5ЃЉЯТСаИїЯюДыЪЉжаЃЌВЛФмЬсИпВтЖЈзМШЗЖШЕФЪЧ_________ЃЈЬюБъКХЃЉЁЃ
aЃЎдкМгШыбЮЫсжЎЧАЃЌгІХХОЛзАжУФкЕФCO2ЦјЬхЃЛ bЃЎЕЮМгбЮЫсВЛвЫЙ§ПьЃЛ
cЃЎдкAЁЊBжЎМфдіЬэЪЂгаХЈСђЫсЕФЯДЦјзАжУ
dЃЎдкBЁЊCжЎМфдіЬэЪЂгаБЅКЭЬМЫсЧтФЦШмвКЕФЯДЦјзАжУ
ЃЈ6ЃЉЪЕбщжазМШЗГЦШЁ8.00gбљЦЗШ§ЗнЃЌНјааШ§ДЮВтЖЈЃЌВтЕУBaCO3ЦНОљжЪСПЮЊ3.94gЁЃдђбљЦЗжаЬМЫсИЦЕФжЪСПЗжЪ§ЮЊ_________ЁЃ
ЃЈ7ЃЉгаШЫШЯЮЊВЛБиВтЖЈCжаЩњГЩЕФBaCO3жЪСПЃЌжЛвЊВтЖЈзАжУCдкЮќЪеCO2ЧАКѓЕФжЪСПВюЃЌвЛбљПЩвдШЗЖЈЬМЫсИЦЕФжЪСПЗжЪ§ЁЃЪЕбщжЄУїАДДЫЗНЗЈВтЖЈЕФНсЙћУїЯдЦЋИпЃЌдвђЪЧ
_________________________________________________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2012НьИпШ§ЩЯбЇЦкОХдТЗндТПМЛЏбЇЪдОэЃЈБиао1Ек1Ѓ3еТВПЗжФкШнЃЉ ЬтаЭЃКЪЕбщЬт
(26Зж) ЃЈ1ЃЉТСЭСПѓЃЈжївЊГЩЗжЮЊAl2O3ЃЌЛЙКЌгаSiO2ЁЂFe2O3ЃЉЪЧЙЄвЕЩЯжЦБИбѕЛЏТСЕФжївЊдСЯЁЃЙЄвЕЩЯЬсШЁбѕЛЏТСЕФЙЄвеСїГЬШчЯТЃК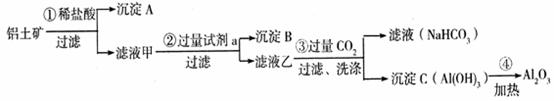
Ђй ГСЕэ AЁЂBЕФГЩЗжЗжБ№ЪЧ ЁЂ ЃЛВНжшЂкжаЕФЪдМСaЪЧ ЃЛ
Ђк ЪдаДГіВНжшЂлжаЗЂЩњЗДгІЕФРызгЗНЪН ЁЂ ЃЛ
ЂлМђЪіМьбщЫљЕУТЫвКМзжаДцдкFe3ЃЋЕФВйзїЗНЗЈЃК__________ _ЁЃ
ЃЈ2ЃЉгУКЌЩйСПЬњЕФбѕЛЏЭжЦШЁТШЛЏЭОЇЬхЃЈCuCl2ЁЄxH2OЃЉЁЃгаШчЯТВйзїЃК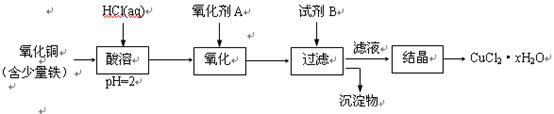
вбжЊЃКдкpHЮЊ4ЁЋ5ЪБЃЌFe3+МИКѕЭъШЋЫЎНтЖјГСЕэЃЌCu2+ШДВЛЫЎНтЁЃ
Ђй МгШШЫсШмЙ§ГЬжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНгаЃК ЁЃ
Ђк бѕЛЏМСAПЩбЁгУ ЃЈЬюБрКХЃЌЯТЭЌЃЉЁЃ
A.KMnO4 B. HNO3 C. Cl2
Ђл вЊЕУЕННЯДПЕФВњЦЗЃЌЪдМСBПЩбЁгУ ЁЃ
A. NaOH B. CuO C.FeO
Ђм ЪдМСBЕФзїгУЪЧ ЁЃ
A. ЪЙCu2+ЭъШЋГСЕэ ЁЁ B. ЪЙFe3+ЭъШЋГСЕэ
C. НЕЕЭШмвКЕФpH D. ЬсИпШмвКЕФpH
Ђн ДгТЫвКОЙ§НсОЇЕУЕНТШЛЏЭОЇЬхЕФЗНЗЈЪЧ ЃЈАДЪЕбщЯШКѓЫГађбЁЬюБрКХЃЉЁЃ
A. Й§ТЫ B. еєЗЂжСИЩ ЁЁ C. РфШДЁЁ D. еєЗЂХЈЫѕ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2012-2013бЇФъКкСњНЪЁКзИквЛжаИпЖўЯТбЇЦкЦкФЉПМЪдЛЏбЇЪдОэЃЈДјНтЮіЃЉ ЬтаЭЃКЪЕбщЬт
МзЁЂввСНИіЬНОПадбЇЯАаЁзщЃЌЫћУЧФтВтЖЈЙ§бѕЛЏФЦбљЦЗЃЈКЌЩйСПЕФNa2OЃЉЕФДПЖШЁЃ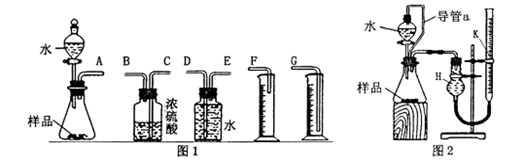
ЃЈ1ЃЉМззщЭЌбЇФтбЁгУЭМ1ЪЕбщзАжУЭъГЩЪЕбщЃК
ЂйаДГіЪЕбщжаЫљЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН ЃЛ
ЂкИУзщЭЌбЇбЁгУзюМђЕЅзАжУЕФСЌНгЫГађЪЧЃК
AНгЃЈ ЃЉЃЌЃЈ ЃЉНгЃЈ ЃЉЃЌЃЈ ЃЉНгЃЈ ЃЉЃЈЬюНгПкзжФИЃЌПЩВЛЬюТњЃЉЃЛ
ЃЈ2ЃЉ ввзщЭЌбЇзаЯИЗжЮіМззщЭЌбЇЕФЪЕбщзАжУКѓЃЌШЯЮЊЃКЫЎЕЮШызЖаЮЦПжаЃЌМДЪЙВЛЩњГЩбѕЦјЃЌ вВЛсНЋЦПФкПеЦјХХГіЃЌЪЙЫљВтбѕЦјЬхЛ§ЦЋДѓ;ЪЕбщНсЪјЪБЃЌСЌНгЙуПкЦПКЭСПЭВЕФЕМЙмжагаЩйСПЫЎДцдкЃЌЪЙЫљВтбѕЦјЬхЛ§ЦЋаЁЁЃгкЪЧЫћУЧЩшМЦСЫЭМ2ЫљЪОЕФЪЕбщзАжУЁЃ
ЂйзАжУжаЕМЙмaЕФзїгУЪЧЃК ЁЃ
ЂкЪЕбщНсЪјКѓ,дкЖСШЁСПЦјЙмkжавКУцЖСЪ§ЪБЃЌФуШЯЮЊзюКЯРэЕФЫГађЪЧ (гУAЁЂ BЁЂCзжФИБэЪО)
A. ЪгЯпгыСПЦјЙмkжаАМвКУцЕФзюЕЭЕуЯрЦН
B. ЕШД§ЪЕбщзАжУРфШД
C. ЩЯЯТвЦЖЏСПЦјЙмk,ЪЙkжавКУцгыHжаЕФвКУцЯрЦН
ЂлШєЪЕбщжабљЦЗЕФжЪСПЮЊwgЃЌЪЕбщЧАКѓСПЦјЙмkжавКУцЖСЪ§ЗжБ№ЮЊV1ЁЂV2(ЛЛЫуГЩБъПіЃЉЁЃдђбљЦЗЕФДПЖШЮЊ_______ (КЌwЁЂVЕФБэДяЪНЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2013НьаТНЎЮкТГФОЦыЕиЧјИпШ§ЕквЛДЮеяЖЯадВтбщЛЏбЇЪдОэЃЈДјНтЮіЃЉ ЬтаЭЃКЪЕбщЬт
МзЁЂввСНИіЬНОПадбЇЯАаЁзщЃЌЫћУЧФтВтЖЈЙ§бѕЛЏФЦбљЦЗЃЈКЌЩйСПЕФNa2OЃЉЕФДПЖШЁЃ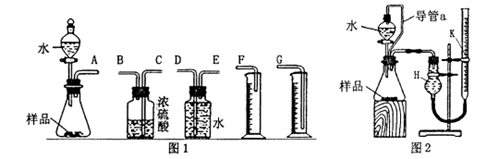
(1)МззщЭЌбЇФтбЁгУЭМ1ЪЕбщзАжУЭъГЩЪЕбщЃК
ЂйаДГіЪЕбщжаЫљЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН_______ЃЛ
ЂкИУзщЭЌбЇБиаыбЁгУЕФзАжУЕФСЌНгЫГађЪЧЃК
AНгЃЈ ЃЉЃЌЃЈ ЃЉНгЃЈ ЃЉЃЌЃЈ ЃЉНгЃЈ ЃЉЃЈЬюНгПкзжФИЃЌПЩВЛЬюТњЃЉЃЛ
(2) ввзщЭЌбЇзаЯИЗжЮіМззщЭЌбЇЕФЪЕбщзАжУКѓЃЌШЯЮЊЃКЫЎЕЮШызЖаЮЦПжаЃЌМДЪЙВЛЩњГЩбѕЦјЃЌ вВЛсНЋЦПФкПеЦјХХГіЃЌЪЙЫљВтбѕЦјЬхЛ§ЦЋДѓ;ЪЕбщНсЪјЪБЃЌСЌНгЙуПкЦПКЭСПЭВЕФЕМЙмжагаЩйСПЫЎДцдкЃЌЪЙЫљВтбѕЦјЬхЛ§ЦЋаЁЁЃгкЪЧЫћУЧЩшМЦСЫЭМ2ЫљЪОЕФЪЕбщзАжУЁЃ
ЂйзАжУжаЕМЙмaЕФзїгУЪЧЃК_______ЁЃ
ЂкЪЕбщНсЪјКѓ,дкЖСШЁСПЦјЙмkжавКУцЖСЪ§ЪБЃЌФуШЯЮЊзюКЯРэЕФЫГађЪЧ_______(гУAЁЂ BЁЂCзжФИБэЪО)
A. ЪгЯпгыСПЦјЙмkжаАМвКУцЕФзюЕЭЕуЯрЦН
B. ЕШД§ЪЕбщзАжУРфШД
C. ЩЯЯТвЦЖЏСПЦјЙмk,ЪЙkжавКУцгыHжаЕФвКУцЯрЦН
ЂлШєЪЕбщжабљЦЗЕФжЪСПЮЊwgЃЌЪЕбщЧАКѓСПЦјЙмkжавКУцЖСЪ§ЗжБ№ЮЊV1ЁЂV2(ЛЛЫуГЩБъ ПіЃЉЁЃдђбљЦЗЕФДПЖШЮЊ _______ (КЌwЁЂVЕФБэДяЪНЃЉЁЃ
(3)ЭМ2ЕФзАжУвВПЩВтЖЈвЛЖЈжЪСПТСУОКЯН№ЃЈВЛКЌЦфЫќдЊЫиЃЉбљЦЗжаТСЕФжЪСПЗжЪ§ЁЃЗжвКТЉЖЗжаМгШыЕФЪдМСЪЧ_______ЃЌФмЗёМгШыЧтбѕЛЏФЦШмвК _______ (ЬюЁАФмЁБЛђЁАВЛФмЁБЃЉЃЌЫЕУїРэгЩ______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2011НьМЊСжЪЁгЭЬяИпжаИпШ§ЕквЛДЮФЃФтЛЏбЇЪдОэ ЬтаЭЃКЪЕбщЬт
ЃЈ14ЗжЃЉТСУОКЯН№вбГЩЮЊЗЩЛњжЦдьЁЂЛЏЙЄЩњВњЕШаавЕЕФживЊВФСЯЁЃбаОПадбЇЯАаЁзщЕФЭЌбЇЃЌЮЊВтЖЈФГКЌУО4ЃЅЁЋ6ЃЅЕФТСУОКЯН№ЃЈВЛКЌЦфЫќдЊЫиЃЉжаУОЕФжЪСПЗжЪ§ЃЌЩшМЦСЫЖржжЪЕбщЗНАИЃЌЦфжажЎвЛЪЧЃКНЋТСУОКЯН№гызуСПNaOHШмвКЗДгІЃЌВтЖЈЪЃгрЙЬЬхжЪСПЁЃАДвЊЧѓЬюаДЯТСаПеАзЃК
1.ГЦШЁ5.4gТСУОКЯН№ЗлФЉбљЦЗЃЌШмгкV mL 2.0 mol/L NaOHШмвКжаЁЃ
ЂХЪЕбщжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЁЃ
ЂЦЮЊЪЙЦфЗДгІЭъШЋЃЌдђNaOHШмвКЕФЬхЛ§V Ён mLЁЃ
2.Й§ТЫЁЂЯДЕгЁЂИЩдяЁЂГЦСПЙЬЬхЁЃИУВНжшжаШєЮДЯДЕгЙЬЬхЃЌВтЕУУОЕФжЪСПЗжЪ§НЋ ЁЃ
(ЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЛђЁАЮогАЯьЁБ)ЁЃ
3. NaOHШмвКЕФХЈЖШПЩгУЯЁСђЫсВтЖЈЃЌгћгУжЪСПЗжЪ§98ЃЅЃЈУмЖШЮЊ1ЃЎ84 g/cm3ЃЉЕФХЈСђЫсХфжЦ3 mol/LЕФЯЁСђЫс100 mLЁЃЛиД№ЯТСаЮЪЬтЃК
ЂХашвЊгУСПЭВСПШЁХЈСђЫс mLЁЃ
ЂЦХфжЦВйзїПЩЗжНтГЩШчЯТМИВНЃЌе§ШЗЕФВйзїЫГађЪЧ ЁЃ
AЃЎМЬајЭљШнСПЦПжааЁаФЕиМгеєСѓЫЎЃЌЪЙвКУцНгНќПЬЖШЯп1~2cmЪБЁЃ
BЃЎгУЩйСПеєСѓЫЎЯДЕгЩеБМАВЃСЇАєЃЌНЋШмвКзЂШыШнСПЦПЃЌВЂжиИДВйзїСНДЮЁЃ
CЃЎНЋРфШДЕФЯЁ СђЫсзЊвЦЕНШнСПЦПжаЁЃ
СђЫсзЊвЦЕНШнСПЦПжаЁЃ
DЃЎИљОнМЦЫуЃЌгУСПЭВШЁвЛЖЈЬхЛ§ЕФХЈСђЫсЁЃ
EЃЎНЋХЈСђЫсбиЩеББкТ§Т§зЂШыЪЂгаеєСѓЫЎЕФаЁЩеБжаЃЌВЂВЛЖЯгУВЃСЇАєНСАшЁЃ
FЃЎ ИЧЩЯШнСПЦПШћзгЃЌеёЕДЃЌвЁдШЁЃ
ИЧЩЯШнСПЦПШћзгЃЌеёЕДЃЌвЁдШЁЃ
GЃЎгУНКЭЗЕЮЙмМгеєСѓЫЎЃЌЪЙШмвКАМвКУцЧЁКУгыПЬЖШЯпЯрЧа
ЂЧЯТСаВйзїЃЌЪЙжЦЕУЕФЯЁСђЫсШмвКХЈЖШЦЋаЁЕФЪЧ ЃЈЬюаДБрКХЃЉЁЃ
AЃЎгУСПЭВСПШЁвЛЖЈвКЬхЪБЃЌИЉЪгвКУцЖСЪ§ЁЃ
BЃЎдкШнСПЦПЖЈШнЪБИЉЪгПЬЖШЯпЁЃ
CЃЎзЊвЦШмвККѓЮДЯДЕгЩеБКЭВЃСЇАєЁЃ
DЃЎШнСПЦПИегУеєСѓЫЎЯДОЛЃЌУЛгаКцИЩЁЃ
EЃЎЖЈШнЪБЃЌЕЮМгеєСѓЫЎЃЌЯШЪЙвКУцТдИпгкПЬЖШЯпЃЌдйЮќГіЩйСПЫЎЪЙвКУцАМУцгыПЬЖШЯпЯрЧаЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2010ЁЊ2011бЇФъИЃНЈЪЁАВЯЊвЛжаЁЂбје§жабЇИпвЛЩЯбЇЦкЦкФЉСЊПМЛЏбЇЪдОэ ЬтаЭЃКЪЕбщЬт
ЃЈ12ЗжЃЉЙигкЁАТСШШЗДгІЁБЕФЯжЯѓгаетбљЕФУшЪіЃКЁАЗДгІЗХГіДѓСПЕФШШЃЌВЂЗЂГівЋблЕФЙтУЂЁЃЁБЁАжНТЉЖЗЕФЯТВПБЛЩеДЉЃЌгаШлШкЮяТфШыЩГжаЁЃЁБгжвбжЊAlЁЂFe2O3ЁЂAl2O3ЁЂF eЕФШлЕуКЭЗаЕуЃЌШчЯТБэЫљЪОЃК
eЕФШлЕуКЭЗаЕуЃЌШчЯТБэЫљЪОЃК
ЃЈ1ЃЉФГЭЌбЇЭЦВтЃЌТСШШЗДгІЕУЕНЕФШлШкЮягІЪЧТСЬњКЯН№ЁЃРэгЩЪЧЃКИУЗДгІЗХГіЕФШШФмЪЙЬњШлЛЏЃЌЖјТСЕФШлЕуБШЬњЕФЕЭЃЌЗХГіЕФШШвВПЩЪЙТСШлЛЏЃЌДЫЪБвКЬЌЕФЬњКЭТСаЮГЩТСЬњКЯН№ЁЃФуШЯЮЊетЮЛЭЌбЇЕФНтЪЭКЯРэТ№ЃП__________ЃЈЬюЁАКЯРэЁБЛђЁАВЛКЯРэЁБЃЉЁЃ
ЃЈ2ЃЉЩшМЦвЛИіМђЕЅЕФЪЕбщЗНАИжЄУїЩЯЪіЫљЕУЕФШлШкЮяжаКЌгаН№ ЪєТСЃЌВЂЬюаДЯТСаБэИёЃК
ЪєТСЃЌВЂЬюаДЯТСаБэИёЃК
| ЫљгУЪдМС | |
| ЪЕбщВйзїМАЯжЯѓ | |
| гаЙиЗДгІЕФЛЏбЇЗНГЬЪН | |
| AЃЎMgCl2ШмвК | BЃЎЯЁСђЫс | CЃЎХЈЯѕЫс | DЃЎNaOHШмвК |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2011НьЙуЖЋЪЁжаЩНЪабюЯЩвнжабЇИпШ§ЩЯбЇЦкСЊПМЛЏбЇОэ ЬтаЭЃКЪЕбщЬт
ЃЈ1)ЃЈ4ЗжЃЉЮИЪцЦНжївЊГЩЗжЪЧЧтбѕЛЏТСЃЌЭЌЪБКЌгаШ§ЙшЫсУО(Mg2Si3O8.nH2O)ЕШЛЏКЯЮяЁЃШ§ЙшЫсУОЕФбѕЛЏЮяаЮЪНЮЊ ЃЌФГдЊЫигыТСдЊЫиЭЌжмЦкЧвдзгАыОЖБШУОдзгАыОЖДѓЃЌИУдЊЫиРызгАыОЖБШТСРызгАыОЖ (ЬюЁАДѓЁБЛђЁАаЁЁБ)ЃЌИУдЊЫигыТСдЊЫиЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяжЎМфЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊЃК
ЃЈ2ЃЉЃЈ2ЗжЃЉ Al2O3ЁЂMgOКЭSiO2ЖМПЩвджЦФЭЛ№ВФСЯЃЌЦфдвђЪЧ ЁЃ
aЃЎAl2O3ЁЂMgOКЭSiO2ЖМВЛШмгкЫЎ bЃЎAl2O3ЁЂMgOКЭSiO2ЖМЪЧАзЩЋЙЬЬх
cЃЎAl2O3ЁЂMgOКЭSiO2ЖМЪЧбѕЛЏЮя dЃЎAl2O3ЁЂMgOКЭSiO2ЖМгаКмИпЕФШлЕу
ЃЈ3ЃЉЯђЪЂгаKIШмвКЕФЪдЙмжаМгШыЩйаэCCl4КѓЕЮМгТШЫЎЃЌCCl4ВуБфГЩзЯЩЋЁЃШчЙћМЬајЯђЪдЙмжаЕЮМгТШЫЎЃЌеёЕДЃЌCCl4ВуЛсж№НЅБфЧГЃЌзюКѓБфГЩЮоЩЋЁЃ
ЭъГЩЯТСаЬюПеЃК
ЂйЃЈ4ЗжЃЉаДГіВЂХфЦНCCl4ВугЩзЯЩЋБфГЩЮоЩЋЕФЛЏбЇЗДгІЗНГЬЪН(ШчЙћЯЕЪ§ЪЧ1ЃЌвЊЬюаД)ЃК
ЂкЃЈ2ЗжЃЉЃЉЯђЪЂгаKIШмвКЕЮМгТШЫЎЕФећИіЙ§ГЬжаЕФЛЙдМСЪЧ ЁЃ
ЂлЃЈ2ЗжЃЉАбKIЛЛГЩKBrЃЌдђCCl4ВуБфЮЊКьзиЩЋЃЌМЬајЕЮМгТШЫЎЃЌCCl4ВуЕФбеЩЋУЛгаБфЛЏЁЃCl2ЁЂHIO3ЁЂHBrO3бѕЛЏадгЩЧПЕНШѕЕФЫГађЪЧ ЁЃ
ЂмЃЈ2ЗжЃЉМгЕтбЮжаКЌЕтСПЮЊ20mgЁЋ50mgЃЏkgЁЃжЦШЁМгЕтбЮ(КЌKIO3ЕФЪГбЮ)1000kgЃЌШєНЋKIгыCl2ЗДгІжЦKIO3ЃЌжСЩйашвЊЯћКФCl2 L(БъзМзДПіЃЌБЃСє2ЮЛаЁЪ§)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2011НьЩНЖЋЪЁбЬЬЈЪаИпШ§ЩЯбЇЦкФЃПщМьВтЛЏбЇЪдОэ ЬтаЭЃКЪЕбщЬт
ЙЄвЕЩЯгУТСЭСПѓЃЈжївЊГЩЗжЮЊAl2O3ЃЌЛЙКЌгаFe2O3ЁЂSiO2ЃЉЬсШЁбѕЛЏТСзівБСЖТСЕФдСЯЃЌЬсШЁЕФВйзїЙ§ГЬШчЯТЃК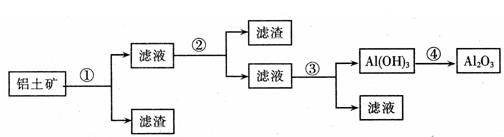
ПЩЙЉбЁдёЕФЪдМСЃКЯЁбЮЫсЁЂNaOHШмвКЁЂЯЁАБЫЎЃЌCO2ЕШ
ЧыаДГіФуЫљЩшМЦЕФЗНАИжаИїЗДгІЕФЛЏбЇЗНГЬЪНЁЃ
Ђй ЃЛ
Ђк ЃЛ
Ђл ЃЛ
Ђм  ЁЃ
ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК2010ФъЙуЖЋЪЁЙужнЖЋнИЮхаЃИпШ§ЩЯбЇЦкЕкЖўДЮСЊПМЃЈРэзлЃЉЛЏбЇ ЬтаЭЃКЪЕбщЬт
ЃЈ16ЗжЃЉТСУОКЯН№вбГЩЮЊТжДЌжЦдьЁЂЛЏЙЄЩњВњЕШаавЕЕФживЊВФСЯЁЃбаОПадбЇЯАаЁзщЕФШ§ЮЛЭЌбЇЃЌЮЊВтЖЈФГКЌУО3ЃЅ-5ЃЅЕФТСУОКЯН№ЃЈВЛКЌЦфЫќдЊЫиЃЉжаУОЕФжЪСПЗжЪ§ЃЌЩшМЦЯТСаШ§жжВЛЭЌЪЕбщЗНАИНјааЬНОПЁЃЬюаДЯТСаПеАзЃЈПЩФмгУЕНЕФЯрЖддзгжЪСПЃКAl-27ЃЉ
[ЬНОПвЛ] ЪЕбщЗНАИЃКТСУОКЯН№ ВтЖЈЪЃгрЙЬЬхжЪСПЁЃ
ВтЖЈЪЃгрЙЬЬхжЪСПЁЃ
ЪЕбщВНжшЃК
ЃЈ1ЃЉГЦШЁ5.4gТСУОКЯН№ЗлФЉбљЦЗЃЌЭЖШыVmL 2.0molЁЄLЃ1NaOHШмвКжаЃЌГфЗжЗДгІЁЃNaOHШмвКЕФЬхЛ§VЁн ЁЃ
ЃЈ2ЃЉЙ§ТЫЁЂЯДЕгЁЂИЩдяЁЂГЦСПЙЬЬхЁЃИУВНжшжаШєЮДЯДЕгЙЬЬхЃЌВтЕУУОЕФжЪСПЗжЪ§НЋ
ЃЈЁАЦЋИпЁБЛђЁАЦЋЕЭЁБЃЉ
[ЬНОПЖў] ЪЕбщЗНАИЃКТСУОКЯН№ ВтЖЈЩњГЩЦјЬхЕФЬхЛ§ЃЈЪЕбщзАжУШчЯТЭМЃЉ
ВтЖЈЩњГЩЦјЬхЕФЬхЛ§ЃЈЪЕбщзАжУШчЯТЭМЃЉ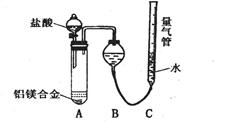
ЮЪЬтЬжТлЃК
ЮЊЪЙВтЖЈНсЙћОЁПЩФмОЋШЗЃЌЪЕбщжагІзЂвтЕФ
ЮЪЬтЪЧЃЈаДГіПЩФмЕФвЛЕуЃЉЃК
ЁЃ
[ЬНОПШ§] ЪЕбщЗНАИЃКГЦСПm gТСУОКЯН№ЗлФЉЃЎЗХдкШчгвЭМЫљЪОзАжУЕФЖшадЕчШШАхЩЯЃЌЭЈЕчЪЙЦфГфЗжзЦЩеЁЃ
ЮЪЬтЬжТлЃКгћМЦЫуMgЕФжЪСПЗжЪ§ЃЌИУЪЕбщжаЛЙашВтЖЈЕФ
Ъ§ОнЪЧ ЁЃ
[ЪЕбщЭиеЙ] ЧыФуСэЩшМЦвЛИіЪЕбщЗНАИЃЌВтЖЈИУТСУОКЯН№жаУОЕФжЪСПЗжЪ§ЃЈЪщаДаЮЪНПЩвдФЃЗТЬНОПвЛЁЂЖўЪЕбщЗНАИЃЉ
ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com