
【题目】化学与科学技术、生产生活及环境保护等密切相关。
(1)我省启动保卫碧水蓝天的“263“行动,减少煤炭消费总量,减少雾霾天气的发生。形成硫酸型酸雨的主要气体是__________;严格整治畜禽养殖场污染,主要是为减少_________和P等元素及化学需氧量对水体的污染。
(2)目前正在推广用尿素水解液来消除柴油汽车尾气中的氮氧化物。写出脉素水解液中的NH3与NO在催化剂作用下,反应生成无污染物质的化学方程式____________________________________。
(3)三硅酸镁 Mg2Si3O8·nH2O具有治疗胃酸过多的作用,写出其与酸反应生成SiO2·H2O等物质的化学方程式_____________。
【答案】 SO2 N(氮) 6NO+4NH3 ![]() 5N2+6H2O Mg2Si3O8·nH2O+4HCl===2MgCl2 +3SiO2·H2O+(n-1)H2O
5N2+6H2O Mg2Si3O8·nH2O+4HCl===2MgCl2 +3SiO2·H2O+(n-1)H2O
【解析】(1)根据造成酸雨的原因以及造成水体污染的主要原因来分析;(2)(3)根据反应物、生成物、反应条件写出反应的化学方程式;(1)二氧化硫是形成硫酸型酸雨的主要气体;严格整治畜禽养殖场污染,主要是为减少氮元素与磷元素及化学需氧量对水体的污染;(2)在催化剂存在的条件下,氨气与NO反应生成无毒的N2和H2O,反应的化学方程式为4NH3+6NO![]() 5N2+6H2O;(3)三硅酸镁Mg2Si3O8·nH2O与HCl反应生成MgCl2、SiO2·H2O、H2O,反应的化学方程式为Mg2Si3O8·nH2O+4HCl=2MgCl2 +3SiO2·H2O+(n-1)H2O。
5N2+6H2O;(3)三硅酸镁Mg2Si3O8·nH2O与HCl反应生成MgCl2、SiO2·H2O、H2O,反应的化学方程式为Mg2Si3O8·nH2O+4HCl=2MgCl2 +3SiO2·H2O+(n-1)H2O。


科目:初中化学 来源: 题型:
【题目】恩施州内的很多景点都已经在全国乃至世界享有盛名,如“腾龙洞”、“恩施大峡谷”等;而形成这些奇谷异洞的根本原因与当地的石灰石有关。某中学的“化学兴趣小组”为了测定“腾龙洞”内石灰石样品中CaCO3的含量。取8g样品研碎后放入烧杯中,再加入100g稀盐酸恰好完全反应后,烧杯中剩余物质105.8克(假设样品中杂质不溶也不反应,不考虑水的蒸发及CO2的溶解等因素,结果保留百分号前一位小数)。试计算:
(1)样品中CaCO3的质量分数是多少_________?
(2)所得溶液中溶质的质量分数是多少_________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钙及其化合物在生产、生活中具有广泛的应用
(一)钙及其化合物的应用
(1)青少年缺“钙”易患的疾病是________。
(2)混凝土中也含有一定量的含钙物质,钢筋与混凝土混合形成钢筋混凝土,以上叙述中不涉及的材料是_________。 a.无机材料 b.合成材料 c.复合材料
(3)即热型快餐加热原理是利用生石灰和水反应放热,用方程式表示其反应__________。
(二)过氧化钙(CaO2)的性质
(1)CaO2中氧元素的化合价为_____________。
(2)CaO2能与稀盐酸发生复分解反应,反应的化学方程式为_____________。
(3)鱼类长途运输的增氧剂的主要成分为CaO2,它与水缓慢反应生成O2,还生成一种碱,其化学式为_______,Na2O2也能与水反应,原理与CaO2相同,但却不能作为鱼虾运输的供氧剂,请分析可能的原因___________________。
(三)过氧化钙晶体的制备
(资料)过氧化钙晶体(CaO2·yH2O),常温为白色,能溶于酸,难溶于酒精。
制备原理:CaCl2+H2O2+NH3+H2O ![]() CaO2·yH2O↓+NH4Cl,装置如下。
CaO2·yH2O↓+NH4Cl,装置如下。

(1)装置A中试管内发生反应的化学方程式为______________________。
(2)装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ. 该反应是放热反应,温度低有利于提高CaO2·yH2O产率;
Ⅱ. _____________________________。
(3)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·yH2O。
①洗涤时采用95%的酒精溶液洗涤的优点是_________________。
②检验晶体已洗涤干净的方法为________________________。
(四)过氧化钙晶体组成的测定
称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水)

(1)0—150℃质量不发生改变的原因是______________________。
(2)根据上图可知y=________。
(3)350℃时发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一烧杯中盛有2.4g金属镁,向其中加入一定质量的稀硫酸,充分反应后,向所得溶液中逐滴滴入未知溶质质量分数的氢氧化钠溶液,产生沉淀与滴入氢氧化钠溶液的质量关系曲线如图所示。
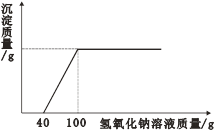
(1)完全反应后,产生沉淀的质量为________g;
(2)氢氧化钠溶液中溶质的质量分数是_________?(写出计算过程,结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生物体中含有多种氨基酸(结构如图所示)。下列有关叙述正确的( )
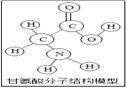
A. 甘氨酸是有机高分子化合物
B. 一个甘氨酸分子中含有10个原子
C. 甘氨酸是由碳、氢、氧、氮四种原子构成的
D. 甘氨酸中碳元素与氧元素的质量比为1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳、硫的含量影响钢铁性能、某兴趣小组用如下流程对钢样进行探究。
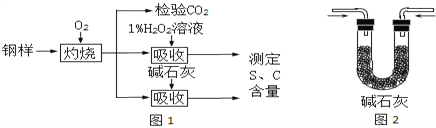
(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧生成两种氧化物,其中一种是固体,固体产物中Fe、O元素的质量比为21:8,则该固体产物的化学式为_________。灼烧的反应方程式为_________;
(2)钢样灼烧生成的气体是___________和___________,检验前者需要的试剂是_______________,检验后者需要的试剂是_____________________;
(3)取10.00g钢样在足量氧气中充分灼烧,将生成的气体用适量1%的H2O2溶液充分吸收,吸收液呈现酸性,用10g0.8%的NaOH溶液恰好将吸收液中和至中性;另取10.00钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U型管(如图2),碱石灰增重0.614g。
①用1%H2O2溶液吸收SO2,发生化合反应,化学方程式为_________________________________;
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。下列说法正确的是

A. N点对应的ZnSO4溶液升温或降温均都可能析出晶体
B. M点对应的ZnSO4溶液是不饱和溶液
C. ZnSO4饱和溶液的溶质质量分数随温度升高而增大
D. 40℃时,ZnSO4的溶解度为41g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验操作的规范性、安全性是实验成败的关継,同时也反映了实验者的化学素养。下列如图所示的实验操作正确的是
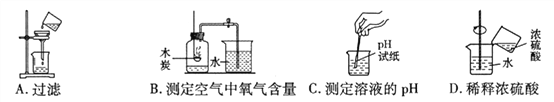
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱厂生产的某批次碳酸钠产品中可能含有氯化钠杂质。
定性检验
(1)要确定该产品中是否含有杂质氯化钠,你的方法是_________________。
定量测定:
(2)若利用沉淀法测定该产品中碳酸钠的质量分数,你确定的反应原理是(用化学方程式表示)_______________________________。
(3)假设你取样的质量为m1,根据你确定的反应原理,你需要通过实验测量沉淀(填化学式)____的质量(假设你测得的沉淀的质量为m2)。
(4)请你设计实验方案,获得数据m1、m2,把方案填在下表中。
适用的仪器名称 | 实验步骤 |
____________ | ______ |
(5)数据处理:
请用含m1、m2的式子表示所测样品中碳酸钠的质量分数,______________________。
分析讨论:
(6)要测定混合物中某成分的含量,可通过化学方法将不易测定的物质转化为易测量的物质。除沉淀法外,还可依据反应(用化学方程式表示)_______________来测定该纯碱样品中碳酸钠的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com