
【题目】下表是KNO3、NaCl在不同温度下的溶解度。
温度(℃) | 0 | 20 | 30 | 40 | 60 | 80 | |
溶解度 | KNO3 | 13.3 | 31.6 | 45.8 | 63.9 | 110 | 169 |
NaCl | 35.7 | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | |
(1)根据表中的数据,在坐标纸上绘制出氯化钠和硝酸钾两种物质的溶解度曲线。(在答题卡的坐标纸上绘图)____
①两种物质中,溶解度受温度的影响变化较大的是_____。
②根据绘制的溶解度曲线可知,50℃时,硝酸钾的溶解度约为_____。
③将接近饱和的KNO3溶液转化为饱和溶液的一种方法是_____。
④从较浓的NaCl溶液中得到NaCl晶体,较好的方法是_____(填“蒸发结晶”或“降温结晶”)。
(2)A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体。

①A溶液为_____(选填“饱和”或“不饱和”)溶液。
②对以上过程的分析,正确的是_____(选填编号)。
a.A到B的过程中,溶质质量没有改变
b.B中溶质与溶剂的质量比为169:100
c.开始析出KNO3固体的温度在60℃至80℃之间
d.A溶液的质量等于222g
(3)烧杯内原有某物质,向其中加入物质X,X的质量与变量Y的关系如图,下列一定能正确反映X、Y对应关系的是_____。
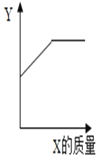
选项 | 烧杯内原有物质 | X | Y |
A | NaCl饱和溶液 | NaCl固体 | NaCl溶液的溶质质量分数 |
B | 水 | NH4NO3固体 | 溶液的温度 |
C | 氯化亚铁溶液 | 锌粉 | 溶液的质量 |
D | 稀硫酸 | 铁粉 | 溶液中氢元素的质量 |
【答案】 ; KNO3(硝酸钾); 85(±1)g; 加KNO3或蒸发水分或降温; 蒸发结晶; 不饱和 ac; C。
; KNO3(硝酸钾); 85(±1)g; 加KNO3或蒸发水分或降温; 蒸发结晶; 不饱和 ac; C。
【解析】
(1)依据表中的数据绘制氯化钠和硝酸钾两种物质的溶解度曲线,如图:
 ;
;
①通过分析溶解度曲线可知,两种物质中,溶解度受温度的影响变化较大的是硝酸钾;②通过分析绘制的溶解度曲线可知,50℃时,硝酸钾的溶解度约为85g;③硝酸钾的溶解度随温度的升高而增大,所以将接近饱和的KNO3溶液转化为饱和溶液的一种方法是:加KNO3或蒸发水分或降温;④氯化钠的溶解度受温度变化影响较小,所以从较浓的NaCl溶液中得到NaCl晶体,较好的方法是蒸发结晶;
(2)A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体。

①A溶液恒温蒸发20g水没有晶体析出,所以A溶液为不饱和溶液;②a、A溶液恒温蒸发20g水没有晶体析出,所以A到B的过程中,溶质质量没有改变,此选项正确;b、B中溶质与溶剂的质量比为(102g+31.6g):(120g-20g)=133.6:100,此选项错误;c、B中含有100g水、(102g+31.6g)的硝酸钾,硝酸钾在80℃时的溶解度是169g,在60℃时的溶解度是110g,所以开始析出KNO3固体的温度在60℃至80℃之间,此选项正确;d、C溶液为20℃时,硝酸钾的饱和溶液,仍有部分硝酸钾还溶解在水中,所以A溶液的质量大于222g,此选项错误,故选ac。
(3)A、氯化钠饱和溶液中加入氯化钠固体,溶液质量分数不变,此选项错误;
B、硝酸铵溶于水,溶液温度降低,此选项错误;
C、Zn+FeSO4=ZnSO4+Fe,每65份质量的锌和硫酸亚铁反应生成硫酸锌和56份质量的铁,所以反应后溶液质量增加,当氯化亚铁溶液反应完以后,溶液的质量不变,此选项正确;
D、铁和稀硫酸反应生成硫酸亚铁和氢气,氢元素的质量逐渐减小,此选项错误。故选C。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:
【题目】分类、类比是学习化学常用的方法。
(1)初中化学实验可以按照实验目的分为:“混合物的分离提纯实验”、“探究反应条件实验”“探究物质性质实验”等。据此我们可以将实验A与实验①_____(填字母)分为一类,分类依据是②_____。
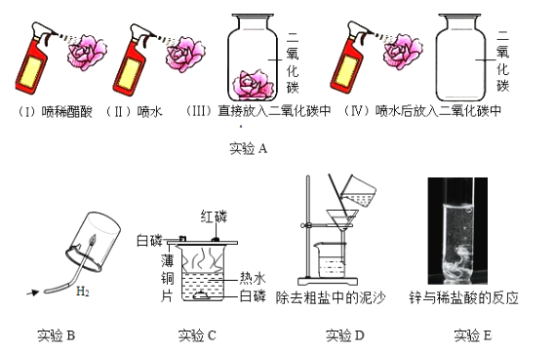
(2)在金属活动性顺序中,排在前面的“钾、钙、钠”三种金属与盐溶液接触时先与溶液中的水反应生成碱和氢气。已知金属钾与水反应的化学方程式为:2K+2H2O═2KOH+H2↑.现将金属钠加入硫酸铜溶液中,请写出发生总反应的化学方程式为①_____。金属钠很容易被空气中的氧气氧化,由此推测实验室保存金属钠的注意事项是②_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是在一定条件下,某物质发生化学反应的微观模拟图,请从微观角度回答下列问题:

(1)请在B和C图中补充相关粒子图形,使其表示正确________;
(2)C图中补充相关粒子图形的依据是_____;
(3)从微观角度说明A物质是由两种单质组成混合物的依据是_____;
(4)此变化前后没有发生改变的微观粒子有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A B C D E F G为常见的物质,其中B E G属于单质,反应![]() 是炼铁中的主要反应,它们之间的相互转化关系如图所示:
是炼铁中的主要反应,它们之间的相互转化关系如图所示:

![]() 物质B的化学式是______;写出反应
物质B的化学式是______;写出反应![]() 的基本反应类型______。
的基本反应类型______。
![]() 写出C的一种用途:______。
写出C的一种用途:______。
![]() 写出反应
写出反应![]() 中生成红色固体E的化学方程式:______。
中生成红色固体E的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列对比实验设计不能实现相应实验目的是( )
选项 | A | B | C | D |
实验 目的 | 探究温度对分子 运动速率的影响 | 探究水对铁钉 锈蚀的影响 | 探究同种物质在不同溶剂中的溶解性 | 探究Mg、Fe金属的活动性强弱 |
实验 设计 |
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示A~F是初中化学常见的物质。图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件未标出)。其中A是紫红色金属,B常温下是气体,C是人体胃液中含有的酸。则下列说法正确的是 ( )

A. E一定是二氧化碳
B. B可能为氢气或一氧化碳
C. 该过程中没有涉及到复分解反应
D. D转化为A的反应可以为置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年5月9日,我国“高分五号”卫星发射成功。
(1)高氯酸钾(KClO4) 可用作火箭燃料,其中氯元素的化合价为_________________。
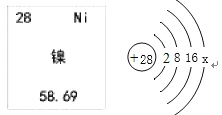
(2)“高分五号”用钛镍形状记忆合金制作卫星天线。下图是镍元素在元素周期表中的信息以及原子结构示意图。镍元素的相对原子质量为_____________。X的数值是_____。
(3)“高分五号”是我国首颗对大气中二氧化硫、二氧化氮、二氧化碳、甲烷等多个环境要素进行监测的卫星。
①上述四种气体可以造成酸雨的是____________(写一种即可):
②催化还原法是消除大气中氮氧化物污染的新工艺,主要的微观示意图如下。
下列说法正确的是___________(填序号)。
A.反应前后分子的种类不变 B.反应前后原子的种类发生改变
C.反应前后元素化合价都不变 D.反应后丁、戊的分子个数比为2: 1

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在点燃的条件下,2.6g的C2H2与7.2g的O2恰好完全反应,生成6.6gCO2、1.8gH2O和ag的X,下列关于该反应的说法不正确的是( )
A. a=1.4
B. X中一定不含碳元素
C. X中的氧元素与消耗的氧气质量之比为1:9
D. 该反应的化学方程式为:4C2H2+9O2![]() 6CO2+4H2O+2CO
6CO2+4H2O+2CO
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为CO还原CuO“微型”实验装置(夹持仪器等略).已知HCOOH![]() H2O+CO↑.下列说法错误的是( )
H2O+CO↑.下列说法错误的是( )

A. 实验中所需CO可现制现用
B. 此装置可节约药品,污染小,现象明显
C. 此装置内空间较小,空气易排空,实验危险系数小
D. 该实验中所涉及反应的基本类型有分解反应和化合反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com