
| 甲 | 乙 | 丙 | |
| 所取样品质量 | 25g | 30g | 25g |
| 加入的盐酸质量 | 100g | 100g | 150g |
| 充分反应后溶液质量 | 116.2g | 121.2g | 166.2g |
分析 (1)根据溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(3)根据甲、乙实验中,生成二氧化碳的质量都是8.8g,说明乙中样品过量进行分析;
(4)根据甲、丙实验中,生成二氧化碳的质量都是8.8g,说明丙中盐酸过量,由此可知,甲中的碳酸钠和稀盐酸恰好完全反应,再根据提供的数据可以进行相关方面的计算;
(5)根据碳酸钠和氢氧化钠之间的转化关系和题中的数据进行解答.
解答 解:设甲中稀盐酸中的氯化氢质量为x,碳酸钠质量为y,生成氯化钠的质量为z,
甲中反应生成二氧化碳的质量为:25g+100g-116.2g=8.8g,
2HCl+Na2CO3=2NaCl+CO2↑+H2O,
73 106 117 44
x y z 8.8g
$\frac{73}{x}$=$\frac{106}{y}$=$\frac{117}{z}$=$\frac{44}{8.8g}$,
x=14.6g,y=21.2g,z=23.4g,
(1)设设需要浓盐酸质量为m,
由计算可知,100g稀盐酸中含有14.6g氯化氢,则200g稀盐酸中含有29.2g氯化氢,
根据题意有:m×36.5%=29.2g,
m=80g,
需要水的质量为:200g-80g=120g,
需浓盐酸和水的质量比为:80g:120g=2:3;
(2)发生反应的化学方程式为:2HCl+Na2CO3=2NaCl+CO2↑+H2O;
(3)该样品中的碳酸钠的含量为:$\frac{21.2g}{25g}$×100%=84.8%;
(4)向恰好反应后的溶液中加入83.8g水后,所得溶液的质量分数为:$\frac{25g-21.2g+23.4g}{116.2g+83.8g}$×100%=13.6%;
(5)设需要纯碱的质量为m,
Na2CO3----2NaOH
106 80
m×84.8% 200t×(1-15.6%)
$\frac{106}{m×84.8%}$=$\frac{80}{200t×(1-15.6%)}$
m=264t
故答案为:(1)2:3;
(2)发生反应的化学方程式为:2HCl+Na2CO3=2NaCl+CO2↑+H2O;
(3)该样品中的碳酸钠的含量为:$\frac{21.2g}{25g}$×100%=84.8%;
(4)向恰好反应后的溶液中加入83.8g水后,所得溶液的质量分数为:$\frac{25g-21.2g+23.4g}{116.2g+83.8g}$×100%=13.6%;
(5)264t.
点评 本题主要考查了化学方程式的有关计算,难度较大,需要找准各个量之间的关系,才能正确解答.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 成分 | 糖类 | 柠檬酸 | 蛋白质 | 维生素C | 钙、铁、磷、锌等 |
| 质量g/mL | 11.50 | 1.03 | 0.90 | 0.08 | 1.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
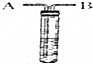 化学兴趣小组的同学,为研究“人体呼出的气体中二氧化碳的含量是否比空气中多”的问题,用如图所示的实验装置,选择了二种不同的试剂进行实验,成功得出“人体呼出的气体中二氧化碳的含量比空气中多”的结论.试根据你所学的化学知识回答问题:实验时应先从B处吸气,再从A处呼气(选填“呼气”或“吸气”)
化学兴趣小组的同学,为研究“人体呼出的气体中二氧化碳的含量是否比空气中多”的问题,用如图所示的实验装置,选择了二种不同的试剂进行实验,成功得出“人体呼出的气体中二氧化碳的含量比空气中多”的结论.试根据你所学的化学知识回答问题:实验时应先从B处吸气,再从A处呼气(选填“呼气”或“吸气”)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
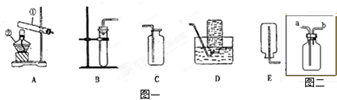 小强和几位同学在实验室用下列装置制取几种气体:
小强和几位同学在实验室用下列装置制取几种气体:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com