
【题目】(11分)氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气.探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液.经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
(1)【猜想与假设】
猜想一:NaOH
猜想二:
猜想三:NaOH、Na2CO3
猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因 。
(2)【实验验证】
实验 | 现象 | 结论 |
实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想 ① 不成立 |
实验二:另取滤液,向其中加入 ② | 先无变化后产生气泡 | 猜想三成立 |
(3)【反思与拓展】①若向NH4Cl的溶液中加一定量CaH2,充分反应,产生的气体是氢气和 .②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是 .
【答案】(1)NaOH、Ca(OH)2(2分),Na2CO3+Ca(OH)2=CaCO3![]() +2NaOH(2分)(2)①二(2分)②足量稀盐酸(2分)(3)①氨气(NH3)(1分)②氢化钙明显比氢气更易携带,使用也较方便(2分)
+2NaOH(2分)(2)①二(2分)②足量稀盐酸(2分)(3)①氨气(NH3)(1分)②氢化钙明显比氢气更易携带,使用也较方便(2分)
【解析】
试题分析:根据题中的叙述及反应进行的程度可知(1) 猜想二为NaOH、Ca(OH)2;猜想四是不合理的,因为碳酸钠与氢氧化钙不能共存,碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;故答案为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.(2)【实验验证】在实验一中,取滤液,向其中滴入少量碳酸钠溶液,无明显现象,说明没有氢氧化钙,即猜想二不成立;实验二:另取滤液,向其中加入足量稀盐酸,观察到先无变化后产生气泡的现象时,说明滤液中含有氢氧化钠和碳酸钠,即猜想三成立;(3)【反思与拓展】若向NH4Cl的溶液中加一定量CaH2,充分反应,产生的气体是氧气、氨气,因为氢化钙(CaH2)与水反应生成氢氧化钙和氢气,氯化铵和氢氧化钙反应生成氯化钙和水和氨气;登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是氢化钙明显比氢气更易携带,使用也较方便。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】维生素C(化学式为C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病
A.维生素C的相对分子质量为176
B.维生素C是由碳元素、氢元素和氧元素组成的
C.维生素C中,C、H、O三种元素的质量比为9:1:12
D.维生素C中,C、H、O三种元素的个数比为3:4:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映对应的实验操作的是
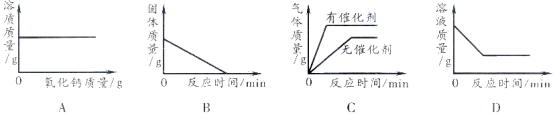
A.向一定量的饱和石灰水中加入氧化钙
B.加热一定量高锰酸钾固体产生氧气
C.用一定量的双氧水制取氧气
D.向一定量的硝酸银溶液中插入铜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 相同质量的CO和CO2,则CO和CO2所含的氧元素质量比为_________,若CO和CO2所含的氧元素质量相等,则CO和CO2质量比为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法错误的是
物质 | a | b | c | d |
反应前质量(g) | 10 | 10 | 10 | 2 |
反应后质量(g) | 待测 | 2 | 21 | 2 |
A.该反应是化合反应,d可能是催化剂
B.b物质可能是单质
C.a、b两种物质中元素种类一定与C物质中元素种类相同
D.反应后a物质的质量为3g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】区分下列各组物质的方法不正确的是
A.水和双氧水——加二氧化锰
B.二氧化碳和氮气—将燃着的木条伸入瓶中
C.高锰酸钾和二氧化锰——看颜色
D.石灰水和水——通二氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质的性质与所对应的用途没有直接关系的是
A.氧气的密度比空气略大﹣﹣用于急救病人
B.稀有气体的性质稳定﹣﹣作保护气
C.石墨能导电﹣﹣可作电极
D.干冰升华吸热﹣﹣用于人工降雨
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(11分)医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙为原料(含量为97.5%,含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙的主要流程如下:
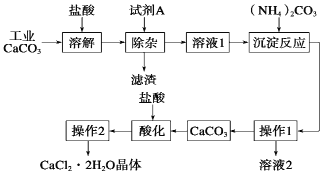
(1)除杂操作时加入试剂A,调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+。试剂A是Ca(OH)2,还可以选择 。
a.NaOH b.NH3 c.Na2CO3
(2)请指出下列操作的名称:操作1 ;操作2蒸发浓缩、 ;操作1中所用的玻璃仪器有漏斗、玻璃棒、 。
(3)酸化操作是加入过量盐酸,调节溶液的pH为4.0,目的之一是为了将少量的 转化为CaCl2。
(4)写出加入碳酸铵所发生的反应的方程式: +(NH4)2CO3=CaCO3↓+2NH4Cl
写出溶液2的一种用途 。
(5)测定样制得品中Cl-含量的方法是:称1.5g样品,溶解,滴加过量的 AgNO3 溶液,过滤、洗涤、干燥,称得沉淀质量为2.87g,证明沉淀洗净的标准是:取最后一次洗涤的滤液,滴加 试剂,若 现象,则已经洗净。
(6)计算上述样品中CaCl2·2H2O的质量分数为: 。若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com