
【题目】甲、乙、丙是初中化学常见的三种物质,其相互转化关系如图,通常甲为固态单质,乙、丙为常温下的两种常见气体,且所含元素种类相同,乙易与血液中的血红蛋白结合。下列说法正确的是( )
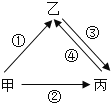
A.①②两个转化的反应中,只能验证甲具有可燃性
B.干燥的丙能使紫色石蕊变成红色
C.③的转化可通过和金属氧化物反应来实现
D.乙和丙均由分子构成,且都易溶于水
【答案】C
【解析】
甲、乙、丙是初中化学常见的三种物质,其相互转化关系如图,通常甲为固态单质,乙、丙为两种气体,且所含元素种类相同,乙易与血液中的血红蛋白结合,乙是一氧化碳,固态单质碳在氧气中充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,因此甲是碳,丙是二氧化碳。
A、①②两个转化的反应中,只能验证甲具有可燃性,甲可能还原氧化铜生成二氧化碳,故选项错误;
B、干燥的丙不能使紫色石蕊变成红色,故选项错误;
C、③的转化为一氧化碳反应生二氧化碳,一氧化碳和氧化铜在加热下反应生成铜和二氧化碳,可通过和金属氧化物反应来实现,故选项正确;
D、一氧化碳和二氧化碳均由分子构成,但二氧化碳易溶于水,一氧化碳难溶于水,,故选项错误。故选C。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:初中化学 来源: 题型:
【题目】(1)净化水的方法有:①过滤、②加明矾吸附沉降、③蒸馏、④消毒杀菌。要将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为_____(填序号).
(2)如图是a.b.c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
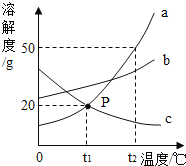
①P点的含义是__________________。
②t2℃时a、b、c三种物质的溶解度按由大到小的顺序排列是_____。
③若b中混有少量的a ,最好采用_____的方法提纯 b;
④t1℃时15ga物质加入到50g水中充分搅拌,得到溶液的质量为____g。
⑤将t2℃时等质量的a、b、c 三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数由大到小的顺序是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】茶叶是人们喜爱的饮品之一,科学研究证实茶叶中含茶氨酸(化学式为 C7H14N2O3)、锌、 硒等多种对人体有益的成分。请计算:
(1)锌、硒属于 (选填“常量”或“微量”)元素;
(2)茶氨酸中氢、氮元素的质量比 (填最简整数比);
(3)若茶氨酸中碳元素的质量为 4.2g,则茶氨酸的质量为 g。
查看答案和解析>>
科目:初中化学 来源: 题型:
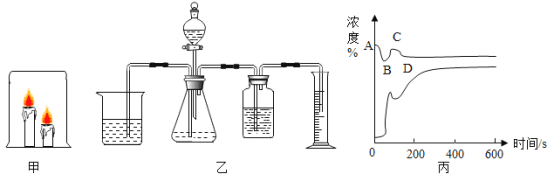
【题目】某校化学兴趣小组同学将一只烧杯罩在2支高低不同的燃着的蜡烛上(如图1所示),发现总是高的蜡烛先熄灭。请你同他们一起进行探究。
(提出问题)为什么高的蜡烛先熄灭?
(猜想假设)猜想1:高的蜡烛先灭是因为上部的二氧化碳浓度高;猜想2:高的蜡烛先灭是因为上部的氧气先被消耗。
(实验探究1)为了验证猜想1是否成立,冰冰同学进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
将浸有澄清石灰水的滤纸条分别放在烧杯的顶部和底部,在滤纸条上滴加酚酞,变色后,用烧杯罩住点燃的高低蜡烛,观察高低滤纸条褪色顺序(实验装置如图甲所示) | _________ | 猜想1成立,该实验涉及的反应的化学方程式为_________ |
明明对冰冰的结论表示怀疑,他用图乙装置收集一瓶80%二氧化碳和20%氧气的混合气体,然后将燃着的蜡烛伸入收集的混合气体瓶中,发现_________,从而证明冰冰的结论不正确。
(实验探究2)明明为了验证猜想2,他利用手持技术实验,用O2、CO2传感器在烧杯顶部测量杯内两支蜡烛从点燃到全部熄灭后,杯内O2和CO2的浓度变化,如图丙所示,图中______(填“上方”或“下方”)的曲线表示CO2浓度的变化。反应后剩余氧气浓度为15.65%,二氧化碳浓度为1.898%,氧气浓度明显下降,二氧化碳浓度却增大不多。
(实验结论)___________。
(反思评价)根据图2中上面一条曲线(装置内氧气浓度)变化分析,在________(填“A”“B”“C”或“D”)点时蜡烛全部熄灭:请解释曲线AB段、BC段、CD段变化的原因。
AB段:_____________;BC段:___________;CD段:_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物(Y2O3)广泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含Y2O3约70%,含Fe2O3、CuO、SiO2等约30%)生产大颗粒氧化钇的一种工艺如下:
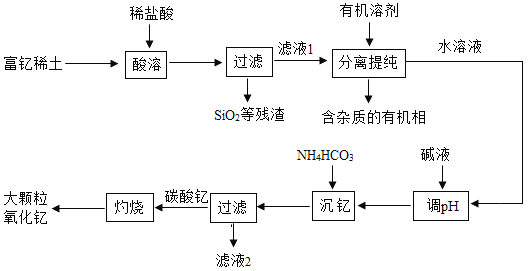
(1)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是______。
(2)“分离提纯”是为了除去滤液1中的_______(填化学式)。
(3)碳酸钇灼烧分解的化学方程式是______。
(4)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如表(D50表示颗粒直径):
实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
沉淀反应温度/℃ | 60 | 80 | 85 | 93 | 93 | 93 |
料液浓度/(kgL) | 30 | 30 | 30 | 30 | 40 | 40 |
灼烧温度/℃ | 1100 | 1100 | 1100 | 1100 | 1100 | 1100 |
氧化钇D50/μm | 6.00 | 21.65 | 35.99 | 38.56 | 35.99 | 61.34 |
分析表中数据,其他条件不变时,若将灼烧温度均升高至1400℃ ,预期所得氧化钇D50最大的是___(填实验编号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,是国际通用语言,请用适当的化学用语填空。
(1)由3个氧原子构成的单质分子:_______;
(2)两个硝酸根离子:_________;
(3)氯酸钾中氯元素的化合价:_________;
(4)氖气:_________;
(5)三个五氧化二磷分子:_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
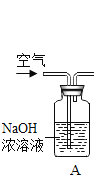
【题目】牙膏中常用碳酸钙、二氧化硅等物质作为摩擦剂。某同学对牙膏中摩擦剂碳酸钙的含量进行探究。
(实验原理)测定C装置中生成的BaCO 3 沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。
(查阅资料)CO2+Ba(OH)2=BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生。
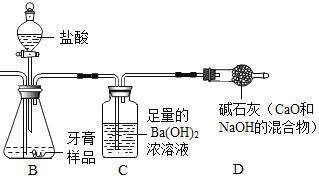
(实验装置)
根据探究过程回答下列问题:
(1)装置A中氢氧化钠溶液的作用是_____。若没有A装置,直接通入空气,则测得CaCO3的质量分数_____(填“偏大”、“偏小”或“不变”)。装置B中发生反应的化学方程式为_____。
(2)实验过程中需持续缓缓通入空气,其作用有:①搅拌B、C 中的反应物,使其充分反应;②_____。
(3)从C中过滤出BaCO3沉淀,所需的玻璃仪器有烧杯、_____和玻璃棒。
(4)只要测定装置C在吸收CO2前后的质量差,同样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,分析的原因是_______。
(5)为提高测定准确度,应采取必要措施,其中能达到目的的是____(填序号)。
①在加入盐酸之前,排净装置内的CO2气体
②放慢滴加盐酸的速度
③在A~B之间增添盛有浓硫酸的洗气装置
④在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取三份牙膏样品,每份4.0g,进行三次测定,测得生成BaCO3的平均质量为1.97g。则样品中CaCO3的质量分数为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是元素周期表中的一格,提供了氯元素的相关信息。
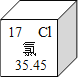
(1)氯元素的原子序数为_____。
(2)用化学符号表示氯离子_____。
(3)二氧化氯是一种常见的漂白剂,化学式为_____,其中氯元素的化合价为____。
(4)84消毒液能有效灭活新冠状病毒,它的主要成分是次氯酸钠(NaClO),使用时要注意它不能和洁厕灵(主要成分为HCl)混合共用,两者反应能生成氯化钠、水和有毒的氯气(Cl2),写出该反应的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~G是初中化学常见的物质,其中A,B常温下为无色气体且组成元素相同,C是大理石的主要成分,D、E均为黑色固体。它们之间的转化关系如图所示(反应条件、部分反应物及生成物已略去)。请回答下列问题:
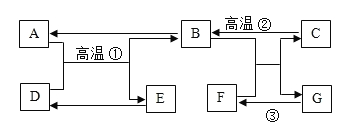
(1)F的化学式:_____。
(2)反应③的基本反应类型是_____。
(3)写出反应①的化学方程式_____。
(4)写出反应②的化学方程式_____。
(5)反应①在生产中的应用是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com