
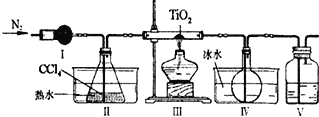
【题目】某小组以固态TiO2和气态CCl4为原料在无氧、无水的条件下制取液态TiCl4,反应的化学方程式是:TiO2(固态)+CCl4(气态)═TiCl4(气态)+CO2(气态),实验装置和相关数据如下(熔点和沸点为101.3千帕时测得)。下列分析错误的是
物质 | 熔点 | 沸点 | 其他性质 |
CO2 | -78℃ | -78℃ | 不易溶于CCl4 |
CCl4 | -23℃ | 76℃ | 与TiCl4互溶 |
TiCl4 | -25℃ | 136℃ | 遇潮湿空气产生白雾 |
A. 实验过程中应持续通入氮气
B. 热水的温度不低于76℃
C. 冰水使生成物全部液化
D. 装置V中的试剂为浓硫酸,其作用是防止空气中的水和氧气进入装置
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:初中化学 来源: 题型:
【题目】 化学兴趣小组的同学取10g铜锌合金样品于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7g时,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题:
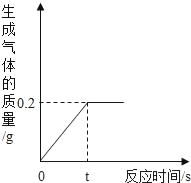
(1)样品中锌的质量为_____ g。
(2)反应后,所得溶液中溶质的质量分数为多少________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验探究是学习化学的重要途径。
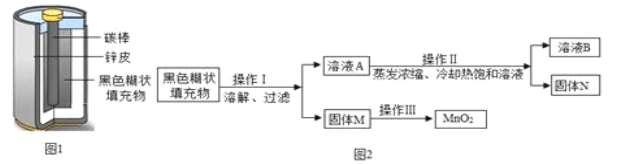
在一次实验探究活动中,老师用酸性锌锰电池与同学们一起进行实验探究,电池内部的结构如图1所示,请你一起参与他们的探究。
(查阅资料)
(1)金属锌(含有少量的铁)
(2)糊状填充物由炭黑、MnO2、ZnC12和NH4Cl等组成
(3)有关数据见下表
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
(实验探究一)老师取适量黑色糊状填充物,按图2所示实验流程进行探究。
(1)一致认为溶液A中溶质主要有_________(填写化学式;
(2)欲从固体M 中得到较纯的MnO2,操作Ⅲ可采用的简便方法是________。
(实验探究二)小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。
(3)取一块锌皮放入盛有适量稀盐酸的烧杯中, 实验中可观察到的现象是_______ 。
(4)下列各组物质混合后,也能生成ZnCl2的有_______(填字母序号)。
A ZnO与稀盐酸 B Zn与NaCl溶液 C Zn(NO3)2溶液与NH4Cl溶液
(5)化学课代表另取一块锌皮放入盛有一定CuSO4溶液的烧杯中,充分反应后得到溶液E和固体F。当溶液E中只含有一种溶质时,该溶质是______(填化学式);当固体F中只含一种物质时,溶液E中最少含有______种溶质。
(6)老师称取6.5g锌皮与足量稀硫酸完全反应,则生成氢气的质量______(填>、<、=)0.2g.
(7)某化学活动小组为测定由氧化铜和铜组成混合物中氧化铜的质量分数,取该固体混合物20g,将其加入100g某稀硫酸中,恰好完全反应,测得剩余固体的质量为4g,计算所用稀硫酸中溶质的质量分数______。(计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验中学化学兴趣小组的同学要测定某品牌纯碱样品中碳酸钠的质量分数。他们称取 12g 样品加入到 100g 水中完全溶解,然后向溶液中逐滴滴加氯化钡溶液至不再产生沉淀,共用去氯化钡溶液 150g,过滤,称得滤液质量为 242.3g。
(1)生成沉淀的质量为_______g。
(2)计样品中碳酸钠的质量分数______。(写出计算过程,计算结果保留到0.1%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是 a、b、c 三种固体物质的溶解度曲线,下列说法正确的是_____
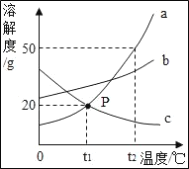
A t1℃时 a、c 的溶解度相等
B 使 t1℃时 a、b 的饱和溶液升温至 t2℃仍为饱和溶 液,需加入的 a 比 b 多
C t1℃时 a、c 的溶液中溶质质量分数一定相等
D t2℃时,将 a、b、c 的饱和溶液的温度降低至 t1℃,所得溶液中溶质质量分数大小关系为_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学学习小组从下图中选择合适的装置(称量、固定和加热装置省略),利用合适的药品,设计实验粗略测定出了铜锌合金中粉末锌的质量分数。(实验过程中不考虑水的蒸发)

实验过程:称取a g黄铜样品,加入足量稀硫酸充分反应。测定的实验数据如下。
①测定生成H2的体积为b L(氢气的密度为w g/L)。
②将反应后的剩余物过滤、洗涤、加热烘干,测定所得固体的质量为c g。
③测定……
(1)装置A中发生反应的化学方程式为______________。
(2)小昊选用三个装置进行实验,装置接口的连接顺序为_______,用①中的数据计算出铜锌合金中锌的质量分数为________(写出最终计算结果的表达式)。
(3)小烨选用装置AF进行实验,利用②中的数据计算出了铜锌合金中锌的质量分数。小聪认为小烨的方案中测定值会___________(填“偏大”、“偏小”、“不变”、“或无法确定”)。
(4)小琪仅选用装置A进行实验,利用③中的数据也计算出了铜锌合金中锌的质量分数。③中需要测定的数据是_____________。
(5)老师认为利用小昊的方案进行实验,在实验过程和操作均正确的情况下,测定值也会比实际略大,原因是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知烧杯中装有200g硫酸和硫酸锌混合溶液,其中含硫酸锌12.1g。向烧杯中逐渐加入锌粒,放出气体质量与加入锌粒质量的关系如图14所示。当恰好完全反应时,所得的溶液为不饱和溶液。
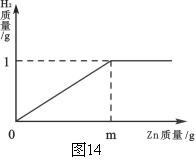
请计算:
(1)m的值。
(2)原混合溶液中H2SO4的质量分数。
(3)恰好完全反应时,所得溶液中溶质的质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色固体可能由NH4Cl、Na2 SO4、Na2 CO3、Ba(OH)2、ZnCl2中的一种或几种组成,为确定其成分,进行了如下实验,请回答下列问题.
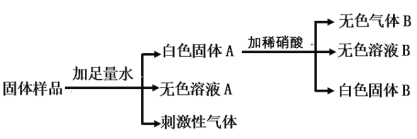
(1)刺激性气体的化学式为_____;
(2)根据流程图所示实验,能确认原白色固体中一定含有的物质是_____;
(3)取白色固体B,继续加入足量稀硝酸,若观察到仍有白色固体剩余,则产生这种剩余白色固体的反应化学方程式为_____;
(4)证明ZnCl2是否存在的实验操作为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】H2S剧毒,可用FeCl3、FeCl2、CuCl2的混合液处理并得到化工原料S(如图)。下列说法不正确的是( )

A. 在如图的转化中,化合价改变的元素有Fe、S、O
B. 该反应的总方程式:2H2S+O2![]() 2S
2S![]() +2H2O
+2H2O
C. 转化I发生的反应:H2S+CuCl2=CuS+2HCl
D. 随着反应的进行,整个溶液的pH值逐渐减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com