
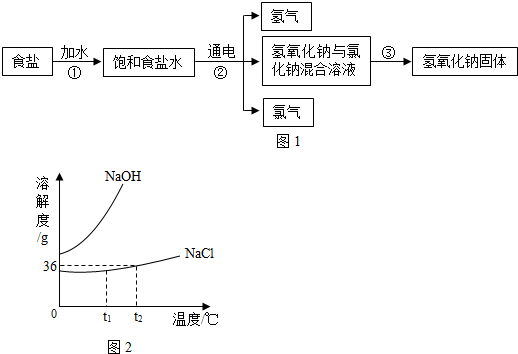
分析 (1)根据过程中涉及到的物质有食盐(盐)、饱和食盐水(混合物)、氢气(单质)、氯气(单质)、氢氧化钠(碱)进行分析;
(2)根据过程②发生反应的化学方程式为2NaCl+2X$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,可以根据质量守恒定律推断X的化学式,氯化钠中含有氯元素,氯气中含有氯元素,可以根据钠元素的化合价为+1价以及化合价规则求算对应氯元素的化合价;
(3)根据溶解度曲线图可知,分离得到氢氧化钠,曲线图显示氢氧化钠溶解度受温度影响较大,而氯化钠受温度影响较小,所以可以降温结晶,先出来的是氢氧化钠.
解答 解:(1)过程中涉及到的物质有食盐(盐)、饱和食盐水(混合物)、氢气(单质)、氯气(单质)、氢氧化钠(碱),属于属于碱的是NaOH;
(2)过程②发生反应的化学方程式为2NaCl+2X$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,根据质量守恒定律,生成物中出现了4个氢原子和两个氧原子,也就是2分子的X中含有4个氢原子和2个氧原子,则每个X分子中含有两个氢原子和一个氧原子,氯化钠中,由于钠元素为+1价,所以根据化合物中化合价的代数和为零,可得氯元素的化合价为-1价,在氯气中,由于单质中元素的化合价为零,所以含有的氯元素的化合价为0;
(3)由于氢氧化钠溶解度受温度影响较大,而氯化钠溶解度受温度变化影响较小,所以分离氢氧化钠和氯化钠得到氢氧化钠固体的方法降温结晶.
故答案为:(1)NaOH;
(2)H2O;-1,0;
(3)降温结晶.
点评 质量守恒定律,在具体使用中,是利用了元素不变,原子种类不变,原子个数不变.在实际使用时要做出准确的选择.根据方程式推断物质的化学式利用的是原子种类不变,原子个数不变进而确定化学式.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3 | 12.5 g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.lg | I2.7g |
| 性质 | Na2CO3 | NaHCO3 | 性质比较 |
| 溶液的酸碱性 | 碱性 | 碱性 | 相铜条件下,Na2C03溶液的碱性更强 |
| 热稳定性 | 稳定 | 不稳定 | NaHCO3受热分解生成Na2C03、C02 和H20 |
| 与盐酸反应 | 反应 | 反应 | 均产生CO2,但NaHCO3与盐酸的反应更加剧烈 |
| 实验方案 | 实验现象及结论 1 |
| 方案一:20℃时,在100 g水中加入11 g该白色固体,充分溶解 | 若有白色固体剩余,样品为碳酸氢钠; 否则为碳酸钠. |
| 方案二:分别将两种待测固体溶于水制成5%的溶液,用玻璃棒分别蘸取少量待测液于pH试纸上,静置,观察现象 | pH值大的为碳酸钠溶液,pH值小的为碳酸氢钠溶液. |
| 方案三:分别取少量固体于試管中加热,将产生的气体通入澄清的石灰水中. | 若石灰水变浑浊,样品为碳酸氢钠,否则为碳酸钠. |
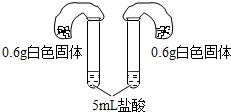
| 方案四:如阁所示,分别将气球中的白色固体全部且同时倒入装有盐酸的试管中,观察现象. | 气球胀大速度快且大的,原固体为碳酸氢钠,否则为碳酸钠 |
 【实验反思】
【实验反思】查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | SO2:“2”表示一个二氧化硫分子含有两个氧原子 | |
| B. | 2N:“2”表示两个氮元素 | |
| C. | $\stackrel{+2}{Mg}$O:“+2”表示氧化镁中镁元素的化合价为+2价 | |
| D. | 2NO3-:“2”表示两个硝酸银离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.对除杂的认识 | B.食品安全 |
| ①用稀硫酸除去Zn中混有的Ag ②用灼烧的方法除去Fe2O3中混有的C ③用碳酸钙除去CaCl2溶液中的HCl | ①霉变的大米洗净烧熟后可以食用 ②利用甲醛水溶液浸泡水产品防腐 ③补充维生素A防止夜盲症 |
| C.对现象的认识 | D.化学学科的价值 |
| ①干冰作制冷剂,因为升华时吸收大量的热 ②打开浓盐酸瓶塞,瓶口上方出现大量白烟 ③电解水生成氢气和氧气的体积比为2:1 | ①研制高效低毒农药,保障粮食生产 ②开发新型材料,改善人类生存条件 ③利用化学合成药物,保障人体健康 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com