
【题目】![]() 、
、![]() 、
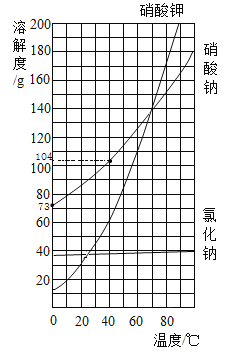
、![]() 三种物质的溶解曲线如下图所示,下列说法正确的是( )
三种物质的溶解曲线如下图所示,下列说法正确的是( )
A. ![]() 的溶解度比
的溶解度比![]() 大
大
B. 将![]() 饱和溶液降温,溶液中
饱和溶液降温,溶液中![]() 的质量分数不变
的质量分数不变
C. ![]() 饱和溶液中含少量
饱和溶液中含少量![]() ,可通过降温结晶的方法提纯
,可通过降温结晶的方法提纯
D. 将100g 40℃的![]() 饱和溶液降温至0℃,析出31g晶体
饱和溶液降温至0℃,析出31g晶体
【答案】C
【解析】
A、由图可知,当温度低于20℃时,硝酸钾的溶解度比氯化钠的溶解度小,当温度高于20℃时,硝酸钾的溶解度比氯化钠的溶解度大,题目中未指明温度,所以无法比较硝酸钾与氯化钠的溶解度大小,选项错误;
B、硝酸钾的溶解度随温度升高而增大,给硝酸钾的饱和溶液降低温度,硝酸钾的溶解度变小,溶液中会有晶体析出,则溶液中硝酸钾的质量分数会变小,选项错误;
C、硝酸钾与氯化钠的溶解度均随温度升高而增大,但硝酸钾的溶解度受温度影响较大,所以硝酸钾的饱和溶液中有少量的氯化钠,可以采用降温结晶的方法来提纯硝酸钾,选项正确;
D、由图可知,40℃时硝酸钠的溶解度为104g,0℃时硝酸钠的溶解度为73g,则将204g40℃的硝酸钠饱和溶液降温至0℃才能析出31g晶体,选项错误,故选C。


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:初中化学 来源: 题型:
【题目】中国科学院院士张青莲教授主持测定了铟等元素的相对原子质量的新值,为相对原子质量的测定做出了卓越贡献,铟元素在元素周期表中的某些信息及原子结构示意图如图所示,请回答下列问题。

(1)铟元素的相对原子质量为_____。
(2)铟原子的核电荷数为_____,在化学反应中铟原子容易_____(填“得到”或“失去”)电子。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对空气中氧气含量测定的再认识。
Ⅰ用燃烧法测定空气中氧气含量
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。

(1) 写出红磷燃烧的文字表达式_______________。
(2) 实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内___________减小,烧杯中水倒吸到集气瓶中。用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
【实验过程】
甲小组同学使用图1装置进行实验,实验前应先进行的操作是 ;
(1)用止水夹夹紧橡皮管;
(2)点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞;
(3)燃烧结束,_______________________;
(4)观察并记录水面的变化情况。
【问题提出】该小组同学多次实验发现,集气瓶内上升的水面始终小于理论值。经查阅资料知:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大。
Ⅱ 改进空气中氧气含量测定的方法
【实验改进】经查阅资料可知:常温下,铁在潮湿的空气中会生锈,因为铁与空气中的氧气、少量水反应生成铁锈(其主要成分是Fe2O3),但速度缓慢。在有食盐(NaCl)、活性炭存在条件下,反应速度较快。乙小组选择该原理,设计了如图2所示实验装置图。

【数据处理】乙小组同学用量筒测量实验前后烧杯中水的体积,测得实验数据如下表:

根据表中数据计算,改进实验后测得的空气中氧气的体积分数是___________(计算结果精确到0.1%)。
【实验反思】与燃烧红磷方法相比,乙小组方法测定空气中氧气含量的优点是___________________________。
【实验再改进】在乙组实验的基础上,丙组同学设计了如图3的装置进行氧气含量的测定,其方法如下:
【实验过程】
步骤1:在注射器中放入足量脱氧剂粉末(即食盐水、铁粉、活性炭的混合物,体积为2mL),封闭。

图3
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹。
步骤3:不断轻轻晃动注射器,至______________时停止实验。
【实验再反思】
丙小组同学的方案与乙小组的方案同学相比,优点是_________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】正常雨水因溶解了少量二氧化碳,pH为5.6,化石燃料燃烧可能产生![]() ,最终导致降雨的酸性增强,下图是形成酸雨的其中一条途径:
,最终导致降雨的酸性增强,下图是形成酸雨的其中一条途径:

(1)我们把pH_____5.6(填“>”“<”或“=”)的降雨称为酸雨。
(2)以上途径的各物质中,硫元素的化合价有_______种。
(3)为减少酸雨危害,下列措施合理的有_________(填序号)
①减少汽车尾气排放 ②禁止使用化石燃料
③将燃煤锅炉烟囱加高 ④开发风能、太阳能等新能源
(4)可用氢氧化钠溶液吸收二氧化硫,其化学方程式为______________________。
(5)![]() 通入碘水(
通入碘水(![]() 的水溶液)会生成硫酸和氢碘酸(HI),我们可利用此原理来测定空气中
的水溶液)会生成硫酸和氢碘酸(HI),我们可利用此原理来测定空气中![]() 的含量,该原理的化学方程式为___________________。
的含量,该原理的化学方程式为___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲乙丙三种固体物质的溶解度曲线
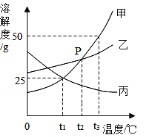
(1)P点表示_____
(2)在t1℃时,甲乙丙三种物质的溶解度大小关系是_____
(3)t1℃时,向20g甲物质中加入50g水,充分溶解后所得溶液的溶质质量分数为_____
(4)在t3℃时,将甲乙丙三种物质分别溶解在50g水中达到饱和,降温至t1℃,析出晶体多少关系是_____
(5)甲物质中含有少量乙物质,可用_____方法提纯甲物质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国海水晒盐的历史悠久。学习小组对粗盐进行提纯,并利用氯化钠进行实验探究。
Ⅰ.粗盐的提纯
粗盐中含有不溶性泥沙、可溶性CaCl2,MgCl2等杂质。学习小组设计了如下方案提纯粗盐:

(1)用化学方程式表示Na2CO3溶液的作用:_______。
(2)“过滤”中玻璃棒的作用为_____;“操作X”的名称为______。
Ⅱ.探究氨盐水与二氧化碳的反应
步骤1 取50mL.浓氨水于锥形瓶中,加入NaCl晶体至不再溶解,制得氨盐水。
步骤2 向烧瓶中加入20mL氨盐水和约16g干冰,塞紧瓶塞,振荡、静置。一段时间后溶液中析出细小晶体,过滤、用冷水洗涤晶体并低温干燥。
(提出问题)晶体的成分是什么?
(实验探究1)①经甲同学检验,晶体中不含铵盐。甲同学的实验操作及现象是_______。
②乙同学取晶体少许,加入稀硝酸,晶体溶解并产生无色气体,再滴加几滴AgNO3溶液,未见明显现象,说明晶体中不含有______离子。
(提出猜想)晶体的成分为Na2CO3或NaHCO3或两者的混合物。
(查阅资料)Na2CO3受热不分解;
NaHCO3受热易分解:2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
(实验探究2)称取m1g晶体,利用下图装置(夹持仪器略)探究晶体的成分。
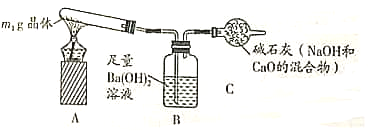
(实验现象)反应一段时间后,试管口凝结了少量小液滴,Ba(OH)2溶液变浑浊。
(实验分析)①晶体中一定含有______(填化学式)。
②将晶体加热至残留固体的质量不断改变,测得残留固体的质量为m2g。
若m1g:m2g![]() _____,说明晶体为NaHCO3。
_____,说明晶体为NaHCO3。
(拓展延伸)①氨盐水与二氧化碳反应所得铵盐的用途为_______。
②丙同学认为通过测定装置B中沉淀的质量,经计算分析也可确定晶体的组成。请对两同学的观点进行评价:________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下图回答相关问题:

(1)写出两种仪器的名称;a_________,d_________.
(2)收集干燥的![]() 气体,可选用_________(填“C”或“D”)戴置;若改用G、H和I这个组合装置收集,H装置的作用是__________________。
气体,可选用_________(填“C”或“D”)戴置;若改用G、H和I这个组合装置收集,H装置的作用是__________________。
(3)制氢气时,用B装置代替A装置的优点是__________________;若用E装置收集氢气,气体应从_________(填“b”或“c”)端进入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验:
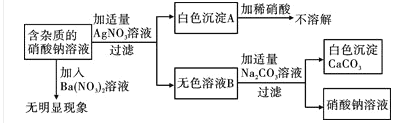
下列判断正确的是
A. 无色溶液B的溶质是硝酸钙
B. 原溶液中的杂质一定是氯化钙
C. 原溶液中的杂质可能由三种物质组成
D. 该实验中涉及的基本反应类型不止一种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硅酸钠(Na2SiO3)是我国优先发展的精细化工产品。实验室以5g石英砂粉末(其中SiO2质量分数为96%,其余为不溶于水也不与其他物质反应的杂质)为原料,与一定量NaOH溶液反应制取硅酸钠溶液,反应的方程式为:2NaOH+SiO2=Na2SiO3+H2O。充分反应后,过滤,得到硅酸钠溶液20g,滤渣洗涤、烘干,称量质量为2g。
(1)硅酸钠中钠元素、硅元素、氧元素的质量比为_____;
(2)若把20g硅酸钠溶液,稀释为质量分数为10%的溶液,求需要加入水的质量;_____
(3)求原氢氧化钠溶液中溶质的质量分数。_____(计算结果精确到0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com