
【题目】某学校环保实验小组的同学定期会对学校旁边的小河河水进行酸碱度及金属含量测定,其中操作不正确的是
A.定量量取河水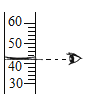 B.过滤河水泥沙
B.过滤河水泥沙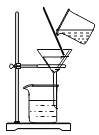 C.测定河水pH
C.测定河水pH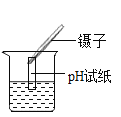 D.测定金属含量
D.测定金属含量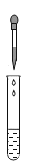
科目:初中化学 来源: 题型:
【题目】向容积为250mL的细颈玻璃仪器A中加水至虚线处,再滴几滴红墨水,一段时间后,水变红了,说明_______; 继续向体A中加酒精至凹液面最低处正好与刻线相切。塞紧玻璃塞,将A中液体倒转摇匀,重复2次。静置一段时间后,A中液面下降,说明_____。仪器A细颈部分的作用__________。
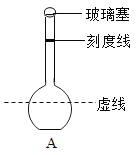
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向含有AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后,过滤,向虑出的固体中滴加稀硫酸,有气体生成,则滤出的固体中一定含有_____,滤液中含有的离子是_____ ,可能发生反应的化学反应的方程式是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所给的仪器和实验用品,回答相关问题。
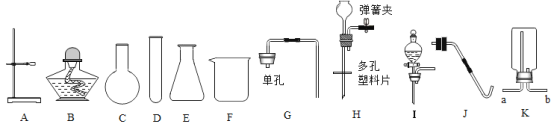
(1)仪器F的名称是______
(2)用氯酸钾和二氧化锰混合制取氧气时,反应的化学方程式为____。组装一套发生并导出氧气的装置,应选取的仪器和用品是A_____J(请补齐编号)。
(3)实验室用大理石制取CO2的化学方程式为____,若要组装一套能控制该反应随时发生和停止的发生装置,则可选择的仪器和用品是A__ (请补齐编号);若用K装置收集CO2,则气体应从_____口 (填“a”或“b”)通入。
(4)用ABCGDF及石棉网组装成一套装置,可作为实验室制取少量____的简易装置,制取时需要在C中加入几粒沸石,以防加热时出现_____
(5)下列反应均能产生氨气,在实验室制取氨气时你会选择的反应是___ (填序号) 。
①![]()
②![]()
③![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语填空:
(1)保持氩气化学性质的最小粒子:__;
(2)氧化铝中铝元素的化合价:__;
(3)下图为甲、乙、丙三种物质的溶解度曲线图,请回答下列问题:
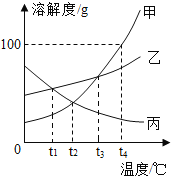
①将10g甲物质(不含结晶水)配成t4℃时的饱和溶液,需水的质量为__g。
②将t4℃时甲、乙、丙三种物质等质量的饱和溶液降温到t3℃,下列说法中正确的一项是__。
A 三种溶液仍然为饱和溶液
B 三种溶液中溶剂的质量大小关系为:甲=乙<丙
C 三种溶液溶质质量分数的大小关系为:甲=乙>丙
D 甲、乙析出晶体(不含结晶水)的质量相等,丙无晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合下图实验装置,回答问题。
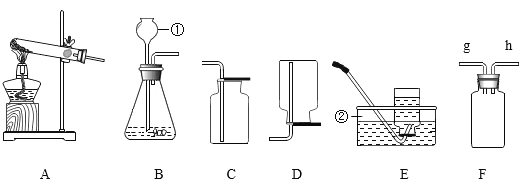
(1)请写出装置①的名称______
(2)实验室用高锰酸钾制取并收集氧气应选择的装置为______(填字母),发生反应的化学方程式为_____,制取ag氧气理论上至少需要高锰酸钾(![]() )____。(列出比例式)。
)____。(列出比例式)。
(3)某气体只能用C装置收集,写出该气体具有的性质________。
(4)用F装置可以收集氢气,氢气从h进入。请补画完整________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有10mL NaOH溶液(其中滴有少量无色酚酞溶液)的烧杯中逐滴加入稀盐酸,用pH计(用来精确测定溶液pH的仪器)测定溶液的pH,所得数据如下:
加入稀盐酸的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
烧杯中溶液的pH | 12.9 | 12.7 | 12.5 | 12.3 | 11.9 | 7.0 | 2.1 | 1.9 |
(1)当加入稀盐酸的体积为___________ mL时,NaOH溶液和稀盐酸恰好完全反应,反应的化学方程式为_____________。
(2)当加入稀盐酸的体积为3mL时,溶液显________色;
(3)当烧杯中溶液的pH=2.1时,溶液中的溶质有:__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】KNO3 的溶解度曲线如下图所示。下列说法错误的是( )
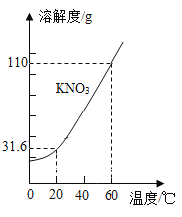
A.0~60℃,KNO3 的溶解度随温度升高而增大
B.60℃时的 KNO3 饱和溶液降温至 20℃,有晶体析出
C.20℃,100g 水中最多能溶解 31.6g KNO3
D.60℃时,可配制溶质质量分数为 60%的 KNO3 溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】胃酸过多须服用抗酸药物(能与盐酸反应),常用的抗酸药物有碳酸氢钠片、铝碳酸镁片,兴趣小组的同学对这两种药物开展如下探究。
(查阅资料)①铝碳酸镁片的主要成分的化学式为AlMg(OH)3CO3;
②抗酸原理:抗酸药物中的离子和胃酸中的氢离子反应,降低胃液酸性。
活动一:定性探究抗酸药物与“胃酸”的反应。
(1)铝碳酸镁片中含有铝离子、镁离子、氢氧根离子和碳酸根离子。结合上述知识分析,该药物起抗酸作用的微粒是_____(填化学符号)。
(2)小王取一定量碳酸氢钠片与4mLpH═1的稀盐酸(模拟胃酸)反应。药片中其他成分不溶于水也不参加反应。他对反应后溶液的成分产生了兴趣。
(作出猜想)
猜想 1:只含 NaCl;
猜想 2:_____;
猜想 3:NaCl、NaHCO3
(设计实验)
实验步骤 | 实验现象 | 实验结论 | |
实验一 | 取一定量反应后的溶液于试管中,滴加_____ | 无明显现象 | 猜想 3错误 |
实验二 | 另取一定量反应后的溶液于试管中,______ | ______ | 猜想 2正确 |
实验二中涉及反应的化学方程式为______。
活动二:定量探究抗酸药物与“胃酸”的反应,对比分析产生 CO2的速率快慢和中和酸的能力强弱。
如图 1,利用数字化实验分别测定碳酸氢钠片、铝碳酸镁片与“胃酸”反应时,产生 CO2的速率快慢和 pH的变化,得到“二氧化碳浓度与时间”曲线(如图 2)、“pH与时间”曲线(如图 3)。
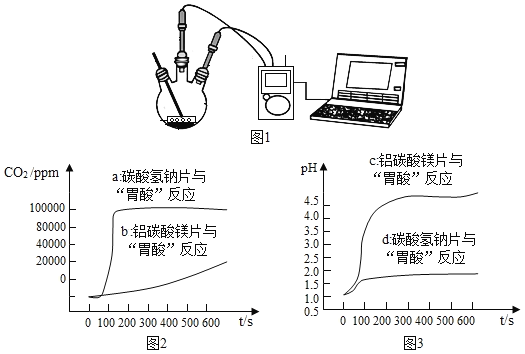
(1)服用碳酸氢钠片更易造成胃胀气,原因是_____。
(2)铝碳酸镁片中和酸的能力更强,理由是_____。
(反思与提升)日常生活中,我们应该根据个人的具体病情,选择合适种类的胃药。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com