草酸晶体(H
2C
2O
4?2H
2O)熔点较低,加热会熔化、气化和分解.草酸(H
2C
2O
4)受热会分解,它与氢氧化钙的反应为:H
2C
2O
4+Ca(OH)
2=CaC
2O
4↓(白色)+2H
2O.
甲、乙两同学对草酸受热分解的产物作如下探究:
(1)猜想与假设:第一种:草酸分解生成CO
2和H
2;第二种:草酸分解生成CO
2、CO和H
2O;
第三种:草酸分解:H
2C
2O
4→CO
2↑+H
2O(未配平);
有同学从理论上就可判断第三种假设不成立,老师也认为这一判断是正确的,该同学判断的理论依据是
.
(2)设计与实验:
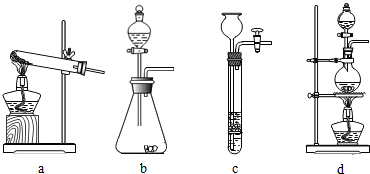
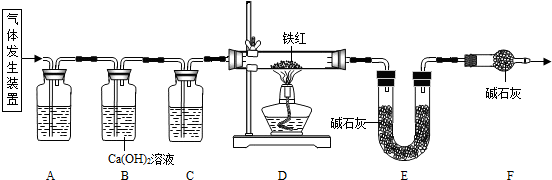
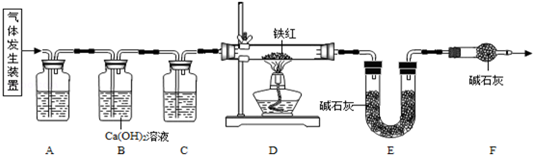
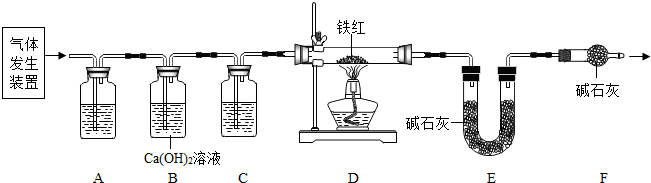
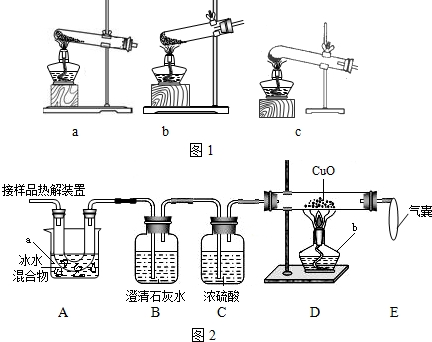
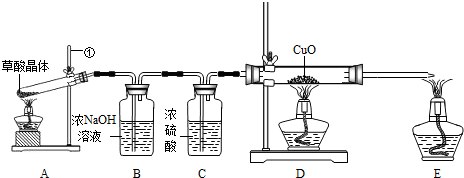
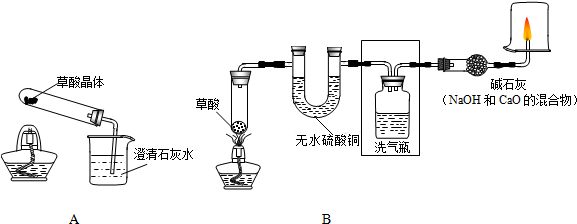
甲、乙两同学分别设计了下图所示的A、B两套实验装置(图中铁架台略去).
①甲同学按A装置实验,观察到澄清石灰水变浑浊,认为此现象是由草酸晶体受热分解产生的CO
2所导致,此判断 不严密(填“严密”或“不严密”).
②乙同学的B装置图方框内的仪器未画完整,请你帮他画完整(直接画在图上或答题卡上).
乙同学按B装置实验,看到无水硫酸铜由白变蓝,洗气瓶中溶液变浑浊.在尖嘴管口点燃剩余气体,火焰上方罩一个
烧杯,有白色固体生成,证明产物中有
;换一个干、冷烧杯罩在火焰上方,内壁无现象,证明产物中无H
2.
(3)结论与思考:
①草酸受热分解的化学方程式为:
.
②若省略B装置方框内的仪器,整套装置也能证明产物中有CO
2(假设每步都反应完全),方法是:
.




 口算题天天练系列答案
口算题天天练系列答案