
【题目】学习了MnO2可催化过氧化氢溶液分解制取氧气后,某同学猜想Al2O3 能否起到类似MnO2的催化作用呢?于是进行了以下探究。
[猜想与假设]
猜想1:Al2O3不是催化剂、也不参与反应,反应前后质量和化学性质不变;
猜想2:Al2O3参与反应并产生O2,反应前后质量和化学性质发生了改变;
猜想3:Al2O3是反应的催化剂,反应前后_____。
[实验设计]用天平称量Al2O3 0.2 g,取5 mL 5%的过氧化氢溶液于试管中,进行如下实验:
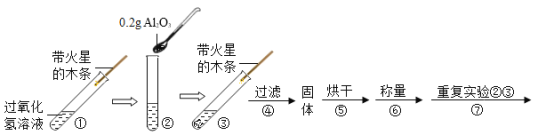
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
溶液中有气泡放出带火星的木条复燃 | 称量Al2O3的质量仍为0.2 g | 溶液中有大量气泡放出_____, | 猜想3成立 |
(2)步骤①③的目的是_____。
(3)写出Al2O3 催化过氧化氢溶液分解产生氧气的文字表达式:_____。
[继续探究]氧化铝是否比二氧化锰的催化效果更好?
小雨以生成等体积的氧气为标准,设计下列三组实验(其他可能影响实验的因素均忽略):
实验序号 | 5%过氧化氢溶液体积 | 催化剂种类及质量 | 待测数据 |
① | 5 mL | ||
② | 5 mL | 0.5 g Al2O3 | |
③ | 5 mL | 0.5gMnO2 |
(4)上述实验测量的“待测数据”是_____。
(5)若测得实验②的数据比实验③的数据大
[实验反思]
(6)影响过氧化氢溶液分解产生氧气快慢的因素还可能有:_____(写两种)。
(7)请设计实验验证你的其中一种猜想:_____。
【答案】质量和化学性质不变 带火星的木条复燃 探究氧化铝是否能加快过氧化氢的分解速率 过氧化氢![]() 水+氧气 收集等量氧气所需时间 MnO2 反应物的浓度、温度 在相同温度下,取不同浓度的过氧化氢溶液分别加入等质量的二氧化锰粉末,观察哪个生成气泡的速度更快
水+氧气 收集等量氧气所需时间 MnO2 反应物的浓度、温度 在相同温度下,取不同浓度的过氧化氢溶液分别加入等质量的二氧化锰粉末,观察哪个生成气泡的速度更快
【解析】
[猜想与假设]:Ⅲ、催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变;故填:质量和化学性质不变;
[实验设计](1)氧化铝对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象是有大量气泡产生,带火星的木条复燃;故填:带火星的木条复燃;
(2)步骤①③的目的是探究氧化铝是否能加快过氧化氢的分解速率;故填:探究氧化铝是否能加快过氧化氢的分解速率;
(3)Al2O3催化过氧化氢溶液分解产生氧气和水;故填:过氧化氢![]() 水+氧气;
水+氧气;
(4)本题的实验目的证明氧化铝能加快过氧化氢的分解,所以“待测数据”是收集等量氧气所需时间。故填:收集等量氧气所需时间;
(5)若测得实验②的数据比实验③的数据大,说明MnO2对过氧化氢溶液分解的催化效果更好。故填:MnO2;
[实验反思](6)影响化学反应快慢的因素很多,如反应物的浓度、温度、催化剂的颗粒大小、接触面积等,故填:反应物的浓度、温度;
(7)探究反应物的浓度对反应速率的影响可设计如下实验:在相同温度下,取不同浓度的过氧化氢溶液分别加入等质量的二氧化锰粉末,观察哪个生成气泡的速度更快;故填:在相同温度下,取不同浓度的过氧化氢溶液分别加入等质量的二氧化锰粉末,观察哪个生成气泡的速度更快。


科目:初中化学 来源: 题型:
【题目】下图是“空气中氧气体积分数测定”实验的两种装置图。甲图的集气瓶容积为200mL,预先装进50mL的水;乙图是对甲实验的改进,加热粗铜丝白磷即被点燃(白磷的燃点为40℃,燃烧产物与红磷相同)
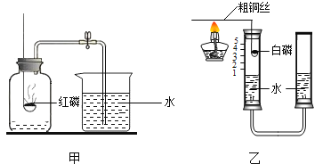
(1)该实验中红磷燃烧的现象____。若用甲图进行实验,获得成功最终集气瓶中水的体积约为__mL;该实验还可推知出氮气性质有____(任写一点)
(2)集气瓶里预先装进的50mL水,在实验过程中所起的作用____(填序号)
A 加快集气瓶内气体冷却 B 液封导气管末端以防气体逸出 C 吸收五氧化二磷
(3)与甲比较乙装置的好处____(写一点)。
白磷燃烧的文字表达式或符号表达式____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)从海水中获得的氯化镁电解可以得到镁和氯气。镁是一种银白色金属,具有密度小、硬度小的性质,其合金被广泛用于军事、航空工业中。镁过去还被用于照相机的闪光灯,称作“镁光灯”,这是由于镁条在空气中点燃,与氧气反应发生燃烧,发出耀眼的白光,同时生成氧化镁。
①上述叙述中,描述镁的物理性质有_______;描述镁的化学性质有__________。
②用文字表达式表示上述叙述中的两个化学变化,并指出反应的类型。
反应一:文学表达式为_______,反应类型为___________;
反应二,文字表达式为_______,反应类型为___________。
(2)下图是配制溶脂质量分数为10%的NaCl溶液的实验操作示意图:
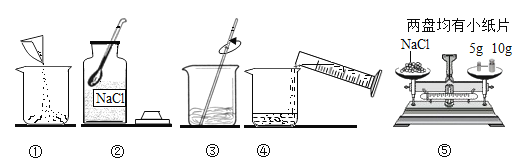
①在溶液的配制过程中,玻璃棒的作用是_______。
②称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数见下图,则制取的NaC1溶液的质量为________。
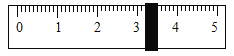
量取读数时,视线与液体的______保持水平:读数时,目光俯视刻度线,则所配溶液的溶质质量分数______(填“偏大”、“偏小”或“无影响”)。
③称量NaCl质量完毕放回砝码时,发现有一个砝码生锈了(锈未脱落),若其他操作步骤正确,则所配溶液的溶质质量分数______(填“大于”、“小于”或“等于”)10%。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年3月,国务院总理李克强在政府工作报告中强调:“坚决打好蓝天保卫战”山西省积极行动,落实整改措施,省城太原首先通过以下三种方式缓解空气污染初见成效。



A.电动出租车 B.垃圾清扫车 C.喷水雾汽车
(1)为了使空气更新,天空更蓝,你作为环保小卫士,认为推广使用上述方式的好处是 (任选一项回答)
(2)空气污染严重损害人体健康,影响作物生长,破坏生态平衡引起空气污染的有害气体种类很多,请举一例 (用化学式表示)
(3)你认为改善空气质量的措施正确的是
a.推广使用新能源
b.加强企业排污管理
c.雾霾多发天气,实行私家车限号出行。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C是初中化学中常见物质,A、B都是纯净物,且两种物质由相同的元素组成,C为气体单质,能使带余烬的木条复燃,它们之间有如图2-3-7所示的转化关系(反应条件和部分反应物已略去),请推断并回答:
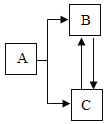
(1)物质A是(物质名称):A_____,B_____,C_____。
(2)写出A生产B和C的方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国“页岩气”总储量居世界第一。“页岩气”是存在于片层状岩石缝隙中的气体,主要成分为甲烷,还含有少量的乙烷等。
(1)“页岩气”属于_____(填“纯净物”或“混合物”)。
(2)加压后,25m3的“页岩气”可以装入0.024m3的钢瓶中,用微粒的观点解释:_____
(3)下图为乙烷分子的结构示意图。

①乙烷中碳元素与氢元素质量比为_____。
②乙烷在空气中完全燃烧的化学反应方程式是_____。
(4)“页岩气”作为燃料燃烧产生大量二氧化碳,造成的环境问题是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学家侯德榜在1926年生产出纯度为99%的“红三角”牌纯碱(Na2CO3),为世界制碱工业作出突出的贡献。化学小组用氯化钡(BaCl2)溶液测定某纯碱样品纯度,有关化学反应(杂质不参与反应)原理为Na2CO3 + BaCl2 = BaCO3↓+ 2NaCl 。若该纯碱样品质量2.15 g,充分反应后产生的BaCO3质量为3.94 g。求:
(1)参加反应的Na2CO3的质量_____。
(2)该纯碱样品的纯度为多少?_____(结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明同学想在实验室完成模拟炼铁的实验,设计下图①→④的思路。已知方框内是初中常见气体制取的发生装置,可供选择的装置见图A或B,提供选择的药品是:氯酸钾晶体、过氧化氢溶液、二氧化锰粉末、稀盐酸、块状石灰石

(1)写出图中标号a、b、c的仪器名称: a是______,b是_______,c是_______;
(2)若用A装置放入①方框内,则X是氧气,写出生成氧气的化学方程式_______;
(3)若用B装置放入①方框内,且能控制反应发生与停止,则X气体______(填能或不能)是氧气,写出生成X气体的化学方程式_____;
(4)③中玻璃管内固体由____色逐渐变成___色,说明氧化铁与一氧化碳反应生成了铁,该化学方程式为______,该反应______(填属于或不属于)置换反应;
(5)④中试管内出现白色浑浊,该化学方程式为_____;④中尾气处理的化学方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图回答问题
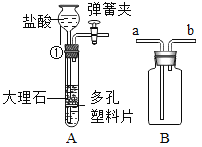
(1)仪器①的名称是_______,A装置的优点是___________, 如果用A装置制取氧气,反应的化学方程式是__________
(2)B装置在化学实验中有广泛的用途:
① 集气:用排水法收集氧气,可在B装置装满水后,使氧气从_______(填“a”或“b”)口进入;
② 储气:若要将储存在B中的氧气排出,水应从________(填“a”或“b”)口进入;
③ 量气:若用B装置测量收集到的气体体积,还必须要增加的仪器是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com