


科目:初中化学 来源: 题型:
| 实验操作步骤 | 实验目的、现象及结论 |
| (1)取少量白色固体粉末,配成水溶液,向其中加入足量的稀酸A,A为___________ | 除去____________________ |
| (2)继续加入足量的B,B为___________ | 除去硫酸钠 |
| (3)向(2)中的滤液中加入C,C为__________溶液 | 若有_________,证明原白色固体粉末中肯定含有氯化钠;否则不含氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
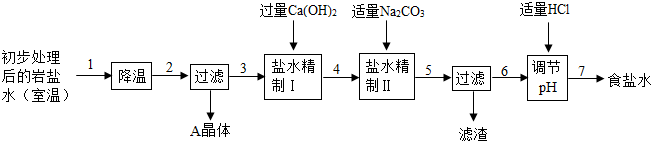
 某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.
某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶 | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 解 | 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 |
| 度 | 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 |
| /g | 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 |
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量 | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量 | 180.3 | 202.6 | 226.4 | 251.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
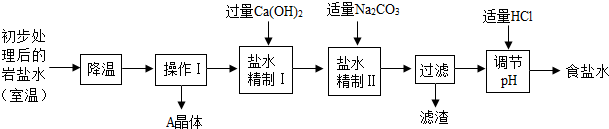
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
查看答案和解析>>
科目:初中化学 来源:广州 题型:填空题
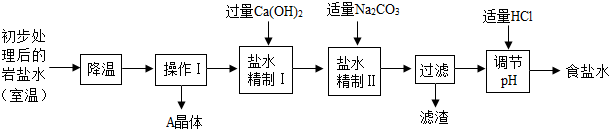
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
查看答案和解析>>
科目:初中化学 来源:崇文区二模 题型:问答题
| 实验操作步骤 | 实验目的、现象及结论 |
| (1)取少量白色固体粉末,配成水溶液,向其中加入足量的稀酸A,A为_______ | 除去_________________________ |
| (2)继续加入足量的B,B为_______ | 除去硫酸钠 |
| (3)向(2)中的滤液中加入C,C为___溶液 | 若有_________,证明原白色固体粉末中肯定含有氯化钠;否则不含氯化钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com