

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:初中化学 来源: 题型:
| 资料卡: 侯氏制碱法的原理可以表示为: NaCl+H2O+NH3+CO2 =NaHCO3↓+NH4Cl 2NaHCO3?Na2CO3+CO2 ↑+H2O该同学设计了如图中的装置进行实验,测定市售纯碱样品中碳酸钠的质量分数.(水蒸气的影响忽略不计,夹持装置已略去)  主要实验步骤如下: ①按图组装仪器,并检查装置的气密性; ②称量5.5g市售纯碱样品放入烧瓶中,加适量蒸馏水溶解,得到试样溶液; ③从分液漏斗滴入稀硫酸,直到不再产生气体时为止; ④缓缓鼓入一定量的N2; ⑤称量B瓶及溶液的质量,发现增重2.2g. 请回答下列问题: (1)写出A中发生反应的化学方程式 (2)鼓入一定量的N2的目的是 (3)如果将分液漏斗中的稀硫酸换成浓盐酸,测试的结果(填偏高、偏低或不变) (4)该样品中碳酸钠的质量分数为 (5)若用与上述实验反应原理不同的实验来测定纯碱样品中碳酸钠的质量分数,请用化学方程式表示实验原理 查看答案和解析>> 科目:初中化学 来源: 题型: (2009?哈尔滨)某兴趣小组的同学们以“稀硫酸与氢氧化钠溶液能否发生反应”为课题进行了科学探究.同学们在烧杯中加入10mL稀硫酸.滴入几滴酚酞试液,接着分两次向烧杯中滴入氢氧化钠溶液.第一次滴加几滴氢氧化钠溶液后,不断搅拌,第二次继续滴加氢氧化钠溶液至过量.则第一次滴加氢氧化钠溶液时,溶液中溶质(不考虑酚酞)的质量变化情况是 H2SO4逐渐减少,Na2SO4逐渐增多 H2SO4逐渐减少,Na2SO4逐渐增多 :第二次滴加氢氧化钠溶液时观察到的现象是溶液由无色变为红色 溶液由无色变为红色 .由上述实验同学们得出了稀硫酸与氢氧化钠溶液能发生反应的结论.[提出问题]是否可以用其他试剂证明稀硫酸与氢氧化钠溶液能发生反应呢? [甲组实验]实验过程如图所示:现象:向a试管中滴加氢氧化钠溶液时无明显现象,再滴加几滴硫酸铜溶液时出现蓝色沉淀.结论:用硫酸铜溶液可以证明稀硫酸与氢氧化钠溶液能发生反应. [乙组实验]实验过程如图所示:现象:向b试管中滴加氢氧化钠溶液时无明显现象,再滴加几滴氯化钡溶液时出现白色沉淀.结论:用氯化钡溶液可以证明稀硫酸与氢氧化钠溶液能发生反应.   [交流评价]请你评价甲、乙两组同学由实验现象获得的结论是否正确,并说明理由.  查看答案和解析>> 科目:初中化学 来源: 题型: 某同学在查阅资料时得知:市售纯碱样品常混有氯化钠杂质. 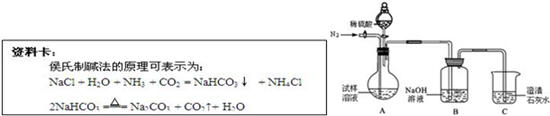 该同学设计了如图中的装置进行实验,测定市售纯碱样品中碳酸钠的质量分数.(水蒸气的影响忽略不计,夹持装置已略去) 主要实验步骤如下: ①按图组装仪器,并检查装置的气密性; ②称量5.5g市售纯碱样品放入烧瓶中,加适量蒸馏水溶解,得到试样溶液; ③从分液漏斗滴入稀硫酸,直到不再产生气体时为止; ④缓缓鼓入一定量的N2; ⑤称量B瓶及溶液的质量,发现增重2.2g. 请回答下列问题: (1)写出A中发生反应的化学方程式 Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ .(2)装置C中澄清石灰水的作用是 防止空气中二氧化碳进入B装置 防止空气中二氧化碳进入B装置 .(3)该样品中碳酸钠的质量分数为 96.4 96.4 %(结果保留到小数点后一位).查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解 某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验. I、实验方案 方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,测得的pH逐渐变小直到pH小于7,则证明NaOH溶液与稀盐酸发生了化学反应. (1)反应后,所得溶液显 酸 酸 性(填“酸”、“碱”或“中”)(2)用pH试纸测定NaOH溶液pH时,正确的操作是: 用干燥的玻璃棒蘸一滴NaOH溶液滴在干净的白瓷板或玻璃片上,再把试纸显示的颜色与标准比色卡比较,即可得出溶液的pH 用干燥的玻璃棒蘸一滴NaOH溶液滴在干净的白瓷板或玻璃片上,再把试纸显示的颜色与标准比色卡比较,即可得出溶液的pH .(3)简述强调“测得的pH小于7”的理由: 排除因稀释而使溶液pH减小的因素 排除因稀释而使溶液pH减小的因素 .方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应. 该组同学将不同浓度的盐酸和NaOH溶液各10克混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
7 7 .(5)某同学在没使用温度计的情况下,通过图1所示装置完成了实验.则该同学根据实验现象: U形管中左边液面下降 U形管中左边液面下降 ,判断NaOH溶液与稀盐酸发生了中和反应.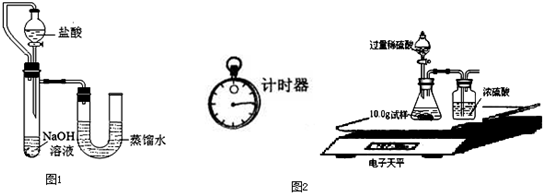 II、实验中的意外情况 在实验过程中,他们发现盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;②可能是Na2CO3; ③可能是NaOH和Na2CO3. (6)小明同学取白色粉末少许,溶于水后,先向溶液中加入足量的 CaCl2或BaCl2 CaCl2或BaCl2 溶液,看到白色沉淀产生,然后向上层清液中加入酚酞试液,看到溶液呈红色,验证了猜想③是正确的.(7)为了进一步研究,三位同学取了10.0g上述样品,利用电子天平共同做了图所示的实验. 实验数据记录如下:
(8)有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是(实验操作均正确): CO2的密度比空气大,残留在装置中,造成最终测得的质量偏大,测得生成的CO2质量偏小,故Na2CO3的质量分数偏小 CO2的密度比空气大,残留在装置中,造成最终测得的质量偏大,测得生成的CO2质量偏小,故Na2CO3的质量分数偏小 .查看答案和解析>> 科目:初中化学 来源: 题型: (2013?鞍山一模)用如图的装置分离CO2和CO的混合气体并测定其中CO2的体积分数.图中a,b,c,d均为活塞,可以控制气体的通过和液体的加入.请选择适宜的试剂完成实验. 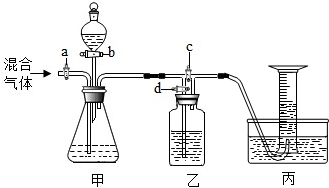 供选用的试剂有:①稀硫酸;②澄清的石灰水;③氢氧化钠溶液(试剂均足量). 实验分以下两步进行: (1)关闭b,c,打开a,d通入混合气体.则甲中发生反应的化学方程式为: CO2+2NaOH═Na2CO3+H2O CO2+2NaOH═Na2CO3+H2O .若乙装置中的现象是澄清石灰水不变浑浊 澄清石灰水不变浑浊 ,说明甲装置中反应是充分的.(注:假设装置中的该气体全部被回收)丙装置中用充满水的倒立量筒收集气体,若通入500mL混合气体,量筒中就会收集到200mL气体,则混合气体中CO2的体积分数为60% 60% ;如果某同学在读取图中量筒数据时俯视读数,则所读取的气体体积会< < 200mL(填“>”“<”或“=”).(2)闭关a,d,打开b,c,让分液漏斗中试剂缓缓流下即可产生另一种气体.则收集该气体应该使用 向上排空气 向上排空气 法.查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |