
【题目】在托盘天平的两端各放一只等质量的烧杯,在两只烧杯中分别加入等质量、等质量分数的足量的稀盐酸,调节天平平衡.向左边烧杯中加入8.4g 碳酸镁,若使天平仍然保持平衡,需向右盘烧杯中加入
A.8.4g碳酸氢钠B.8g氧化铁
C.4.5g铝粉D.4g铜锌合金
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:初中化学 来源: 题型:
【题目】在人类社会的发展进程中,金属起着重要的作用。
(1)青铜是铜锡合金,其属于_______________(填 “金属材料”或“合成材料”) ;
(2)工人师傅常用稀盐酸除铁锈,其反应的化学方程式是___________________;
(3)生铁和钢是使用最多的金属材料,二者性能不同的原因是.___________________;工业上采用赤铁矿石(主要成分为氧化铁)炼铁的反应原理是___________________(用化学方程式表示)。
(4)向硝酸银和硝酸铝的混合溶液中加入一定量的铁粉,观察到溶液由无色变为浅绿色后,对混合物进行过滤,则滤液中一定含有的溶质是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年“119”消防宣传月活动的主题是“防范火灾风险,建设美好家园”。每个人都应该了解消防知识,增强消防安全意识。
(1)由如图所示实验可知,燃烧所需的条件是:______、温度要达到可燃物的着火点、______。
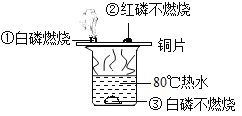
(2)在家中使用天然气时,若发现天然气泄漏,应_____(选填序号)。
A 关闭气源阀门
B 打开门窗
C 立即打开抽油烟机
(3)目前人们利用最多的能源是煤、石油和天然气等化石燃料。煤燃烧会产生二氧化氮、二氧化硫、一氧化碳等有害气体。氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中华传统节日的习俗蕴含了许多化学知识。
(1)端午节——赛龙舟吃粽子。每当粽子煮熟的时候,一股股的清香扑鼻而来,从微观角度分析,能闻到清香的原因是_____;一些不法商贩为了使粽叶的色泽更加鲜艳,会用硫酸铜浸泡粽叶,硫酸铜在化合物分类中属于______。
(2)中秋节-------吃月饼赏月。月饼是传统美味食品,月饼制作时用到面粉、蔗糖、鸡蛋、精炼油、肉松等原料,其中富含糖类的是_____;某些独立包装的月饼中还会附一袋含铁粉的脱氧剂,其脱氧原理是_________________。
(3)春节-------买爆竹放烟花。 由于燃放烟花爆竹会污染环境,引发火灾,近年来很多地方禁止燃放烟花爆竹,某烟花的火药中添加了锑粉,已知锑在周期表中的部分信息及其原子结构示意图如图所示,下列说法正确的是_____ ( 填选项,双选)。
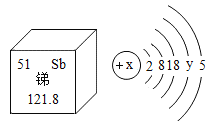
A 锑是一种非金属元素
B 锑的相对原子质量为121.8g
C 图中y=18
D “Sb”可表示一个锑原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO和Fe3O4。为了测定铁红中铁的质量分数,兴趣小组的同学称取10.0 g铁红样品进行如下实验:
[资料]①草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解: 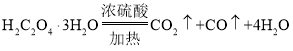 ;②碱石灰的主要成分是CaO和NaOH。
;②碱石灰的主要成分是CaO和NaOH。
[设计实验]利用图一装置__使草酸晶体分解,然后将草酸分解产物通入图二装置进行实验。
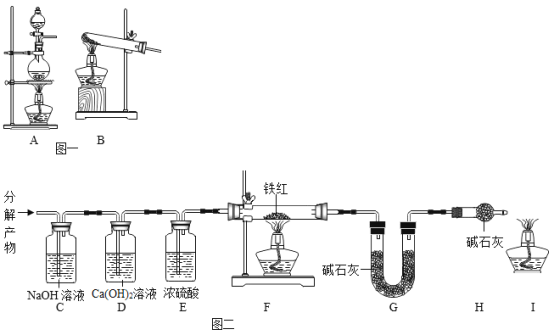
[实验分析]
(1)D装置的作用是____。
(2)对F装置加热前和停止加热后,都要通入过量的CO,其作用分别是①加热前,_____;②停止加热后,___________。
(3)写出F装置玻璃管中所发生反应的一个化学方程式:_____。
[数据记录]铁红样品质量为10.0 g,充分反应后称得G装置增重6.6g。
[数据处理]此铁红中铁的质量分数是_______。
[实验评价]如果缺少E装置,则测得样品中铁的质量分数会__ (填“ 偏小”“不变”或“偏大”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知 A 是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,它受热可分解为三种化合物,物质转化关系如图所示.其中 C、F、H、I是无色气体,B 通电时,在阴极产生I,在阳极产生 H.根据推断回答下列问题:
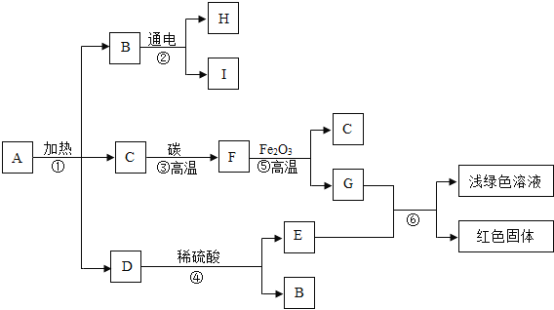
(1)铜锈的主要成分是碱式碳酸铜. 铜生锈与空气中氧气和水有关,还与空气中的_____________ (填化学式)有关;
(2)E 物质的化学式是_________;
(3)在①~⑥反应中属于化合反应的是_________ (填数字序号);
(4)反应⑤的化学方程式为 ________________,该反应体现了F 的_________性.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是“××牌发酵粉”的部分信息,课外化学兴趣小组的同学对其进行了如下探究:

[查阅资料]
(1)酒石酸是一种易溶解于水的固体有机酸;
(2)发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2;
(3)Na2CO3受热不分解。
[提出问题]
NaHCO3在发酵粉加水或加热时如何产生CO2?
[猜 想]
甲.……
乙.酒石酸与NaHCO3在溶液中反应产生CO2;
丙.NaHCO3加热产生CO2。
[实验探究]
(1)小明同学取少量NaHCO3粉末于试管中,加入适量水,无气体产生,从而否定了猜想甲,则猜想甲是______;小明又将酒石酸溶液和NaHCO3溶液混合,产生了CO2,从而验证了猜想乙,说明了NaHCO3具有的性质之一是______。
(2)小英同学为探究猜想丙设计了如图所示的实验装置。
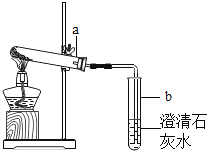
小英另取适量NaHCO3粉末加入a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊。b试管中反应的化学方程式为_____。
持续加热直至两支试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末,向该粉末中滴加稀盐酸,有CO2产生,说明该粉末是______。
[小结]
NaHCO3在发酵粉中产生CO2的条件是_____。此发酵粉的保存方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用木炭还原氧化铜的实验装置如图所示.
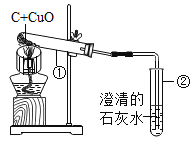
(1)①中反应的化学方程式为:________
(2)该实验成功的关键是保证碳粉与氧化铜粉末干燥并充分混合,充分混合的目的是________,实验中通常氧化铜和碳粉的质量比为10:1时实验效果更好,使碳过量的目的是________.
(3)标志着反应发生的实验现象是________.
(4)小红按氧化铜和碳粉的质量比10:1的比例混合后,给混合物加热,始终没有得到铜,可能的原因是(写一种)________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】选择下列部分实验操作可完成两个实验,甲实验为除去粗盐中难溶性的杂质,乙实验为配制溶质质量分数为10%的氯化钠溶液。下列说法正确的是( )
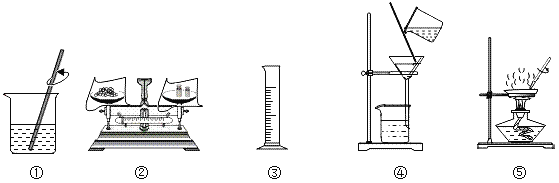
A. 操作①和⑤中玻璃棒的作用是相同的
B. 甲实验和乙实验都要用到的实验操作①
C. 甲实验在操作⑤时,将水全部蒸发后停止加热
D. 乙实验在操作③时,若俯视读数,会使所配制溶液的溶质质量分数偏小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com