
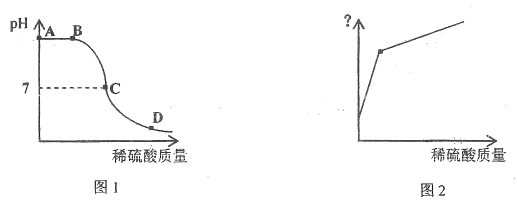
【题目】某恒温容器中盛有NaOH饱和水溶液且仍有部分NaOH固体剩余,向容器中缓慢滴加稀硫酸,经测定,溶液pH随加入稀硫酸质量的变化如图1所示,(已知溶液中![]() 浓度越大,溶液碱性越强;
浓度越大,溶液碱性越强;![]() 浓度越大,溶液酸性越强)
浓度越大,溶液酸性越强)
(1)写出实验过程中发生反应的化学方程式_____________
(2)从A点到B点过程中,溶液所含溶液NaOH的质量____(填“不变”或“变大”或“变小”)。
(3)写出D点对应溶液的溶质__________(填化学式)。
(4)图2中纵坐标可表示________(填序号)。
①溶剂质量 ②溶液质量 ③NaOH溶质质量分数
【答案】 2NaOH + H2SO4 ==Na2SO4 + 2H2O 变大 Na2SO4 和H2SO4 ①②
【解析】(1)稀硫酸与氢氧化钠反应生成硫酸钠和水,反应方程式为2NaOH + H2SO4 ==Na2SO4 + 2H2O。(2)因为容器中盛有NaOH饱和水溶液且仍有部分NaOH固体剩余,当加入稀硫酸时,溶剂质量增多,没有溶解的NaOH固体继续溶解,所以从A点到B点过程中,溶液所含溶质NaOH的质量变大。(3)D点溶液的pH<7,溶液显酸性,稀硫酸剩余,故溶液中的溶质有生成的Na2SO4及剩余的H2SO4。(4)①加入稀硫酸时,溶剂质量增多,增多的质量是生成水的质量和稀硫酸中水的质量的总和,当氢氧化钠完全反应后,溶剂增多的质量是稀硫酸中溶剂的质量,故反应过程中溶剂质量增加的快,正确;②加入稀硫酸时,由于溶剂质量增多,没有溶解的NaOH固体继续溶解,溶液增加的质量是溶解的NaOH固体的质量与加入稀硫酸的质量之和,当NaOH固体完全溶解后,溶液增加的质量等于加入的稀硫酸的质量,正确;③随着稀硫酸的加入,溶液中NaOH的质量逐渐减少到零,错误。故选①②。


科目:初中化学 来源: 题型:
【题目】根据大量的实验总结得出酸碱盐之间相互发生复分解反应的条件是:生成物中有沉淀、气体或水。依据该条件,某化学小组的同学推断稀硫酸和氯化镁溶液不能发生复分解反应。为了进一步确认该推断的可靠性,该小组同学将一定量稀硫酸和一定量氯化镁溶液在烧杯中混合后,进行了如下探究活动。
(1)甲同学取烧杯中混合溶液分别进行以下两个实验,记录实验现象如下。请依据实验现象填写实验结论:
实验 | 实验现象 | 实验结论 |
| 溶液变红 | 溶液中含有_____(写离子符号) |
| 产生白色沉淀 | 溶液中含有_____(写离子符号) |
(甲同学的结论)稀硫酸与氯化镁溶液没有发生反应 | ||
(2)乙同学看到甲同学的实验报告后,认为甲同学的结论不正确,原因是_____。为了进一步确认两者没发生反应,还需检验烧杯内的混合液中是否含有氯化镁。于是,乙同学设计了如下两个实验:
①取少量烧杯内的混合液于试管中,逐滴加入过量的_____溶液,证明了混合液中含有Mg2+.整个实验过程中乙同学观察到的实验现象是_____。
②乙同学另取少量烧杯内的混合液,通过实验成功地检验出混合液中含有Cl﹣.他设计的方案为_____(写出操作和现象)。
(总结)通过上述实验,该小组同学证明了稀硫酸和氯化镁溶液确实没有发生反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硬水受热后会产生水垢,水垢的主要成分是 CaCO3 和 Mg(OH)2。实验室由水垢制取纯净 CaCl2 固体的流程如下:(水垢中其它成分不参与反应),请按要求填空:

⑴ 试剂 A 的名称为_______________。
⑵ 试剂 B 的化学式是___________,若加入的试剂A、B都是过量的,则加入试剂 B 发生的非中和反应的化学反应方程式是_______________。操作Ⅰ的名称是__________,该操作中除用到玻璃仪器外,还需要的实验用品有_________。
⑶ 酸化过程加试剂 A 的作用__________________________。
⑷“操作Ⅱ”包含的操作有:蒸发浓缩、______________、过滤、洗涤、干燥等。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】欲测定盐酸与氯化钙的混合溶液中氯化钙的质量分数,进行了如下实验:取混合溶液100g于锥形瓶中,向其中逐渐加入一定溶质质量分数的碳酸钠溶液(如图一),并不断测定锥形瓶中溶液的pH.反应过程中所得溶液的pH与锥形瓶中物质的总质量的关系如图二所示。其中,当锥形瓶中溶液的质量增加至147.8g时,共消耗碳酸钠溶液的质量为50g。(忽略二氧化碳在水中溶解的量;氯化钙溶液显中性。)

(1)m点的数值是_____。
(2)a→b段表示碳酸钠与混合溶液中的_____反应。
(3)参加反应的碳酸钠溶液的溶质的质量分数是_____。
(4)请计算原混合溶液中CaCl2的质量分数为_______(写计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸(HNO3)是实验室常见的一种酸。实验小组对硝酸的某些性质进行研究。
Ⅰ.挥发性
(实验1)取一瓶质量分数为68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到________,是由于挥发出来的硝酸蒸体遇到空气里的水蒸气形成硝酸小液滴的缘故。
Ⅱ.不稳定性
(查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体。
(1)硝酸分解的化学方程式为:4HNO3 ![]() 4NO↑+O↑+_____。
4NO↑+O↑+_____。
(实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26℃)。记录溶液上方的气体颜色随时间的变化情况。
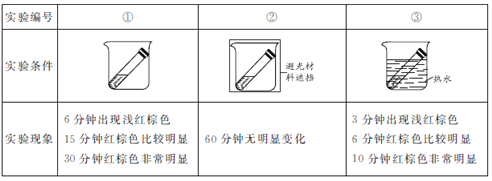
(2)实验①、②对比是研究______对浓硝酸稳定性的影响。
(3)实验①、③对比可得出的结论是_______。
Ⅲ.酸性
(查阅资料2)硝酸能够与金属氧化物反应生成盐和水。
(实验3)向氧化铜粉末中加入硝酸,能够看到的现象是_______。
IV .氧化性
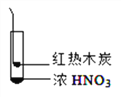
(查阅资料3) 浓硝酸在加热条件下能与木炭发生反应:C+4HNO(浓) ![]() 4NO↑+CO↑+2H2O。
4NO↑+CO↑+2H2O。
(实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能有________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示是实验室制取气体的常用装置,请根据要求回答问题:
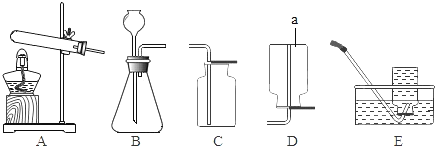
(1)利用装置B制取氧气时,反应的化学方程式是_________________________________;实验时,锥形瓶内长颈漏斗要插入液面以下,其原因是______________________________________;
(2)已知:氨气(NH3)是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水,实验室常用加热氯化铵和熟石灰两种固体的混合物来制备氨气。请你从如图中选出制备一瓶氨气所需要的装置组合是____________________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图示中 A 为生活中使用最多的金属,C 为胃酸的主要成分,G 为蓝色沉淀。各 物质间的反应均在溶液中进行,相互转化关系如下图所示。
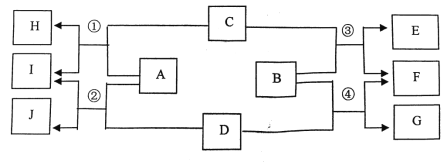
请回答以下问题:
(1)B 溶液中的阴离子是_____,E 的化学式为_____
(2)反应②的化学方程式________
(3)①②③④四个反应中属于复分解反应的是_____
(4)H 的一种用途_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一包固体粉末可能含有Na2CO3、FeCl3、CaCl2、NaOH中的一种或几种,为了探究它的成分,进行了如下实验:
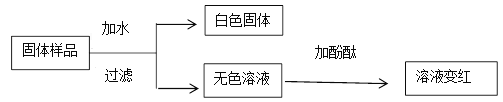
(1)推断粉末中一定含有的物质有哪些?_________________
(2)为了确定可能含有的物质,请设计实验证明(简要写出实验操作、现象和结论)。_________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组对酸、碱、盐的部分性质进行探究。
(探究一)氢氧化钠与二氧化碳反应
甲同学设计实验方案如图1所示
(1)实验现象为______,甲同学由此判断氢氧化钠和二氧化碳发生了反应。
(2)小组内其他同学认为甲同学方案不完善,理由是______。
(探究二)氢氧化钠和盐酸发生中和反应时放出热量。
乙同学向一定量10%的氢氧化钠溶液中滴加10%的盐酸,滴加过程中温度变化如表
加入盐酸体积V/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
混合溶液温度 T/℃ | 15.2 | 19.6 | 22.0 | 26.0 | 28.2 | 26.7 | 25.7 | 24.7 | 23.7 | 22.9 |
(3)反应的化学方程式为_____。
(4)根据表中数据分析混合溶液温度变化的原因_____。
(5)小组内其他同学提出“将10%的盐酸直接滴入氢氧化钠固体中也能得出相同结论”,你认为是否合理并说明理由_____。
(6)丙同学将甲同学和乙同学实验后的溶液混合,未发现明显现象。现将混合液中的氯化钠进行提纯,具体的操作为______。
(探究三)碳酸钠溶液与稀盐酸的分步反应
(查阅资料)向碳酸钠溶液中逐滴加入稀盐酸的反应是分步反应,第一步反应生成碳酸氢钠和氯化钠,当碳酸钠反应完后才发生第二步反应。
丁同学向106g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为3.65%的稀盐酸,生成二氧化碳的质量变化如图2所示(不考虑CO2的溶解)。
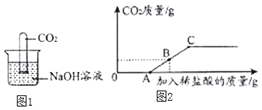
(7)A→C段发生反应的化学方程式为____。
(8)若B点横坐标为150,则其纵坐标为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com