
【题目】根据图示实验、部分记录和溶解度曲线,判断下列说法正确的是( )

A. 无法判断a中溶液是否为饱和溶液
B. c中溶液溶质的质量分数为33.3%
C. b中溶液在加热过程中始终为饱和溶液
D. 常用冷却热的饱和溶液的方法获得氯化钠晶体
科目:初中化学 来源: 题型:
【题目】“宏现微现符号”是化学独特的表示物质及其变化的方法。请完成下列问题。
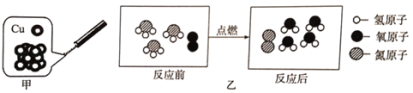
(1)图甲中“Cu”表示多种信息,如铜元素、铜单质,还能表示___。
(2)经研究发现氨气(NH3)燃烧的产物没有污染,且释放大量能量,有一定应用前景。其反应的微现示意图如图乙所示,请将其补充完整__。该反应的化学方程式为__,从宏观角度看,该反应前后没有变化的是__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤,课外小组同学决定对蚁酸进行探究。
(查阅资料)
(1).蚁酸化学名称叫甲酸,化学式为HCOOH
(2).蚁酸在一定条件下会分解生成两种氧化物
(3).白色无水硫酸铜粉末遇水变蓝
(提出问题)蚁酸的酸碱性及分解产物是什么?
(猜想与假设)
猜想①:蚁酸的分解产物是水和二氧化碳;
猜想②:蚁酸的分解产物是水和一氧化碳;
猜想③:蚁酸的分解产物是一氧化碳和二氧化碳。
经讨论,小组同学认为猜想③是错误的,理由是____。
(实验探究)
(1).探究蚁酸的酸碱性。
用pH试纸测得蚁酸溶液的pH值____7(填“>、<或=”),证明蚁酸溶液呈酸性。
(2).探究蚁酸分解的两种产物。
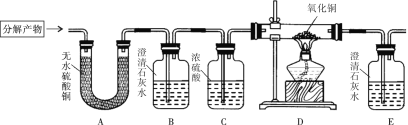
为了确认蚁酸分解的所有产物,小组同学设计实验,将蚁酸分解的产物通入下图所示的实验装置,并观察现象。
(现象与结论)
实验中观察到A中无水硫酸铜变蓝,B中澄清石灰水未变浑浊,D中黑色粉末逐渐变红, E中澄清的石灰水变浑浊。
(1)写出E中发生的反应的化学方程式____;
(2)通过对实验现象的分析,上述猜想____正确。
(实验反思)
(3)从环保的角度考虑,上述实验装置设计上存在的不足之处是____。
(拓展应用)
(4)人们被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒,下列物质中你会选择的物质是____。
A NaOH溶液 B 食醋 C 食盐水 D 肥皂水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图,回答有关问题:
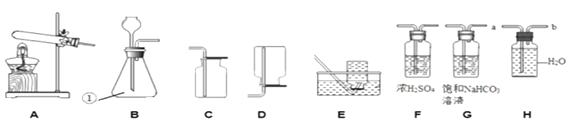
(1)仪器①的名称是__。
(2)从节能环保方面考虑,实验室制取较纯净的O2, 应选择的发生与收集装置是__(填序号),发生反应的化学方程式为___,反应物中氧元素的化合价为___。
(3)组装 A 装置时,酒精灯应在固定试管之_______(填“前”或“后”)放置,该装置一般用于____固体(填“药品名称”)制氧气时使用,试管口的棉花团作用是___。写出用一种白色固体制取氧气的化学方程式____。
(4)如果用大理石和浓盐酸制取CO2,常混有HCl气体,为了得到一瓶纯净干燥的二氧化碳,连接装置的顺序____,其中除去HCl气体时发生的反应的化学方程式为_____。
(5)对于制取CO2后剩下的溶液甲同学进行探究,取少量的溶液滴加无色酚酞试液,溶液无色,甲同学猜想剩余溶液一定是氯化钙溶液。(氯化钙溶液显中性)大家一致认为甲同学实验不能证明他的猜想,理由是___。如果要证明甲的猜想是正确的,可以选择____(填字母)来代替酚酞试液。
A 石蕊试液 B 氢氧化钠溶液 C 稀硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习化学离不开实验
(实验Ⅰ)下图是实验室常用的实验仪器与装置,根据所学知识回答下列问题:
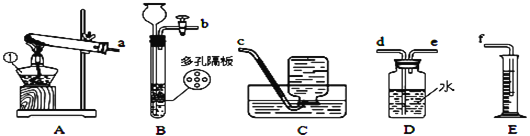
(1)写出图中编号仪器名称:①_____。
(2)用高锰酸钾制取氧气时,所选用的发生装置还需添加的实验用品为_____,反应的化学方程式为_____。若用D装置对氧气进行干燥,可将其中的水换成_____。
(3)为了粗略测定加热一定质量的高锰酸钾所收集到氧气的体积,整套实验装置导管接口的正确连接顺序是a→_____(依次填导管接口,用a、b、c……表示);
(4)实验室若用装置B制取二氧化碳,多孔隔板上常放置的药品应为_____(填名称)
(实验Ⅱ)实验室从氯酸钾和二氧化锰完全反应后的固体混合物中回收二氧化锰和获得产物氯化钾,并配制100g7.5%的氯化钾溶液。
(1)从完全反应后的固体混合物中获得氯化钾的步骤是:溶解→_____→蒸发
(2)蒸发时玻璃棒的作用为_____。
(3)用量筒量水仰视读数,所配溶液溶质质量分数_____7.5%。(填“>”、“=”或“<”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化钠、氢氧化钙是两种常见的碱
(1) 它们有一些相似的化学性质,其原因是溶液中都含有________
(2) 可作某些气体干燥剂的是________
(3) 用氢氧化钙溶液检验二氧化碳,反应的化学方程式为 __________。
(4) 根据化学方程式计算,用7.4kg氢氧化钙能中和硫酸厂排放的污水中硫酸的质量是多少________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组欲分离KCl和BaCl2混合溶液,得到都含单一溶质的两种溶液。他们设计了如下图所示的实验流程:

供选试剂:K2SO4溶液、Na2CO3溶液、K2CO3溶液、盐酸、稀硫酸
(1)步骤①中,分离A、B的实验操名称是_____,试剂a是_____
(2)沉淀B表面残留少量滤液,需用蒸馏水多次洗涤,为了检验沉淀B是否洗涤干净,可向步骤②的最后一次洗涤液中加入的试剂是______(双选,填序号)。
A NaOH溶液 B CaCl2溶液 C NaCl溶液 D AgNO3和HNO3混合溶液
(3)步骤③中,发生反应的化学方程式为______
(4)要达到预期的日的,还需要改进的方法为______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组对课本中“氯化钠能用于制烧碱”的内容产生兴趣,查阅资料得知:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
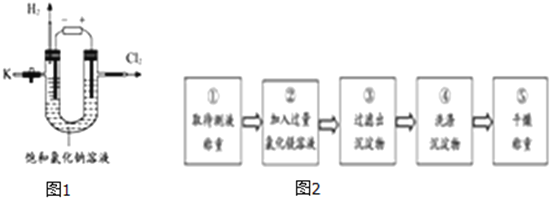
为验证该反应能制烧碱,同学们用如图1装置进行了电解饱和氯化钠溶液的实验,通电一段时间后,关闭电源,从K处倒出溶液作为待测液进行如下探究.
(探究一)检验待测液中含有氢氧化钠
检验含有氢氧化钠的方法是 __________________________.
(探究二)测定待测液中氢氧化钠的质量分数
查阅资料:
Ⅰ.氢氧化镁不溶于水.
Ⅱ.氢氧化钠与氯化镁溶液能发生复分解反应,化学方程式为:________.
进行实验:实验步骤如图2所示.
(1)步骤②加入的氯化镁溶液必需过量,其目的是 _______________.实验过程中,判断所加氯化镁溶液是否过量的方法是 ______________.
(2)实验过程中若缺少步骤④的操作,则测定的待测液中氢氧化钠的质量分数将 ________(填“偏大”、“偏小”或“没影响”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某补钙剂说明书的部分信息如图1所示。化学兴趣小组准备测定该补钙剂中有效成分的质量分数,取10片钙片加入稀盐酸至不再产生气泡为止(其他成分既不溶于水,也不与盐酸反应)。并绘制了加入稀盐酸的质量与放出气体质量的关系图如图2,则回答:
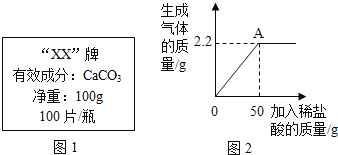
(1)反应生成了二氧化碳气体为______g;A点表示的意义是______。
(2)求该种钙片中主要成分的质量分数。_____。
(3)求加入稀盐酸中溶质的质量分数。_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com