
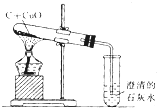
 在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:
在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下: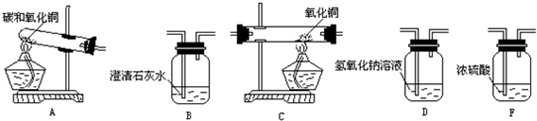
| 实验操作 | 实验现象 | 实验结论 |
| 取7.2g红色固体放入烧杯中,向其中加入足量的稀硫酸,充分反应后,静置 | 若无现象 | 证明红色固体是 |
| 若 |
证明红色固体中肯定含有 |
| 实验操作 | 实验现象 | 实验结论 |
| 铜(或Cu) | ||
| 无色溶液变蓝色,仍有红色固体剩余. | 一定有Cu2O,可能有Cu |
| 144 |
| 7.2g |
| 64 |
| x |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
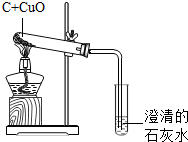 在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如下图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:
在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如下图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下: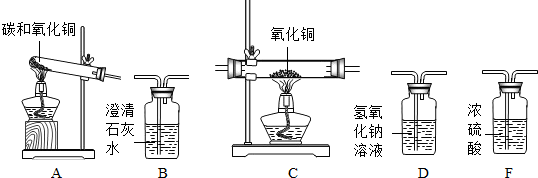
| 实验操作 | 实验现象 | 实验结论 |
| 取7.2g红色固体放入烧杯中,向其中加入足量的稀硫酸,充分反应后,静置 | 若无现象 | 证明红色固体是________ |
| 若______,______ | 证明红色固体中肯定含有 _____,可能含有_____ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如下图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:
在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如下图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:
| 实验操作 | 实验现象 | 实验结论 |
| 取7.2g红色固体放入烧杯中,向其中加入足量的稀硫酸,充分反应后,静置 | 若无现象 | 证明红色固体是________ |
| 若______,______ | 证明红色固体中肯定含有 _____,可能含有_____ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com