
【题目】某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究。(查阅资料)
①生产原料粗盐中含有少量可溶性杂质(MgSO4和CaC12)及不溶性杂质,生产过程中需先将粗盐精制。
②生产原理: ![]() 分离得晶体A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
分离得晶体A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
③氯化铵分解的化学方程式是: ![]()
④部分生产流程如图所示:
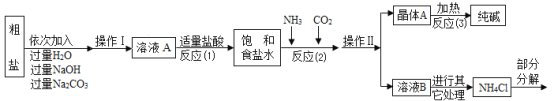
(问题讨论)
(1)①写出加入NaOH溶液所发生反应的化学方程式_______;
②操作I的名称是_________;
③反应(1)中加入适量盐酸的目的是_________;
(2)上述生产流程中可循环使用的物质是_______(填字母)。
A NH3
B NaOH
C HCl
D CO2
【答案】![]() 过滤 除去Na2CO3和NaOH ACD
过滤 除去Na2CO3和NaOH ACD
【解析】
(1)①粗盐中含有硫酸镁,加入氢氧化钠,氢氧化钠与硫酸镁反应生成氢氧化镁和硫酸钠,该反应的化学方程式为:![]() ;
;
②操作I可将难溶性物质除去得到溶液,故名称是过滤;
③向粗盐中加入过量水溶解,然后加入过量氢氧化钠,氢氧化钠与硫酸镁反应生成氢氧化镁和硫酸钠,加入过量碳酸钠,碳酸钠与氯化钙反应生成碳酸钙和氯化钠,加入适量稀盐酸,稀盐酸能与氢氧化钠反应生成氯化钠和水,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,可除去过量的氢氧化钠和碳酸钠;
(2)![]() ,
,![]() ,碳酸氢钠加热分解为碳酸钠、二氧化碳和水,故二氧化碳、氯化氢、氨气既是反应物,又是生成物,可以循环利用。故选ACD。
,碳酸氢钠加热分解为碳酸钠、二氧化碳和水,故二氧化碳、氯化氢、氨气既是反应物,又是生成物,可以循环利用。故选ACD。


科目:初中化学 来源: 题型:
【题目】化学实验小组的同学们对催化剂产生了兴趣,通过查阅资料了解到氧化铁也能加速氯酸钾的分解。为了探究氧化铁能否加快过氧化氢的分解,他们设计了实验装置,并进行气体的制备和测量实验。实验时均以生成40mL气体为标准,相关实验数据记录如下表:
实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 过氧化氢溶液温度/℃ | 氧化铁的用量/g | 收集40mL氧气所需时间/s |
① | 5 | 10 | 20 | 0 | 128.5 |
② | 5 | 10 | 20 | 1.2 | 16.8 |
③ | 15 | 10 | 20 | 1.2 | 10.5 |
④ | 5 | 10 | 70 | 0 | 32.7 |
(1)完成上述实验及数据的测定需要用到下图中的部分装置,请按组装顺序写出所用到的装置代号____。
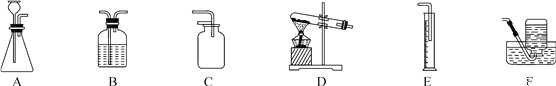
(2)通过实验①和④对比可知,化学反应速率与温度的关系是_______;通过实验②和③对比可知,化学反应速率与______有关;通过实验_______和______对比可知,氧化铁可以加快过氧化氢分解放氧的速率。
(3)若要证明氧化铁是过氧化氢分解的催化剂,还需要验证它在该反应前后的___和____未发生改变。
(4)同学们还想探究催化剂的颗粒大小对化学反应速率是否有影响,请你帮他们设计实验方案进行探究:_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体所需的装置如下图所示。
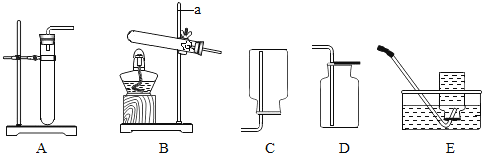
请回答以下问题。
(1)实验仪器 a 的名称是___________。
(2)用高锰酸钾制取氧气的化学方程式为__________,所选用的发生装置为_________(填字母序号,下同),收集装置为__________。
(3)用过氧化氢溶液和二氧化锰制取氧气的化学方程式为____________。所选用的发生装置也可做实验室制备二氧化碳的发生装置,该装置是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,小琪用该实验验证质量守恒定律。
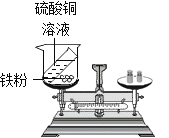
(1)请用简洁的语言,描述该实验的现象。______
(2)请书写出该反应的化学方程式。______
(3)若将硫酸铜溶液换为稀硫酸,还能验证质量守恒定律吗?为什么? ______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图为a、b、c三种物质的溶解度曲线,据图回答:
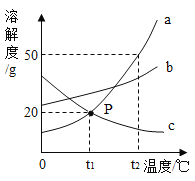
(1)t2°C时a的溶解度是_________,该温度下a物质的饱和溶液中溶质的质量分数是______;
(2)P点的含义是_______;
(3)t2°C时将a物质100g加入到200g水中充分搅拌,形成溶液的质量是_______g;
(4)若b中含有少量a,要提纯b,应用________;
(5)某温度下c物质的在不改变溶质质量分数的前提下将不饱和溶液转变为饱和溶液,可采用的方法是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一密闭容器中,有X、O2、CO2、H2O四种物质,在一定条件下发生某种反应,反应一段时间后,测得反应前后各物质的质量如下表。下列说法正确的是( )
物质 | X | O2 | CO2 | H2O |
反应前的质量/g | 19 | 34 | 6 | 2 |
反应后的质量/g | 11 | 待测 | 28 | 20 |
A.表中的待测值为32
B.X 中可能含有氧元素
C.该反应是置换反应
D.该反应中CO2和H2O的化学计量数之比为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室现有药品石灰石、氯酸钾、二氧化锰、稀硫酸、稀盐酸、碳酸钙、碳酸钠、澄清石灰水及相关仪器和用品,请结合下列装置回答问题:
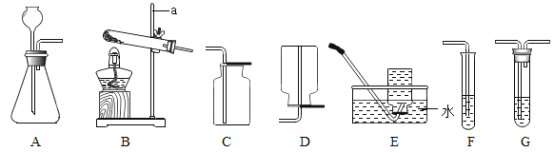
(1)①若用上述药品制取较纯净的氧气,发生反应的化学方程式为_________,选择的装置组合是_______(填字母)。如何检验收集到的气体是氧气_________。
②仪器a的名称是_______。在连接发生装置和收集装置时,将胶皮管和玻璃管连接 在一起的操作是先把_____,然后稍稍用力即可把玻璃管插入胶皮管。
(2)①若用上述药品制取二氧化碳,药品的名称是_________,选择装置的组合是_______(填字母),实验中若二氧化碳没有收集满可能的原因是_________。
②若制取干燥的二氧化碳,需要在发生装置和收集装置之间连接________装置(填字母),该装置中的药品名称是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是镁元素在元素周期表中的信息及三种粒子的结构示意图,下列说法正确的是

A.镁的相对原子质量为24.31g
B.①对应的元素属于金属元素
C.②在化学反应中容易失去电子
D.③的粒子符号为Mg
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲醇是一种新型燃料电池的燃料,甲醇的性质与乙醇(酒精)相似。
(1)根据物质的分类,甲醇(化学式为CH3OH)属于_____(填“有机”或“无机”)化合物;
(2)甲醇燃料电池可用作手机电池,工作时直接将化学能转化为_____能。写出甲醇在空气中完全燃烧的化学方程式为_________________________________。
(3)工业酒精中常含有甲醇,误食工业酒精后会使人眼睛失明,甚至死亡。下面关于甲醇的说法中正确的是_____(填序号)。
a.甲醇由碳、氢、氧三种元素组成
b.一个甲醇分子中共有5个原子
c.甲醇中碳、氢、氧三种元素的质量比为3:1:4
d.甲醇由甲醇分子构成
(4)工业制取甲醇的方法之一:利用二氧化碳与氢气在一定条件下反应制取甲醇,同时生成另一种常见物质A,相关化学方程式为CO2+3H2 CH3OH+A,则A的化学式为_____。若由上述化学工艺利用22g CO2可制备出甲醇_____g。
CH3OH+A,则A的化学式为_____。若由上述化学工艺利用22g CO2可制备出甲醇_____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com