
【题目】固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线如右图所示。下列说法错误的是
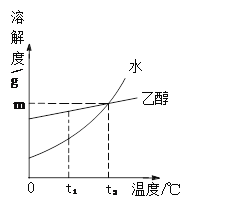
A.物质w在乙醇中的溶解度随温度的升高而升高
B.t1℃时,物质w在水中的溶解度小于在乙醇中的溶解度
C.将t2℃时物质w的水溶液降温至t1℃有晶体析出
D.t2℃时,物质w在水中与在乙醇中的溶解度都为m g
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】A、B、C、D、E是初中化学常见的物质,C是胃液中帮助消化的物质,D是大理石的主要成分。其相互反应情况如右图所示,“一”表示物质之间能反应,“→”表示一种物质能一步转化成另一种物质。
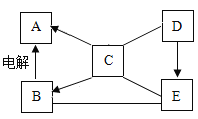
(1)D生成E的化学方程式为____。
(2)B与E的反应为__(填“ 吸热”或“放热”)反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室现有高锰酸钾、稀盐酸、大理石、棉花及下列仪器。请回答问题:
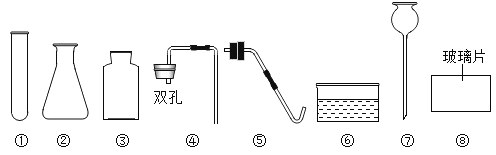
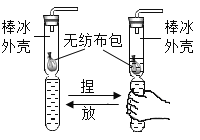
(1)若利用上述仪器和药品制取二氧化碳气体,选择的仪器是_____(填序号)。如用下图的简易制取装置,则无纺布包里装的药品是_______,制取气体时反应的化学方程式为_______,该装置的优点是_______(写一点)。
(2)若利用上述仪器和药品制取氧气,缺少的仪器是_______。制取氧气时,先检查装置气密性,确认装置不漏气后,装入少量药品并加热,导管口开始出现气泡时不宜立即收集,当气泡_______地放出时,再把导管口伸入盛满水的集气瓶口。停止加热时,先把_______,再_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】正确选择实验仪器是实验成功的重要保证,下面是实验室中常见的仪器,请按要求填空。
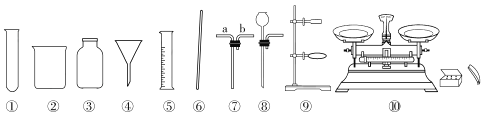
(1)配制一定溶质质量分数的氯化钠溶液,需用到的仪器有______(填序号),还缺少的两种仪器是_______(填名称);过滤粗盐水所用到的仪器有_______(填序号)。
(2)实验室用锌粒和稀硫酸制取氢气,可选上述仪器中的________(填序号)组合成发生装置。
(3)利用仪器③与⑦可组合成一个贮气装置,收集氢气(氢气难溶于水、密度小于空气)时,气体应从仪器⑦的________(填“a”或“b”)端通入。该装置还有其他的用途,请你任举一例:______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一种工业废水其中含有大量硫酸亚铁,少量硫酸铜和硫酸钠。现设计一种经济又合理的方法回收金属铜和硫酸亚铁晶体,其主要流程如图所示:

(1)请写出工业废水中加入铁粉后发生反应的化学方程式________________。
(2)操作Ⅰ为________,进行操作I前加入稀硫酸的目的是________________,能否用稀盐酸代替?____(填“能”或“不能”),原因是________________。
(3)实验室稀释浓硫酸的具体操作为________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验小组的同学在用锌粒与下图硫酸溶液(试剂瓶标签部分腐蚀)反应时,发现有气泡产生,并闻到有刺激性气味。他们对此气体的成分进行了探究。

[提出问题]锌粒加入该硫酸溶液反应生成的气体是什么?
[查阅资料]①浓硫酸与锌反应,但不产生氢气,也不会产生氧气,能生成二氧化硫气体;
②二氧化硫有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色。
[猜想与假设]甲同学认为:气体可能是H2;
乙同学认为:气体可能是SO2;
丙同学认为:气体还可能是_____。
[实验探究]为了验证上述猜想,同学们在老师的指导下设计了如下图的装置(部分夹持器材略去,假设每个能发生的反应都进行完全)进行探究:
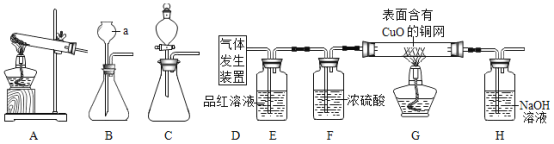
(1)图2中D处气体发生装置可选图1中的_____(填字母序号)。
(2)实验开始后,观察到E中品红溶液褪色,证明气体中含有_____。
(3)写出H装置中发生反应的化学方程式_____。
(4)G装置在点燃酒精灯加热之前应先通段时间的气体。目的是_____加热段时间后,观察到_____,证明气体中含有H2。
[实验结论]_____同学的猜想是正确的。
[反思与交流]
①锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么反应过程中又产生了氢气呢?用文字简述原因:_____。
②锌与浓硫酸、稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是_____(任填一种合理的答案)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的![]() ]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
[提出问题]该瓶溶液中溶质的成分是什么?该瓶溶液中亚硫酸钠的质量分数是多少?
[查阅资料]
a、Na2SO3有较强还原性,在空气中易被氧气氧化:![]() ;
;
b、Na2SO3能与酸反应产生SO2气体;
c、SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
[作出猜想]
猜想1:没有变质,成分是Na2SO3;
猜想2:完全变质,成分是Na2SO4;
猜想3:部分变质,成分是Na2SO3和Na2SO4。
[实验探究I]甲组设计实验探究溶液是否变质:
甲组 | 实验操作 | 现象 | 结论 |
步骤1 | 取少量样品于试管中加入过量稀盐酸。 | 产生气泡 | 溶液中含有_____ |
步骤2 | _____ | _____ | 溶液中含有Na2SO4 |
实验结论是_____。
[实验探究Ⅱ]乙组设计如下实验测定Na2SO3溶液的溶质质量分数。
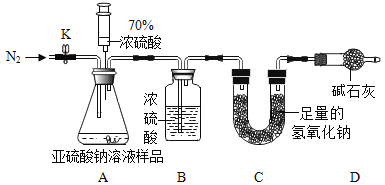
(1)连好装置并检查装置气密性,在锥形瓶中放人126g该样品,通入N2的目的是_____。
(2)实验前称量C装置的质量为128.8g。
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡,注射器可以换为_____,也能控制液体试剂的滴加速率。
(4)打开活塞K,缓缓鼓入一定量的N2,继续通入N2的作用是_____。
(5)再次称量C装置的质量为135.2g。
(6)计算出该溶液中Na2SO3的质量分数为10%,若没有D装置,实验结果将_____(填“偏大”“不变”或“偏小”)。
[反思]由此可得出,保存亚硫酸钠时应_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源、材料、环境、健康问题越来越引起人们的重视。
(1)下表列出的是某品种西瓜每100g食用部分的主要营养成分数据。
营养成分 | 水分 | 蛋白质 | 脂肪 | 糖类 | X | 钙铁锌 |
质量 | 92.5g | 0.7g | 0.2g | 6.1g | 6.8mg | 17.1mg |
①表中“X”是指人体所需六大基本营养素中的_________。
②脂肪是由_________元素组成(填元素符号),________有机高分子化合物(填“属于”、“不属于”)
③西瓜营养成分中属于微量元素的是_________(填元素符号),人体中若缺少__________(填元素符号)元素,则可能易患佝偻病。
(2)能源是国家经济发展的命脉。
①煤、天然气和___________都属于化石燃料。
②燃油汽车尾气中含有二氧化氮,排放到大气中会形成________,对环境造成污染。
③现有三种发电方式:A.风力发电,B.太阳能发电,C.火力发电。其中,A的能量转化方式是把_________能经过一系列变化转化成电能。与C相比,A、B发电的共同优点是___________(写一条)。
(3)大飞机C919用的化学材料如甲图。请回答:

①橡胶属于__________材料;
②图乙是钛(Ti)原子结构示意图,则x=______,钛元素在化学变化中易________(填“得”或“失”)电子变成______(填离子符号)。
③铁比铝的强度大,但制造飞机却用铝合金而不用铁合金,主要原因是铝比铁的密度小且抗腐蚀性能强;金属铝具有很好的抗腐蚀性的原因是____ (用化学方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com