
【题目】实验是学习化学的一种重要途径
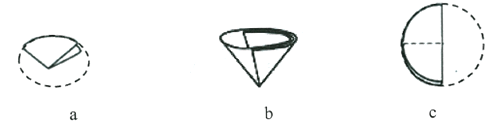
(一)、实验室用下图所示装置制取并收集气体

请回答下列各题:
(l)仪器① 的名称_________,②的名称__________。
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是_______________(填序号),反应的化学方程式是____;若用排水法收集氧气时不能刚有气泡就开始收集,原因是_______________。
(3)既能收集氧气也能收集二氧化碳气体的装置是______(填序号),检验二氧化碳气体是否收集满的方法是__________________;检验瓶中气体是否为二氧化碳可用_____________(填药品名称)。
(4)乙炔(C2H2)气体可用电石(CaC2块状固体)和水反应来制取,化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑,实验室制取乙炔(C2H2)气体的发生装置应选用_____(填序号)。
(二)、某化学兴趣小组的同学利用下图微型实验装置进行探究实验。

(1)请写出一个双球管中可能反应的化学方程式__________________________。
(2)挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,据此现象可说明燃烧需要的条件是_________。
(3)相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气最多的是_________。
【答案】 酒精灯 集气瓶 A 2KMnO4 ![]() K2MnO4+MnO2+O2↑ 刚开始冒出的气体中含有空气,会使收集的气体不纯 C 将一根燃着的木条靠近集气瓶口,若熄灭,则已收集满 澄清石灰水 B 2H2O2
K2MnO4+MnO2+O2↑ 刚开始冒出的气体中含有空气,会使收集的气体不纯 C 将一根燃着的木条靠近集气瓶口,若熄灭,则已收集满 澄清石灰水 B 2H2O2 ![]() 2H2O+O2↑(或CaCO3+2HCl=CaCl2+H2O+CO2↑) 与氧气接触,温度要达到可燃物的着火点 磷(或P)
2H2O+O2↑(或CaCO3+2HCl=CaCl2+H2O+CO2↑) 与氧气接触,温度要达到可燃物的着火点 磷(或P)
【解析】本题主要考查常见气体的发生装置与收集装置的探究,燃烧条件的探究,根据化学方程式的计算。发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择。
一、(l)仪器① 的名称酒精灯,②的名称集气瓶。
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以应选用发生装置是A,高锰酸钾加热生成了锰酸钾和二氧化锰和氧气,反应的化学方程式是2KMnO4 ![]() K2MnO4+MnO2+O2↑;若用排水法收集氧气时不能刚有气泡就开始收集,原因是刚开始冒出的气体中含有空气,会使收集的气体不纯;
K2MnO4+MnO2+O2↑;若用排水法收集氧气时不能刚有气泡就开始收集,原因是刚开始冒出的气体中含有空气,会使收集的气体不纯;
(3)氧气、二氧化碳的密度比空气大,氧气不易溶于水,二氧化碳能溶于水,所以既能收集氧气也能收集二氧化碳气体的装置是C,检验二氧化碳气体是否收集满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明集满;二氧化碳能使澄清石灰水变浊,检验瓶中气体是否为二氧化碳可用澄清石灰水;
(4)实验室制取甲烷的反应物是固体和液体,反应条件是常温,所以实验室制取乙炔(C2H2)气体的发生装置应选用B。
二、(1)双球管中涉及两个反应,分别为过氧化氢在二氧化锰的催化下生成水和氧气,另一反应为碳酸钙和盐酸反应生成二氧化碳、氯化钙以及水,对应的化学方程式分别为2H2O2 ![]() 2H2O+O2↑、CaCO3+2HCl=CaCl2+H2O+CO2↑;
2H2O+O2↑、CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)挤压右滴管并微热燃烧管,白磷燃烧而红磷不燃烧,都有可燃物,都接触氧气,但是由于着火点不同,所以现象不同,由此可说明燃烧需要与氧气接触,温度要达到可燃物的着火点的条件;
(3)相同质量的磷、铁、镁分别在氧气中完全燃烧,设:消耗的可燃物的质量均为mg,对应的消耗的氧气的质量分别为x、y、z。
4P+5O2![]() 2P2O5
2P2O5
124 160
mg x
![]() =
=![]() x≈1.29mg
x≈1.29mg
3Fe+2O2![]() Fe3O4
Fe3O4
168 64
mg y
![]() =
=![]() y≈0.38mg
y≈0.38mg
2Mg+O2![]() 2MgO
2MgO
48 32
mg z
![]() =
=![]() z≈0.67mg
z≈0.67mg
所以消耗氧气最多的是磷(P)。


科目:初中化学 来源: 题型:
【题目】粗盐除去泥砂后含有氯化镁、硫酸钠、氯化钙等杂质,某同学对粗盐进一步提纯的实验操作过程如图所示:

(1)实验中称取5.0g粗盐,为了使粗盐充分溶解(该温度下氯化钠的溶解度为36g/100g水)量取水所用量筒的规格为__________。
A.10mL B.20mL C.50mL D.100mL
(2)步骤②所加试剂X的化学式为__________。
(3)步骤④中加入过量碳酸钠的目的是______________________________。
(4)步骤⑤过滤实验,制作过滤器的正确顺序为______________________________。
过滤后所得滤渣的化学式为______________________________。
(5)步骤⑦蒸发实验除去_________________________(填化学式)得到精盐。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小红同学取某地石灰石样品12.5g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
请计算:
(1)m的值;
(2)石灰石样品中碳酸钙的质量分数;
(3)所用稀盐酸溶质的质量分数是多少?(要求写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】烧杯中现有CaCO3和CaO的混合物若干克,往其中加入97.2g稀盐酸恰好完全反应,反应后所得溶液的质量为100g,则反应后所得溶液溶质质量分数是 ( )
A. 5% B. 5.55% C. 10% D. 11.1%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室里加热30g氯酸钾(KClO3)和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g。请计算:(1)生成氧气的质量为________。 (2)原混合物中氯酸钾和二氧化锰的质量为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类对材料的发现和使用经历了从石器、青铜器、铁器到铝的大规模使用等漫长的征程。请回答:
(1)我国是最早采用湿法冶铜的国家。文献记载“胆铜法”:用铁与“胆水”(含CuSO4)反应获得铜。铁与硫酸铜溶液反应的化学方程式为________;
(2)下列金属矿物中,可以用来炼铁的是______(填正确选项前的字母);
A. 赤铜矿(Cu2O) B.赤铁矿(Fe2O3) C.软锰矿(MnO2)
(3)生活中人们喜欢用铝制品的一个重要因素是它难生锈,铝制品难生锈原因是:______________。
(4)为比较铜和铁的金属活动性,某同学设计实验方案:将大小相同的铜块和铁块分别放入相同浓度的稀盐酸中,比较反应的剧烈程度。你认为该方案__________________(填“合理”或“不合理”),理由是_____________。
(5)我国的高铁技术世界领先.高铁钢轨采用铝和氧化铁在高温下发生置换反应实现无缝焊接,该反应的化学方程式为_____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。

(1)上述图1中,甲可表示___________的溶解度曲线;
(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的物质是___________ ;
(3)20℃时,按图2所示操作:B中的溶液是 ___________(选填“饱和”或“不饱和”)溶液。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________。工业炼铁的主要设备是___________________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙,设计实验方案如下,请参与实验并回答问题。

(1)写出A物质的化学式_____________,写出A物质的俗称_____________。
(2)写出反应②的化学方程式_________________________________________。
(3)反应①中加入过量A物质的目的是_________________________________。
反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度________ (填“有”或“没有”)影响。
(4)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果________ (填“增大”、“不变”或“减小”),其原因是_______________;你认为加入适量盐酸应依据的现象是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com