
【题目】(1)按要求用化学用语填空:
①葡萄糖的化学式为_____;
②四个碳酸根离子_____;
③标出氨气中氮元素的化合价_____;
④碘酒中的溶剂_____。
(2)用于制作航天飞船的合金材料中含有金属钼,如图是钼元素的部分信息,请回答下列问题:

①钼元素的相对原子质量为_____,x=_____。
②钼元素的原子易_____(填“得”或“失”)电子,形成离子为_____。(填化学符号)。
【答案】C6H12O6 4CO32- ![]() C2H5OH 95.94 8 失 Mo+
C2H5OH 95.94 8 失 Mo+
【解析】
(1)①葡萄糖的化学式为C6H12O6,故填:C6H12O6;
②四个碳酸根离子就是在碳酸根离子的前面加上数字4,故填:4CO32-;
③氨气中氮元素的化合价为-3,故填:![]()
碘酒中的溶剂是酒精,故填:C2H5OH
(2)①元素周期表中的一格,左上角的数是原子序数,右上角的是元素符号,中间是元素名称,最下面是相对原子质量,在原子中,质子数=核外电子数,则有:42=2+x+18+13+1,得x=8;
②钼原子的最外层电子数为1,在化学反应中失去1个电子,带一个单位正电荷,电荷数写在元素符号的右上角,数字在前符号在后,电荷数为1时不写,离子符号为:Mo+;


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:初中化学 来源: 题型:
【题目】下图表示的是甲、乙两种物质的溶解度曲线,据图所示,下列说法正确的是( )
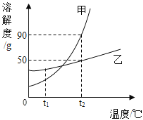
A. t2℃时,甲乙两物质饱和溶液中的溶质质量大小关系是甲>乙
B. 若甲物质中混有少量的乙物质,可以采用降温结晶的方法提纯甲物质
C. t2℃时将30g乙物质加入到50g水中,所得溶液的质量为80g
D. 将t1℃的甲、乙两物质的饱和溶液(均无固体物质剩余)升温到t2℃时,溶液中的溶质质量分数大小关系是甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业废料石膏![]() 可以“变废为宝”,用于生产氧化钙、硫酸钾、电石等。某研究性学习小组展开了如下系列研究:
可以“变废为宝”,用于生产氧化钙、硫酸钾、电石等。某研究性学习小组展开了如下系列研究:
一、高纯CaO的制备
(资料一)
Ⅰ![]() 无水硫酸铜遇水变成蓝色的硫酸铜晶体。
无水硫酸铜遇水变成蓝色的硫酸铜晶体。
Ⅱ![]() 石膏
石膏![]() 与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅲ![]() 能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
甲同学用如下装置制备CaO并验证石膏与焦炭高温反应的其他产物。
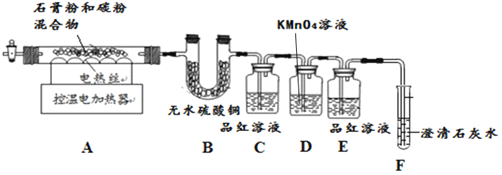
实验过程中发现:B中无水硫酸铜变蓝,说明有______生成;C中产生溶液褪色现象证明有![]() 生成;装置______中无明显变化和装置F中______现象证明有
生成;装置______中无明显变化和装置F中______现象证明有![]() 生成。写出石膏与碳粉在高温条件下反应的化学方程式:______。
生成。写出石膏与碳粉在高温条件下反应的化学方程式:______。
二、硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如下:
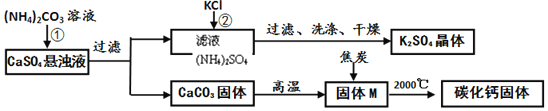
(资料二)常温下,![]() 能溶于水,温度升高,溶解度变大;
能溶于水,温度升高,溶解度变大;
氧化钙与焦炭在高温下反应生成碳化钙和一氧化碳。
![]() 反应
反应![]() 的化学方程式为______。证明固体M中不含
的化学方程式为______。证明固体M中不含![]() 的方法是______
的方法是______![]() 写出实验的方法、现象
写出实验的方法、现象![]() 。
。
![]() 反应
反应![]() 的化学方程式为
的化学方程式为![]() ,为得到纯净的硫酸钾晶体,洗涤反应
,为得到纯净的硫酸钾晶体,洗涤反应![]() 所得晶体是必不可少的步骤。但工业上不用水而用饱和
所得晶体是必不可少的步骤。但工业上不用水而用饱和![]() 溶液洗涤反应
溶液洗涤反应![]() 所得晶体,其目的是______。
所得晶体,其目的是______。
三、研究![]() 加热分解的产物
加热分解的产物
![]() 工业废料
工业废料![]() 中含有
中含有![]() ,为了测定
,为了测定![]() 和
和![]() 的质量比x:y,实验小组利用如下图所示的装置
的质量比x:y,实验小组利用如下图所示的装置![]() 夹持仪器省略
夹持仪器省略![]() 进行实验:
进行实验:
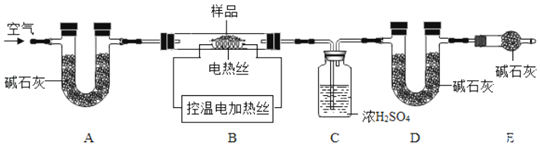
(资料三)碱石灰为固体氢氧化钠和氧化钙的混合物。可吸收水蒸气或二氧化碳。
![]() 实验前首先要______,再装入样品。装置A的作用是______。
实验前首先要______,再装入样品。装置A的作用是______。
![]() 已知
已知![]() 在
在![]() 生成
生成![]() ,
,![]() 时
时![]() 开始分解;
开始分解;![]() 在
在![]() 时分解完全。现控制B装置温度
时分解完全。现控制B装置温度![]() 进行实验并采集了如下数据:
进行实验并采集了如下数据:
![]() 反应前玻璃管与样品的质量m1g
反应前玻璃管与样品的质量m1g![]() 反应后玻璃管中固体的质量为m2g
反应后玻璃管中固体的质量为m2g
![]() 装置C实验后增重m3g
装置C实验后增重m3g![]() 装置D实验后增重m4g
装置D实验后增重m4g
某同学选用c、d数据组合求出x:y的值,若无装置E,则实验测定结果将______![]() 填“偏大”、“偏小”或“无影响”
填“偏大”、“偏小”或“无影响”![]() 。
。
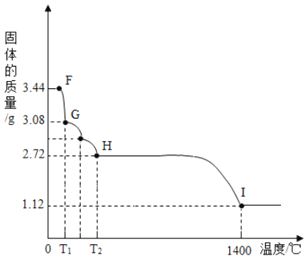
![]() 受热会逐步失去结晶水。
受热会逐步失去结晶水。
取纯净![]() 固体
固体![]() ,放在
,放在![]() 的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示。
的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示。![]() 点固体的化学式是______。请写出计算过程。
点固体的化学式是______。请写出计算过程。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定温度下,向图I烧杯中加入一定量的水,如图Ⅱ所示,所得溶液与原溶液相比,下列判断一定正确的是( )

A. 所得溶液是饱和溶液B. 溶质的质量分数变大
C. 溶质的质量增加D. 溶质的溶解度变大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,将等质量的a、b两种不含结晶水的固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后,现象如图1;然后升温到50℃时,现象如图2;a、b两种物质的溶解度曲线如图3.由这一过程可知( )
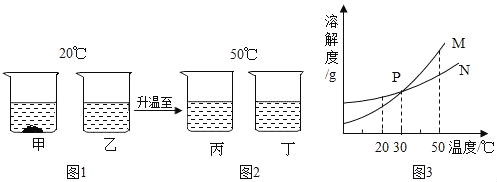
A. 30℃时a、b溶液溶质质量分数不相等
B. 40℃时a、b溶液溶质质量分数大小无法比较
C. 从20℃到50℃,b溶液质量分数不变
D. 图3中表示a的溶解度曲线是N
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有20g10%氢氧化钠溶液的烧杯中逐滴滴入7.3%的稀盐酸,下列是关于溶液总质量或溶液pH随盐酸质量变化的关系图(Q点表示恰好完全反应)。其中正确的是
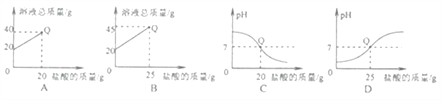
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸在工业上有着重要的用途。以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及工艺流程可简示如下:FeS2![]() SO2
SO2![]()
![]() H2SO4
H2SO4
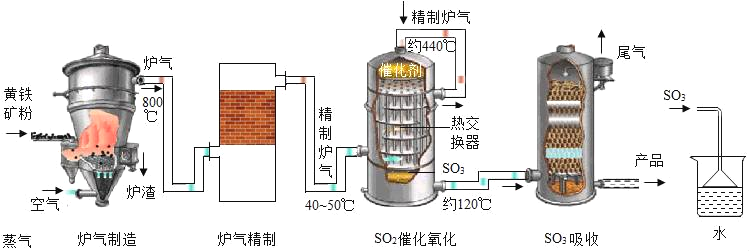
(1)工业生产过程中将矿石粉碎以及在吸收装置中液体由上而下形成喷雾状的目的是_____。
(2)在实验室模拟制硫酸时用如图装置吸收三氧化硫,除了达到与工业上相同的目的外,还可能考虑的因素是_____。
(3)工业上常用熟石灰来吸收尾气中的二氧化硫,请写出反应的化学方程式_____。(提示:生成物有一种是CaSO3)
(4)实验室中常用浓硫酸来配制稀硫酸。稀释时,正确操作是,_____,并用玻璃棒不断搅拌。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学将足量的锌粒加入到浓硫酸中,发现有大量的气泡放出,他们对气体的成分进行了探究。
(提出问题)锌粒加入浓硫酸后生成的气体是什么?
(查阅资料)①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气;
②SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色;
③SO2、CO2与氢氧化钠溶液反应原理相同,且反应前后硫元素化合价不变。
(提出猜想)甲:气体是H2;
乙:气体是:SO2;
丙:气体是_____。
(实验探究)为了验证上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去,假设每个能发生的反应都完全进行)进行探究:
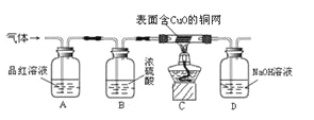
(1)实验开始后,观察到A中品红溶液褪色,证明气体中含有_____。
(2)B装置的作用利用了浓硫酸的_____性。
(3)C装置在点燃酒精灯加热之前应先通一段时间的气体,目的是_____,加热一段时间后,观察到_____的现象,证明气体中含有H2。
(4)D装置的目的是吸收尾气中的SO2,防止造成空气污染。请你写出D瓶中发生反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按要求完成下列各题:
(1)生活中蕴藏科学,留心处皆学问。请选用合适物质填空(选序号):
A. Na2CO3 B. CO2 C. NaCl D. C6H12O6 E. Ca(OH)2 F. KNO3
①联合制碱法的主要产品____;
②与水反应生成一种酸_____;
③用来提取海水中的镁_____;
④人体血糖含量的“糖”____;
⑤家庭常用的食物防腐剂____;
⑥农业上常用作复合肥 ____;
(2)请写出相应的化学符号或名称:
2个碳原子_____; +2价的锌元素_____; 2SO42-_____; 2H2_____。
(3)请你用所学知识回答下列问题:
①衣服以纯棉质地为佳。生活中鉴别纯棉与涤纶常用______方法。
②均衡膳食。下列食物中,能提供大量维生素的是_____(填字母序号)。
A、蔬菜 B、牛奶 C、大米
③严禁吸烟。香烟烟气中含有几百种对人体有害的物质,毒性作用最大的有______(写名称)、尼古丁和焦油等。
④常开窗户呼吸新鲜空气。你能闻到窗外的花香,是因为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com