
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D |
硫在氧气中燃烧
| 测定空气中氧气含量
| 铁丝在氧气中燃烧
| 排水法收集呼出的气体
|
集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察呼出气体何时收集满 |
A.AB.BC.CD.D
 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:
【题目】如图是电解水的实验装置图,填空:
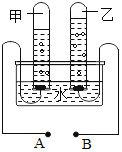
(1)A为_______极;
(2)甲管与乙管中产生的气体体积比约是_______;
(3)该实验中往往要在水中滴入氢氧化钠溶液,其目的是_______;
(4)若将质量分数为1%的NaOH溶液100g进行电解,当溶液中NaOH 的质量分数升高到2%时停止电解,则生成的H2的质量为_______g(结果保留1位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2015年11月13日,吉林石化公司双苯厂某车间因意外,发生连续爆炸,排放物对附近的河流造成了污染.
(1)分析当地最初的水样,发现主要污染物是苯和硝基苯,它们在水中能明显分层(如图),请总结出硝基苯的两条物理性质________、________.
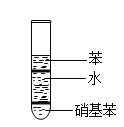
(2)专家建议,用活性炭就可以有效的除去苯和硝基苯等污染物,该过程属于________(填“物理”或“化学”)变化.
(3)若欲完全除去水中的各种杂质,需对水进行________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】维生素C(C6H8O6)主要存在于蔬菜、水果中。它能促进人体生长发育,增强人体对疾病的抵抗力。下列关于维生素c的说法正确的是
A.维生素C属于氧化物
B.一个维生素C分子由6个CO分子、4个氢分子构成
C.维生素C中碳、氢、氧三种元素的质量比为3:4:3
D.维生素C中氧元素的质量分数约为54.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是化学实验中常用的几种装置。根据图示回答下列问题:

(1)编号①的仪器名称为_____;
(2)若A装置用于实验室制取氧气,该反应的化学方程式为_____;用B收集氧气时,观察到_____时,证明氧气已经集满。
(3)若A装置用于实验室制备CO2,则仪器①中加入的药品为_____(填名称)。
(4)若A装置用于实验室制备H2,其反应的化学方程式为_____;若用C装置收集氢气,氢气应从_____;(填“a”或“b”)端通入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列反应,属于分解反应的是()
A.Fe2O3+6HCl=2FeCl3+3H2O
B.2KClO3 2KCl+3O2↑
2KCl+3O2↑
C.3CO+Fe2O3![]() 3CO2+2Fe
3CO2+2Fe
D.2CO+O2![]() 2CO2
2CO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸氢钠、碳酸钠都是人们常用的膨松剂,对膨松剂的质量,国家有明确的要求。某兴趣小组在市场上发现一种食品膨松剂,其标签如下图所示。兴趣小组对该食品级膨松剂进行了检测,称取 4.00g 样品放入试管中,加热,试管中剩余物质的质量与加热时间的关系如下表所示(忽略其它杂质)。

已知:2NaHCO3![]() Na2CO3 + H2O +CO2↑ 。
Na2CO3 + H2O +CO2↑ 。
时间/min | 0 | 0.5 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 5.0 |
剩余物质量/g | 4.00 | 3.52 | 3.03 | 2.94 | 2.85 | 2.80 | 2.76 | 2.76 |
(1)反应最后产生的剩余物是_______。
(2)通过计算,判断该膨松剂中 NaHCO3 的质量分数是否符合上图的包装说明_______?(写出计算过程)
(3)若忽略其它杂质,将反应的剩余物放入_______mL 水中,充分溶解后,可得到 15.0% 的溶液。(精确到 0.1mL)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定大理石样品中碳酸钙的质量分数,取 6g 样品置于烧杯中,向其中加入 5%的稀盐酸,恰好不再有气泡产生时(已知杂质不与稀盐酸反应)。共用去稀盐酸 73g。
①该实验中能否用稀硫酸代替稀盐酸______(填“能”或“不能”)。
②用质量分数为 36%的浓盐酸100g 能配制所需5%的稀盐酸______g。
③计算样品中碳酸钙的质量分数______。(根据化学方程式计算,精确到 0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,对社会发展与进步做出了巨大贡献。合成氨的工艺流程图如下:

(1)焦炭和水蒸气反应前需先将焦炭粉碎,目的是_____。
(2)用化学符号写出变化②中N2、H2反应生成NH3的反应式_____。
(3)工业上常采用液化、蒸发的方法将沸点不同的气体分离开来。工业合成氨中各气体的沸点如下表,变化①要从液态空气中分离得到N2和O2最适宜的温度范围是_____(填序号),变化①属于_____变化(填“化学”或“物理”)。
物质 | H2 | N2 | O2 | NH3 |
沸点/℃ | -252 | -195.8 | -183 | -33.35 |
A -183.5℃≥T≥-195℃
B -182℃≥T≥-195℃
C T>-195.8℃
(4)实际生产中,N2和H2不可能全部转化为NH3,上述工艺流程中能循环利用的物质是_____(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com