
| A. | 反应前后化学性质不发生改变 | B. | 反应前后质量发生了改变 | ||
| C. | 能改变某些化学反应的速率 | D. | 某些催化剂可催化不同的反应 |
分析 催化剂是指能改变其它物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有改变的物质;
解答 解:A、催化剂本身的质量和化学性质在化学反应前后都没有改变的物质,正确但不符合题意,故选项错误;
B、催化剂本身的质量和化学性质在化学反应前后都没有改变的物质,反应前后质量发生了改变错误,错误符合题意,故选项正确;
C、催化剂是指能改变其它物质的化学反应速率,因此能改变某些化学反应的速率正确,正确但不符合题意,故选项错误;
D、某些催化剂可催化不同的反应正确,如二氧化锰可以做过氧化氢的催化剂,也可以做氯酸钾的催化剂,正确但不符合题意,故选项错误;
故选B
点评 本考点考查了催化剂的特点和催化作用,基础性强,要加强记忆,理解应用,本考点主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:填空题
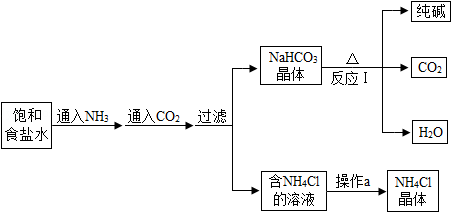
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生活中常见的有机物有甲烷、乙醇、乙酸、葡萄糖、蛋白质、苏打等 | |
| B. | 家用电器着火可用干粉灭火器扑灭 | |
| C. | 对人体有害的物质有甲醛、黄曲霉素、重金属、亚硝酸钠等 | |
| D. | 造成温室效应的气体主要就是CO2,还有氟氯烃(CFC〕、甲烷、低空臭氧、和氮氧化物气体等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
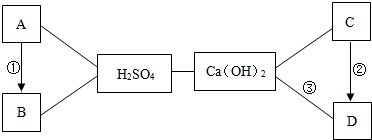
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
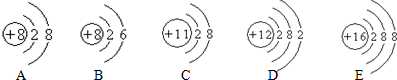
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
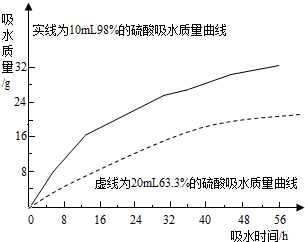 硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:| 方案 | 实验假设 | 实验方案 | 实验现象与结论 |
| Ⅰ | 能发生钝化 | 取一铁片先插入浓硫酸中,一段时间后取出,再插入硫酸铜溶液中. | 无明显变化,假设成立. |
| Ⅱ | 能发生钝化 | 取两片相同的铁片,一片放入浓硫酸中,一段时间后取出,与另一片同时放入硫酸铜溶液中. | 浸过浓硫酸的铁片表面无明显变化,另一铁片表面产生红色固体,假设成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
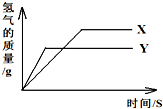 将等质量的锌粉和铁粉分别加入相同质量分数的足量稀盐酸中,反应生成氢气的质量与反应时间的关系如图所示,回答下列问题:
将等质量的锌粉和铁粉分别加入相同质量分数的足量稀盐酸中,反应生成氢气的质量与反应时间的关系如图所示,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com