
| A. | 所有的物质都是由分子构成的 | |
| B. | 气态和液态物质的分子是运动的,固态物质的分子是静止的 | |
| C. | 酸碱中和反应的本质是氢离子和氢氧根离子结合成水分子的过程 | |
| D. | 原子的实际质量很小,等于其含有的质子质量总和 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 火灾发生后应用湿毛巾捂住口鼻迅速逃离,并拨打119 | |
| B. | 油库、面粉加工厂、纺织厂等场所要严禁烟火 | |
| C. | 只要温度到达着火点,可燃物一定会燃烧 | |
| D. | 扑灭森立大火,可将大火蔓延路线前的一片树木砍掉,形成隔离带 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
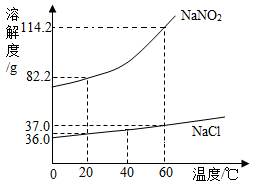 亚硝酸钠(NaNO2)有毒、有咸味.外形与食盐相似.人若误食会引起中毒.NaNO2、NaCl的溶解度曲线如图所示.
亚硝酸钠(NaNO2)有毒、有咸味.外形与食盐相似.人若误食会引起中毒.NaNO2、NaCl的溶解度曲线如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
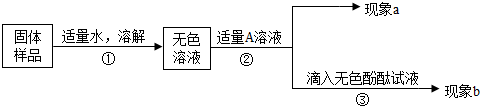
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
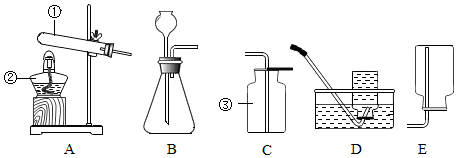
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com