
【题目】某同学为探究生石灰暴露空气中的变质情况,设计如下实验:称取生石灰w,露置空气一段时间后,所得粉末A的质量为1.2w,加入足量稀盐酸,生成气体B,依次通入浓硫酸,足量澄清石灰水,得到沉淀0.25w。推断粉末A的组成________(写清楚成分及其对应质量),计算粉末A 中氧化钙的质量分数________。
【答案】CaO 0.58w 、Ca(OH)2,0.37w、 CaCO3,0.25w 48.3%
【解析】
加入足量稀盐酸,生成气体B,依次通入浓硫酸,足量澄清石灰水,得到沉淀0.25w,0.25w就是二氧化碳与氢氧化钙反应生成碳酸钙的质量;二氧化碳又是粉末A中的碳酸钙与稀盐酸反应得到,依据:CaCO3→CO2→CaCO3得,粉末A中的碳酸钙的质量就是0.25w;
设生成0.25w的碳酸钙需要二氧化碳的质量是x
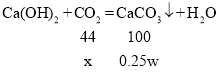
![]()
x=0.11w
生石灰的质量是w,露置空气一段时间后,所得粉末A的质量为1.2w,固体增重的质量=1.2w-w=0.2w;也就是增加了0.11w的二氧化碳,剩余的0.2w-0.11w=0.09w,就是生石灰吸收的水的质量;
设与0.09w的水反应生成的氢氧化钙的质量是y
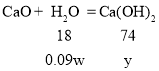
![]()
y=0.37w
则粉末A的中CaO的质量=1.2w-0.37w-0.25w=0.58w
粉末A的组成是:CaO 0.58w 、Ca(OH)2 0.37w、 CaCO3 0.25w
故填:CaO 0.58w 、Ca(OH)2 0.37w、 CaCO3 0.25w。
粉末A 中氧化钙的质量分数=![]()
故填:48.3%。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:初中化学 来源: 题型:
【题目】某化学活动兴趣小组用如图1装置进行木炭还原氧化铜的探究实验,反应一段时间后,,甲中试管内黑色粉末全部变成红色,乙中澄清石灰水变浑浊。
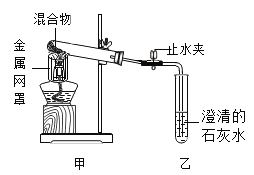
(1)写出木炭还原氧化铜的化学方程式_____________。
(2)待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若罩不关闭止水夹,可能出现的问题是___________。
[查阅资料]木炭还原氧化铜在反应过程中,有可能生成氧化亚铜(Cu2O),氧化亚铜为红色固体。
[探究一]同学们对反应后玻璃管中的红色粉末是否含有氧化亚铜展开探究,已知氧化亚铜能与稀硫酸反应:![]() 。取少量红色固体于试管中,加入过量的稀硫酸,观察到______________,说明红色粉末中含有Cu2O。
。取少量红色固体于试管中,加入过量的稀硫酸,观察到______________,说明红色粉末中含有Cu2O。
[探究二]有同学提出,木炭还原氧化铜的过程中,除了会生成氧化亚铜,还有可能生成一氧化碳,他的依据是___________。于是他重复实验并收集反应生成的气体,将气体干燥后,再通过灼热的氧化铜,观察到有___________,色固体生成,说明有CO生成。
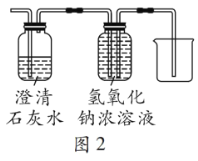
[反思与评价]根据以上探究,有同学认为原实验装置存在不足,于是将乙装置改进为如图2所示,改进后装置的优点是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质世界中的“八国家”举行集团首脑会议。“八国家”的首脑A~H分别是盐酸、硫酸、氧气、铁、一氧化碳、氧化铜、硝酸银溶液、碳酸钙中的一种。会谈的位置安排要求相邻的代表之间能发生化学反应(所涉及反应均为初中常见化学反应),如图所示。其中A、B是单质,B是气体,G是胃液的主要成分。请回答下列问题:
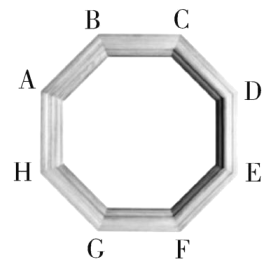
(1)D的化学式是________________。
(2)F物质的用途为__________。
(3)A与H反应的化学方程式为_____________。
(4)八种物质中相邻物质之间的反应一定没有涉及的基本反应类型是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
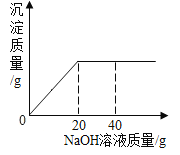
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器中有A、B、C、D 四种物质,在一定条件下反应,各物质组成见下表 1。下列说法正确的是()
| A | B | C | D |
反应前 | 70% | 14% | 6% | 10% |
反应x分钟 | a | 11% | c | d |
反应y分钟 | 42% | b | 40% | 10% |
表1容器各组分物质质量分数随反应时间的变化情况
A.图 中 a=56%
B.该反应为化合反应,且一定存在元素化合价的升降
C.D是催化剂
D.若反应可以进行彻底则B有剩余
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是地球表面覆盖最多的物质,也是生命活动不可缺少的物质。城镇自来水厂生产流程可用下图表示:
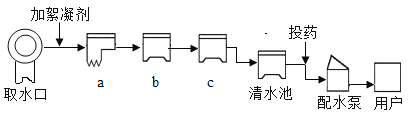
资料:常用的絮凝剂有明矾[KAl(SO4)2·12H20],消毒剂有液氯(Cl2)。
回答下列问题:
(1)流程图中c处为_____(填“沉淀池”或“过滤池”或“吸附池”)。
(2)明矾作絮凝剂是因为与水反应生成氢氧化铝,氢氧化铝的化学式为_____。
(3)要鉴别自来水是硬水还是软水,可向自来水样品中加入适量的_____,搅拌,如果观察到_____,则样品为软水。
(4)净水流程中的有些步骤如“加絮凝剂”“投药”,会人为地向水中加入一些化学物质,针对这一环节,请你向自来水公司提出一条建议_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“食尽人间五味,方知人生百态”。
(1)“甜味”——蔗糖的化学式是C12H22O11,其中碳元素和氧元素的质量比为_________;
(2)“咸味”——烹调时常添加氯化钠来使食物具有咸味。工业上常用电解该物质的饱和溶液制取烧碱,同时生成另外两种气体。请写出该反应化学方程式____________。
(3)“酸味”——吃饭时会加点醋来提味。醋的主要成分是__________(写出化学式)。蒸馒头时常因小苏打过量而导致馒头发黄发苦,有经验的老人会在蒸馒头前向面团中滴加几滴白醋来调节馒头中碳酸钠的涩味,请写出醋酸与碳酸钠反应的化学方程式__________。
(4)“穿衣吃饭”,我们的衣物主要是由纤维织成。棉麻是种植物纤维,它的主要成分是_________,属于糖类。
(5)以下营养物质不能提供人体所需能量的是__________。
A蛋白质 B油脂 C糖类 D维生素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】四种物质在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示,则有关说法中不正确的是
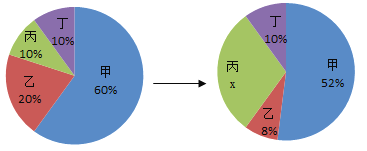
A.X的数值是30%
B.丙一定属于化合物
C.参加反应的甲和乙的质量比为13:2
D.丁可能不参与反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是部分元素的离子结构示意图和元素周期表的一部分。请回答:
| ||||||
| ||||||
|
| |||||
(1)图①、②中属于阴离子的是______(填序号),该元素的质子数为______;13号元素原子的最外层电子数为______。

(2)由表中原子序数为1、8、13的元素组成物质的化学式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com