
����Ŀ����ͼ��ij�о���ѧϰС����Ƶļ���װ�ã�����������ش��������⣺
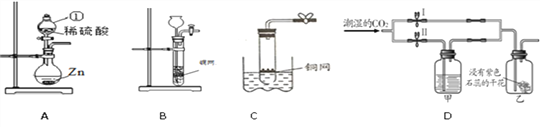
(1)ͼA������������Ϊ________��������Ӧ�Ļ�ѧ����ʽΪ______________��
(2)��Ũ����(������������Ϊ98%���ܶ�Ϊ1.84 g/mL)��ˮ���������Ϊ1�U10���Ƹ�ʵ�������ϡ���ᣬ����ϡ�����������������ԼΪ________(������0.1%)������ϡ����������²�������Һ��pH��ѧ�仯�����ߵ���______(����ĸ���)��
a��������ˮ b������������ c��������Ũ����
(3)װ��B��ʵ���ҳ��������巢��װ�á�ԴԴͬѧ��װ��B�õ�����������һ֧�ײ���һ��С�����ԹܺͿ�Ȫˮƿ��ϳ�װ��C(�г���������ȥ)��������ȡ������̼����C��B��ȶ����е��ŵ���__________����װ��B��C��ȡ������̼�Ļ�ѧ��Ӧ����ʽΪ___________��
(4)��װ��D̽��CO2�IJ������ʣ����رբ�����ɫС��(��ʯ����ҺȾ��)��죻���رբ�����ɫС������죬���ƿ����ʢ���Լ�������______(�����)��
��ŨH2SO4 ��ŨNaOH��Һ �۱���NaCl��Һ
���𰸡� ��Һ©�� Zn+H2SO4==ZnSO4+H2�� 15.2% b ���Կ��Ʒ�Ӧ�Ŀ�ʼ�ͽ��� CaCO3+2HCl==CaCl2+H2O+CO2�� �٢�
��������
��1��ͼA���������Ƿ�Һ©����п�����ᷴӦ��������п����������ѧ����ʽΪ��Zn+H2SO4==ZnSO4+H2����
��2����Ũ����(������������Ϊ98%���ܶ�Ϊ1.84 g/mL)��ˮ���������Ϊ1�U10���Ƹ�ʵ�������ϡ���ᣬ����ϡ�����������������ԼΪ![]() ��100%=15.2%����Ϊ��ͬ�¶��£��������������Խ����Һ������Խǿ����Һ��pHԽС����ϡ�����м��������ˮʱ�����������������С����Һ��pH���û�з�����ѧ�仯����ϡ�����м�������ʱ���������ᷴӦ�����������������С�����Լ�������Һ��pH��������Ũ���ᣬ������������������Һ��pHԽС�����ԣ���Һ��pH��ѧ�仯�����ߵ���b��
��100%=15.2%����Ϊ��ͬ�¶��£��������������Խ����Һ������Խǿ����Һ��pHԽС����ϡ�����м��������ˮʱ�����������������С����Һ��pH���û�з�����ѧ�仯����ϡ�����м�������ʱ���������ᷴӦ�����������������С�����Լ�������Һ��pH��������Ũ���ᣬ������������������Һ��pHԽС�����ԣ���Һ��pH��ѧ�仯�����ߵ���b��
��3��C��B��ȶ����е��ŵ��ǿ��Կ��Ʒ�Ӧ�Ŀ�ʼ�ͽ������ر�ֹˮ�оͿɿ��ƣ���ȡ������̼��̼��������ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼����ѧ��Ӧ����ʽΪCaCO3+2HCl=CaCl2+H2O+CO2����
��4�����رբ����ó�ʪ�Ķ�����̼���徭����ƿ��ͨ����ƿ��������ɫС������죬���رբ���ͨ���������壬������ɫС����죬��ͨ������̼����Ũ���ᱻ�������Ķ�����̼���岻��ʹ������ɫС������죬��ȷ���ڶ�����̼ͨ��ŨNaOH��Һ�����գ����徭����ƿ���ں��ж�����̼��ͨ����ƿ��������ɫС������죬��ȷ����ͨ��ŨNaCl��Һ��ʪ�Ķ�����̼�����ܹ�����̼�ᣬ̼��ʹ����ɫС����죬������٢ڡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���廪��ѧ�о���Ա�ɹ����Ƴ�һ��������ά����,�ɽ�������̼ת����Һ��ȼ�ϼ״�,����ʾ��ͼ��ͼ(ͼ�е���ǡ����ȫ��Ӧ).����˵����ȷ����()

A. ���Ļ�ѧʽΪH2O���÷�ӦΪ�û���Ӧ B. �μӷ�Ӧ�ļ����ҵ�������Ϊ3:1
C. ���ǵ��ʣ��ҡ�����Ϊ������ D. �÷�Ӧǰ����Ӻ�ԭ�ӵ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D��ƿʧȥ��ǩ����ɫҺ�壬���Ƿֱ���ϡ���ᡢ̼������Һ���Ȼ�����Һ������������Һ�е�һ�֡�Ϊ�˼������ǣ���ȡ������Һ������ϣ�ʵ���������ʾ�����С���ʾ�г������ɣ�����ʾ���������ɣ�����ʾ���������������±����ƶϳ�A��B��C��D�ֱ���ʲô���ʣ��ش����⡣
A | B | C | D | |
A | \ | �� | �� | �� |
B | �� | \ | �� | �� |
C | �� | �� | \ | �� |
D | �� | �� | �� | \ |
��1��B����Һ�У����ڵ�������_______��������ţ�A��B�ܷ�����Ӧ��ԭ����_________��
��2��д��D��һ����;_________��D��C��Ӧ����ʵ����__________����һ�ַ���������D��C���Է�����Ӧ________��
��3��д��D��B��Ӧ�Ļ�ѧ����ʽ__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧΪ�˲ⶨһƿ����������Һ�����ʵ�����������ȡ����Һ68.0g�������������2.0g������ȫ��Ӧ�����������ݳ�ʱ���Ƶõ�ʣ�����ʵ�������Ϊ68.4g������:
��1����Ӧ��ȫ�����������������__________g��
��2���ù���������Һ�����ʵ�����������д��������̣�___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ѧϰ��ѧ����Ҫ���ߡ�
(1)�û�ѧ���ű�ʾ��
��2����ԭ��__________�� ��3�������������________�������������Ԫ�صĻ��ϼ�________�� ��þ����__________��
(2)����ĸ�����գ�a������̿ b����ʯ�� c���ɱ� d��������
�ٿ������˹��������_______�� �ڿ�ֱ�ӽ���ѪҺ������������___���ۿ�����������ɫ�ص����ʵ���_______���ܿ���ʳƷ���������___________��
(3)д�����з�Ӧ�Ļ�ѧ����ʽ��
�ٺ����ڿ�����ȼ��_________�� ���Ȼ�����Һ����������Һ��Ӧ_________����������ϡ�����ȥ������������⼣��__________���ܵ�ⱥ��ʳ��ˮ���ռͬʱ��������������(Cl2)_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl2��Һ�л���������CuCl2,Ϊ�˳�ȥCuCl2,ij����С��ͬѧȡ����Һ50g���ձ��У�Ȼ�������5�μ���ij����M��ַ�Ӧ�������������±�����������֪ʶ�����ݻش���������:
���� | 1 | 2 | 3 | 4 | 5 |
����M������(g) | 0.28g | 0.28g | 0.28g | 0.28g | 0.28g |
��Һ��������(g) | 49.96 g | 49.92 g | 49.88g | 49.84g | 49.84g |
(1)д������M�Ļ�ѧʽ______.
(2)�μӷ�ӦM����������________?
(3)FeCl2��Һ��CuC12������������_______?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2017��12��18�գ���ͨ������ʽ��������־����ͨ���롰����ʱ������
��1�������г��������ʹ�õ�þ���Ͻ�����_____����������ϡ��ϳɲ��ϡ�����þ���Ͻ���ŵ���_____��
��2�����������������Ҫʹ�ô����ĸ�������ҵ����������һ����̼����������Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ��_____��
��3��������Ϣ����ϵͳ��ʹ�õĹ��ά�͵���оƬ�Ĺؼ����Ϸֱ�Ϊ�������裨SiO2���;���裨Si��������������ת��Ϊ��Ĺ�������_____��������仯����ѧ�仯������
��4������ʩ�������в����ķ�ˮ���Ͻ��Լ���е©�͵ȣ������ˮ�������Ⱦ��ʹ�û���̿�ɶ���ˮ���д��������������˻���̿��_____�ԡ�
��5��Ϊȷ��������ȫ�������������밲װ�Զ�����ϵͳ�������ˮ������ԭ����_____��
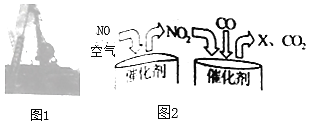
��6������ʩ�����̳���β���к�NO��CO��β��������ͼ2��ʾ��ת����ʵ�ִ���ŷš�д������X�Ļ�ѧʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����立��ϻ�����������ʯ�Һ������ɵ�NH3ȫ���ݳ���������ʧ�˲��ֵ�(��ʯ����������ȫ) ��ȡ������Ϊ10�˵ĸ÷������ݽ���ʵ�飺
�ٽ�һ�ݸ����ȥˮ�ֺ�������Ϊ9.9�ˣ�
�ڽ���һ����������ʯ�һ�ϼ��ȣ���ַ�Ӧ����������������ȫ��ͨ��װ��������ʯ�ҵĸ���ܣ���ַ�Ӧ��ø���ܺ������ʵ���������ͨ������ǰ������1.18�ˡ�
��ʾ��1. (NH4)2SO4+CaO![]() CaSO4+H2O+2NH3��(���������ʣ������뷴Ӧ)
CaSO4+H2O+2NH3��(���������ʣ������뷴Ӧ)
2.��ʯ�Ҳ��백����Ӧ�������������ĸ����
(1)ʵ��ڲ�����ˮ������Ϊ________��
(2)��������е�Ԫ�ص���������(д���������)____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�С�������ʾ����������֮����Է�����Ӧ����������ʾһ�����ʿ���ת������һ�����ʣ����и������ʰ��ס��ҡ�����˳����ͼʾҪ����ǣ�������
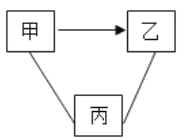
A. C��CO��O2 B. Mg��MgCl2��ZnSO4
C. Ca��OH��2��CaCl2��Na2CO3 D. BaCl2��BaCO3��H2SO4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com