
【题目】氯化钙钾石的化学式为KClxCaCl2(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl和CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解,得到KCl和CaCl2的混合溶液.向该溶液中逐滴加入Na2CO3溶液,发生反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.请回答下列问题:

(1)图中AB段表示的意义是_________.
(2)①样品中CaCl2的质量是多少? ②所用Na2CO3溶液中溶质的质量分数是多少?
(3)①样品中钾元素的质量分数是多少?(精确到0.1%)②氯化钙钾石化学式中的x值是多少?
【要求:(2)、(3)两问写出计算过程】
【答案】(1)CaCl2已完全反应,且Na2CO3溶液过量;(2)①11.1g;② 10%;(3)①21.0%;② 1。
【解析】
试题分析:(1)AB段沉淀碳酸钙的质量没有改变,表示溶液中氯化钙已完全反应,继续加入的碳酸钠溶液过量;(2)设恰好完全反应生成10g碳酸钙沉淀时消耗氯化钙的质量为x,消耗的碳酸钠的质量为y,
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111 100
y x 10g
![]() ,解得:x=11.1g;y=10.6g。故所用Na2CO3溶液中溶质的质量分数是
,解得:x=11.1g;y=10.6g。故所用Na2CO3溶液中溶质的质量分数是![]() ×100%=10%;(3)①样品中氯化钾的质量=18.55g﹣11.1g=7.45g,钾元素的质量为:7.45g×
×100%=10%;(3)①样品中氯化钾的质量=18.55g﹣11.1g=7.45g,钾元素的质量为:7.45g×![]() ×100%=3.9g,样品中钾元素的质量分数是
×100%=3.9g,样品中钾元素的质量分数是![]() × 100%=21.0%;
× 100%=21.0%;
②KClxCaCl2﹣﹣﹣K
74.5+111x 39
18.55g 3.9g
![]() ,
,
解得:x=1。


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:初中化学 来源: 题型:
【题目】图1是某兴趣小组在学习碱的性质时进行的探究活动,请要求回答问题。

(1)通过分析实验一可知,氢氧化钠会吸收空气中的________.
(2)实验二中观察到3个塑料瓶变瘪的程度为A>B>C,可证明CO2能与NaOH、Ca(OH)2反应,其中C瓶在实验中起 _________作用。
(3)晓晓查阅资料了解到往Ba(OH)2溶液中滴加或通入下列图2中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀.
①写出D试管中反应的化学方程式 _________.
②不同的碱溶液中都含有OH﹣,所以,碱有一些相似的化学性质.上述关于Ba(OH)2性质的实验不能体现碱的相似性质的是 _________(填字母序号)
(4)冬冬发现工业上使用的氢氧化钠固体标签如图3所示,于是对其所含杂质进行了探究.
【提出问题】 _________
【提出猜想】
猜想I:查阅资料可知,工业用氢氧化钠可能含有NaCl.
猜想Ⅱ:工业用氢氧化钠可能含有Na2CO3,原因是 _________(用简洁的文字表述).
【进行实验】
实验步骤 | 实验现象 | 解释或结论 |
①取适量固体样品于试管中,加水溶解 | 固体全部溶解 | / |
②向①所得溶液中滴加过量的 _________ | 一开始无明显变化,一会儿后产生能使澄清石灰水变浑浊的气体 | 样品中含有Na2C03 |
③向②所得溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有NaCl.反应的化学方程式为 _________ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室制备物质的常用装置,根据装置回答:
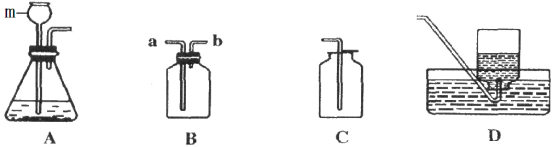
(1)图中仪器m的名称为 ,请写出用装置A制取一种气体的化学方程式为 ,该反应的基本反应类型为 .
(2)装置C可用于收集的常见气体是(写出一种即可) .
(3)若用装置B除去二氧化碳中少量的水蒸气,可在装置中装入 ,气体应从 端进入.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究.
【査阅资料】
①NaN3受撞击会生成Na、N2
②NaN3遇盐酸、H2SO4溶液无气体生成
③碱石灰是CaO和NaOH的混合物
④NaN3的制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和NH3
【问题探究】
(1)汽车受撞击后,30毫秒内引发NaN3迅速分解,该反应的化学方程式为___________;
(2)工业级NaN3中常含有少量的Na2CO3,其原因是___________(用化学方程式表示);
(3)为测定某工业级NaN3样品中Na2CO3的质量分数,小组同学设计了如图实验装罝:

①小明同学认为通过测定装置I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的质量分数,小组同学通过讨论认为不可行,其理由可能是___________(答出一种即可)
②小明同学在大家讨论的基础上,又设计了装罝Ⅱ,请分析:装置Ⅱ中A的作用是___________.若无装置C,对测定结果造成的影响是 (填“偏大”、“偏小”或“无影响”).装置E的作用是___________.
③根据装置Ⅱ,小组同学设计的实验步骤有:
a.称量装置D
b.称量样品,检査装置气密性
c.打开弹簧夹,鼓入空气
d.关闭弹簧夹,打开分液漏斗的活塞和玻璃塞,注入足量的稀琉酸,关闭活塞和玻璃塞.
其正确的顺序为___________(填字母序号,可重复)
④计算碳酸钠的质量分数时,至少需要测定___________个数据.(填数字)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线图,请回答下列问题:
 。
。
(1)20℃时,将15g的甲物质充分溶解在50g水中,所形成溶液的溶质质量分数是 .
(2)10℃时,欲将150g乙物质的饱和溶液质量分数减小一半,需要加水 g.
(3)某同学欲将20℃时300g20%的甲溶液溶质质量分数增大一倍.他采用恒温蒸发水的方法,并进行了如下计算:
解:设蒸发水的质量为x,
300g×20%=x×40%解得:x=150g。试分析:他能否达到目的,并说明理由。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:

(1)写出对应化学符号:① 镁离子 ;② 三个五氧化二磷分子 ;
(2)请从上面右图中写一条关于硅元素的信息: ___________________________________
(3)研究表明:第二周期从3~9号元素的原子电子层数相同,随着核电荷数逐渐增大,原子核对核外电子的引力逐渐增大,故原子半径逐渐减小。请分析第三周期从11~17号元素原子半径变化规律是______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b两种固体物质的溶解度曲线如图所示,下列说法中不正确的是( )

A.t1℃时,a、b物质的溶解度相等
B.a物质的溶解度随温度的升高而增大,b物质的溶解度随温度的升高而减小
C.t2℃时,将a、b两物质的饱和溶液分别降温至t1℃,所得的溶液溶质质量分数相等
D.提纯a中混有少量的b,可采用降温结晶的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从海水中可以提取镁,其中的一个步骤是将卤水(含MgCl2、NaCl、KC1的混合液)转化为氯化镁晶体.实验室中模拟该转化的过程如下,回答有关问题.
(1)制备氢氧化镁:向卤水中加入适量生石灰,充分反应后过滤.
①该过程中发生了多个反应,其中会大量放热的反应是(填化学方程式)
②过滤操作需用到的玻璃仪器除烧杯外,还有 .
(2)制备氯化镁溶液:用盐酸溶解Mg(OH)2.为了便于后续操作,盐酸不宜过量.
①反应的化学方程式是 .
②通过计算,可准确知道所需盐酸的量.理论上溶解11.6gMg(OH)2需要36.5%HCl溶液 g
③由于准确称量Mg(OH)2的步骤繁琐,实验中并不常用,而是通过一定操作方法来达到到控制盐酸用量的目的.操作是:将Mg(OH)2加入烧杯中,逐渐缓慢加入一定量的盐酸,并用玻璃棒搅拌, .
(3)制备氯化镁晶体:蒸发浓缩MgCl2溶液,冷却结晶.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com