
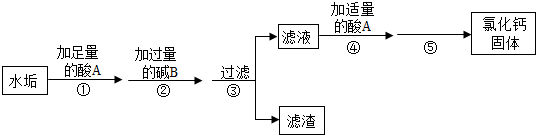
分析 (1)根据人体胃酸的主要成分是盐酸,所以酸A是盐酸进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,氢氧化钙溶液和氯化镁反应生成氢氧化镁白色沉淀和氯化钙进行分析;
(3)根据需要制取的是氯化钙和加入的过量碱B进行分析;
(4)根据滤液中加入酸A后的溶液成分进行分析.
解答 解:(1)人体胃酸的主要成分是盐酸,所以酸A是盐酸,化学式为:HCl;
(2)碳酸钙和盐酸反应会生成氯化钙、水和二氧化碳,氢氧化镁和盐酸反应生成氯化镁和水,最后需要制取氯化钙,所以需要将氯化镁沉淀,依据除杂原则可知,B是氢氧化钙,所以步骤①中生成气体的化学反应方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;步骤②中生成沉淀的反应是氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,化学方程式为:MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;
(3)前面加入的是过量的氢氧化钙,而最后要得到氯化钙,需要将氢氧化钙除去,所以步骤④加酸A的作用是将反应剩余的氢氧化钙除去;
(4)滤液中加入盐酸反应后是盐酸和氯化钙的混合物,所以要从溶液中得到氯化钙,需要用蒸发结晶的方法.
故答案为:(1)HCl;
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;
(3)将反应剩余的氢氧化钙除去;
(4)蒸发结晶.
点评 本题难度不是很大,主要考查了酸的有关的化学性质及有关的化学方程式的书写,培养学生抓住规律、应用规律解决问题的能力.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:初中化学 来源: 题型:多选题
| A. | K2CO3 HCl NaOH BaCl2 | |
| B. | CuSO4 NaOH BaCl2 HCl | |
| C. | NaCl HCl H2SO4 AgNO3 | |
| D. | NaOH KOH MgCl2 H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 小明欲测定一瓶标签破损的NaOH溶液的溶质质量分数.现取10g NaOH溶液样品,将5%的系硫酸溶液逐滴加到样品中,边加边搅拌,随着稀硫酸的不断加入,溶液pH的变化如图所示.试回答:
小明欲测定一瓶标签破损的NaOH溶液的溶质质量分数.现取10g NaOH溶液样品,将5%的系硫酸溶液逐滴加到样品中,边加边搅拌,随着稀硫酸的不断加入,溶液pH的变化如图所示.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 |
| KCl的溶解度/g | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 |
| KNO3的溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 清洁剂 | 彩漂液 | 漂白水 |
| 功 能 | 漂洗衣物,使色彩鲜艳 | 漂除衣物污渍 |
| 有效成分 | H2O2 | NaClO |
 猜想“洁厕灵”的成分中可能含有酸.
猜想“洁厕灵”的成分中可能含有酸.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ①④②③⑤⑥ | C. | ①④③②⑤⑥ | D. | ①③②④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com