
【题目】为得到高纯度碳酸钙,实验室用Na2CO3溶液与CaCl2溶液反应制取。现将150gCaCl2溶液分四次加入盛有100gNa2CO3溶液的烧杯中,充分反应,四次测量所得数据见下表:
次数 | 第一次 | 第二次 | 第三次 | 第四次 |
累计加入CaCl2溶液的质量/g | 40 | 80 | 120 | 150 |
烧杯中溶液的总质量/g | 134 | 168 | 202 | 232 |
(1)第___________次恰好完全反应,此时生成沉淀的总质量为___________g。
(2)第四次测量时,所得溶液中的溶质有___________(填化学式)。
(3)CaCl2溶液的溶质的质量分数为___________。(写出计算过程)
【答案】三 18 NaCl、Ca2Cl 16.65%
【解析】
根据第一次烧杯中溶液总质量减少100g+40g-134g=6g,第二次烧杯中溶液总质量减少100g+80g-168g=12g,第三次烧杯中溶液总质量减少100g+120g-202g=18g,第四次烧杯中溶液总质量减少100g+150g-232g=18g,分析可知即第三次恰好完全反应,则第四次加入氯化钙溶液过量;根据前三次都可以计算出氯化钙溶液的溶质的质量分数。
(1)根据四次实验总质量的减少量知,第三次恰好完全反应,此时生成沉淀的质量为:100g+120g-202g=18g,故填:三,18。
(2)第四次测量时,氯化钙溶液过量,可知溶液中有Na2CO3溶液与CaCl2溶液反应生成的NaCl,以及加入过量的CaCl2溶液,因此含有的溶质为NaCl和CaCl2,故填:NaCl、CaCl2。
(3)由表可知第一次加入40g氯化钙溶液,生成碳酸钙沉淀的质量为100g+40g-134g=6g。设40g氯化钙溶液中溶质的质量为x;
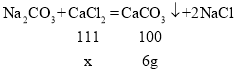
![]()
x=6.66g
则氯化钙溶液的溶质的质量分数为:![]()
答:氯化钙溶液的溶质质量分数为16.65%。


科目:初中化学 来源: 题型:
【题目】选择下列部分实验操作可完成两个实验,甲实验为除去粗盐中难溶性的杂质,乙实验为配制溶质质量分数为10%的NaCl溶液。下列说法正确的是 。
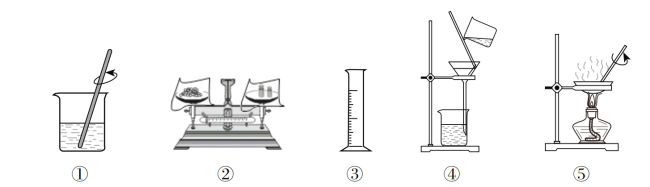
A.操作①和⑤中玻璃棒的作用是相同的
B.甲实验和乙实验都要进行实验操作①
C.甲实验在操作⑤时,将水全部蒸发完后停止加热
D.乙实验在操作③时,若俯视读数,会使所配制溶液的浓度偏小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图,表示某些物质间的转化关系(反应条件均略去)。其中A为天然气的主要成分,C为相对分子质量最小的氧化物,F为红棕色粉末,G为最常见的金属。B、D、E均为无色气体。请回答:
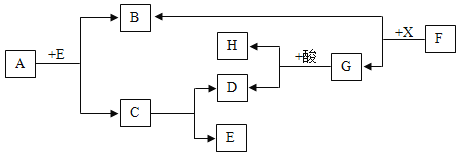
(1) X是____________或____________(填化学式)。
(2)B固态物质在实际生活中的一种用途是_________________________。
(3)写出下列反应的化学方程式:
①A+E→B+C __________________________。
②C→D+E __________________________。
③G与E的反应 __________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是三种常见固体物质的溶解度曲线,下列说法正确的是()
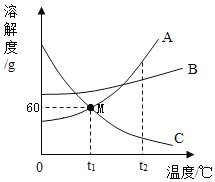
A.t1℃时,A和C的饱和溶液中含有相同质量的溶质
B.欲除去A溶液中少量的B物质,常采用蒸发结晶的方法
C.t1℃时,将80gA的饱和溶液稀释为质量分数为20%的溶液,需要加水的质量为70g
D.t2℃时,将A、B、C的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为:B>A=C
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,甲、乙、丙的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),则下列各组物质按照甲、乙、丙的顺序,不符合要求的是___________。
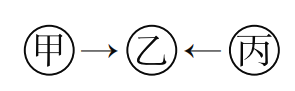
A.C、CO、CO2
B.H2O2、H2O、O2
C.KOH、K2CO3、KNO3
D.Fe2O3、FeCl3、Fe(OH)3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】许多制药厂、化工厂在生产中会产生大量的铁泥(主要含Fe,FeO,Fe2O3等物质),若以铁泥为原料制备FeSO4·7H2O,可实现废物利用。其主要流程如下。

已知:FeO + H2SO4 === FeSO4+H2O;Fe + Fe2(SO4)3 === 3FeSO4
(1)酸浸过程中铁发生反应的化学方程式为______。
(2)还原过程中,元素化合价发生改变的是______。
(3)产品在结晶前需要调节pH。若pH过高需要加入——______进行调节。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据下图所示装置回答问题。

(1)实验室用高锰酸钾制取氧气时,反应的化学方程式为_____。
(2)实验室用大理石和稀盐酸制取二氧化碳时,选用的收集装置是_____,检验二氧化碳是否已收 集满的方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
土豆是继水稻、小麦、玉米之后的第四大粮食作物,含淀粉、蛋白质、维生素C等多种营养物质,是餐桌上的美味食材。

表1鲜土豆中主要营养物质的含量(每100g)
蛋白质/g | 脂肪/g | 淀粉/g | 钙/mg | 磷/mg | 维生素C/mg |
1.5~2.3 | 0.4~0.94 | 17.5~28.0 | 11~60 | 15~68 | 20~40 |
土豆切开后发生褐变,用水浸泡能防止褐变,但会引起营养物质流失。用土豆片进行实验,测得其食用品质、淀粉含量和维生素C含量随浸泡时间的变化如下:

土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒,就算是把变绿、发芽的部位削掉,也不宜食用。除食用外,土豆还可以作为原料广泛用于医药、化工、纺织、造纸等工业中。
依据文章内容回答下列问题。
(1)表1中的“钙”指的是________(填“元素”或“原子”)。
(2)由图1可知:60min内,______(填序号)。
A浸泡30min比10min脆性分值高
B浸泡10min,硬度、咬碎感均无明显变化
C随着浸泡时间的增加,粘结性、弹性分值均降低
(3)由图2可知:土豆片的淀粉含量与浸泡时间的关系是________________。
(4)変绿、发芽的土豆不宜食用,其原因是___________________。
(5)下列说法不正确的是____(填序号)。
A土豆是四大粮食作物之一 B土豆中维生素C含量最高
C用水泡可防止土豆片褐変 D土豆开发应用的前景广阔
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国规定面粉增白剂从5月1日起禁止用于面粉加工。我国食品在面粉中允许添加过氧化苯甲酰最大剂量为0.06g/kg。面粉增白剂过氧化苯甲酰(C14H10O4)超标会破坏面粉的营养,水解后产生的苯甲酸会对肝脏造成损害。下列关于过氧化苯甲酰说法正确的是( )
A.过氧化苯甲酰属于一种氧化物
B.过氧化苯甲酰中碳的质量分数为69℅
C.过氧化苯甲酰是由14个碳原子、10个氢原子和4个氧原子构成
D.面粉中添加过量的增白剂没有任何危害
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com