
【题目】根据如图甲、乙两种物质的溶解度曲线回答相关问题:
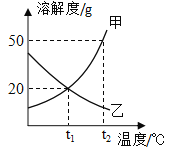
(1)常压下,CO2在水中的溶解度随温度的变化趋势类似于________(填“甲”或“乙”)曲线。
(2) t2℃时若将75g甲的饱和溶液稀释成10%,需加水的质量为____________。
(3)将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃(其他条件不变),所得溶液的溶质质量分数的关系是甲_________乙。(填“>”“<”或“=”)
【答案】乙 175g >
【解析】
(1)影响气体的溶解度的外界因素有压强和温度,压强一定,温度越高,气体溶解度越小,因此曲线乙表示CO2在水中的溶解度随温度的变化。故填:乙。
(2)由曲线图知,物质甲t2℃时,溶解度是50g,则150g甲的饱和溶液里含有溶质50g,则75g甲的饱和溶液中含有溶质25g,将75g甲的饱和溶液稀释成10%,溶质不变仍然是25g,设需要水的质量为x,可列式:![]() ,可得x=175g。故填:175g。
,可得x=175g。故填:175g。
(3)将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃,因物质甲的溶解度随温度的降低而降低,因此甲的饱和溶液会有晶体析出,溶质的质量分数减小;因物质乙的溶解度随温度的降低而升高,因此乙的饱和溶液不会有晶体析出,溶质的质量分数不变,根据溶解度曲线,降温至t1℃等质量的饱和溶液中甲的溶质仍然比乙多,因此降温后所得溶液甲的溶质质量分数大于乙。故填:>。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源,煤气化和液化流程示意图如下:
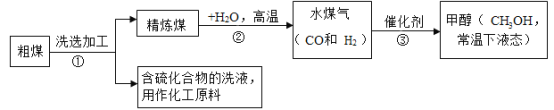
(1)第①步操作发生的是_____(填“物理”或“化学”)变化.
(2)第②步是精炼煤与水蒸气的反应,化学方程式为_____.
(3)第③步中参加反应的CO与H2的微粒个数比是1:2,该反应的基本类型属于_____,甲醇属于_____(填无机物或有机物).
(4)含硫化合物洗液经过提炼后,可用来制硫酸,过程是:含硫化合物氧化得到SO2,SO2进一步氧化得到X,X与水反应得到H2SO4,则X的化学式为_____.
(5)从“绿色化学”的角度分析,“煤的汽化和煤的液化”生产流程的优点_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学中常见物质间的转化关系,其中只有甲为单质,其他都是化合物; A是植物进行光合作用的一种重要原料,C可用于中和酸性土壤,反应②属于中和反应,其余反应条件、部分反应物和生成物已略去,试推断:

(1)B物质的化学式_______;E物质的类别是_________。
(2)写出下列化学方程式:甲→B:_________。反应③:________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组同学欲利用氢氧化钠溶液与硫酸探究中和反应中的热量变化.请你参与探究实验.
(1)实验小组设计了如下方案:在装有20mL10%NaOH溶液的小烧杯中不断滴加质量分数为90%的浓硫酸,边滴边搅拌,并用温度计测量实验过程中烧杯内液体温度的变化情况,请你分析该实验方案中存在的不足之处,提出两点改进措施_____、_____.
(2)实验过程中发生反应的化学方程式是_____.
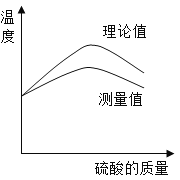
(3)如图为该反应中温度与滴加的硫酸质量变化关系的理论值和测量值的曲线比较情况.
①图示说明实验中测得的中和反应放出的热量比理论值_____(填“高”或“低”).
②请指出造成理论值和测量值差异的一点原因_____.
③图中温度达到最高值后降低的原因是_____.
(4)实验小组欲进一步探究氢氧化钠溶液与硫酸反应放热快慢的因素,你认为有哪些呢?请提出猜想,并设计实验.
猜想:_____
实验方案:_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】进行如下微型实验,研究物质的性质。
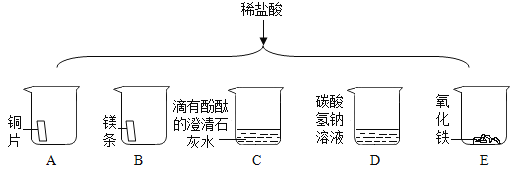
(1)烧杯 B 中发生的化学反应方程式是____________。
(2)能证明 C 中发生反应的现象是____________。
(3)有一只烧杯中的物质不与稀盐酸反应,原因是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲乙两种物质的溶解度曲线,下列说法正确的是( )
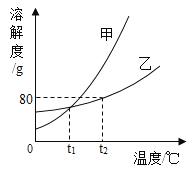
A.tl℃时甲和乙的溶液升温到t2℃,所得溶液的溶质质量分数一定相等
B.t2℃时等质量的甲、乙的饱和溶液中,乙中的溶质质量大于甲的溶质质量
C.t2℃50g水中最多能溶解40g乙物质
D.t2℃时甲和乙的饱和溶液降温,甲析出的固体一定比乙多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样,已知它是无色液体,是初中化学常用的试剂,小华等几位同学很感兴趣,决定对其成分进行探究:

(提出问题)这瓶试剂溶质是什么?
(交流研讨)根据受损标签的情况判断,这瓶试剂不可能是______(填字母序号).
A酸 B碱 C盐
(查阅资料)
①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
②Na2CO3、NaHCO3溶液都呈碱性,NaCl溶液呈中性。
③室温下(20℃)时,4种物质的溶解度的数据如下。
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 36 | 109 | 215 | 9.6 |
(得出结论)小华根据试剂瓶上标注和上表溶解度数据判断,这瓶试剂不可能是______
(猜想与实验)
(1)小亮用洁净的玻璃棒蘸取该溶液,滴到湿润的pH试纸上,测得pH=11,他判断该溶液不可能是______
(2)小强的猜想是Na2CO3溶液。
(质疑)小华则不同意小强的观点,认为溶液中有Na2CO3还可能有NaOH。请你帮助他完成以下探究方案:
探究步骤 | 预计现象 | 结论 |
步骤一:取样品于试管中,向其中滴加足量的______溶液并过滤 | 产生白色沉淀 | 溶液中:既含Na2CO3,又含有NaOH |
步骤二:向上述滤液中滴加酚酞试液 | 酚酞试液变______色 |
(反思)NaOH溶液会因接触空气而变质,写出该反应的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)溶液配制是化学实验室的常见操作,要把50g质量分数98%的浓硫酸,稀释为质量分数20%的硫酸,则需要加水的体积_____mL(水的密度为1g/cm3),将稀硫酸滴入铁粉和氧化铜的混合粉末中,微热,充分反应后过滤,向滤液中加入洁净铁片无现象,则滤液中的溶质是_____(填化学式)。请写出上述反应中的一个化学方程式_____
(2)纯碱(Na2CO3)中常含有少量的氯化钠.化学实验小组同学称取12g纯碱样品放入烧杯中,加入水使其完全溶解,向其中滴加氯化钙溶液至过量,测得加入氯化钙质量与生成沉淀质量如图所示。
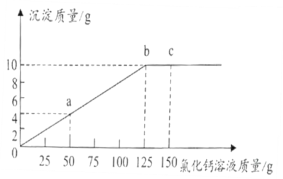
①计算样品中碳酸钠的质量分数_____(要求写出计算过程,精确到0.1%)。
②若要计算氯化钙溶液中的溶质质量分数,如果利用上图中的a、b、c三个数据,其中不能用作计算的是_____(填标号)所对应的数据。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】专家提示在日常防控新型冠状病毒中,“84”消毒液可以使病毒灭活。

(1)其有效成分 NaClO 中氯元素的化合价为______________,所含的阳离子为_____________(写离子符号)。
(2)“84”消毒液的消毒原理为 2NaClO+CO2+X=Na2CO3+2HClO,生成的 HClO(次氯酸具有较强的杀菌 作用。化学方程式中 X 的化学式为_____________。
(3)下图是生活中常见洗涤用品的的 pH,混用会降低去污效果甚至产生危害的组合是_____________(填序号)。

A洁厕灵和“84”消毒液 B肥皂水和威猛先生
C“84”消毒液和肥皂水 D“84”消毒液和威猛先生
(4)探究发现,曝露在空气中(阳光充足)的“84”消毒液的消毒效果随时间的推移而减弱。据此,你认为“84”消毒液应________保存。
(5)“84”消毒液有一定的刺激性与腐蚀性,必须稀释以后才能使用。将 50g 含 NaClO 5%的“84”消毒液稀释至 1%,需向原溶液中加入水的质量为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com