
【题目】“氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na2CO3·3H2O2)。某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究。
【查阅资料】
Ⅰ.过碳酸钠在水中易离解成Na2CO3和H2O2,其水溶液具有Na2CO3和H2O2的双重性质;
Ⅱ.过碳酸钠能与盐酸反应:2(2Na2CO3·3H2O2)+8HCl=8NaCl+4CO2↑+3O2↑+10H2O;
Ⅲ.过碳酸钠的去污能力主要与其在反应中释放出的“活性氧”有关,“活性氧”含量越高,去污能力越强。
(1)20℃时,测得1%过碳酸钠水溶液的pH为10.5,说明其溶液呈______(选填”酸性”、“中性”或“碱性’" )。
(2)向过碳酸钠水溶液中加入少量MnO2时产生大量气泡,发生反应的化学方程式是_____ 。
(3)过碳酸钠样品中“活性氧”含量可按如下公式计算:
![]()
为测定某过碳酸钠样品中“活性氧”含量,取20.0g样品按下图实验装置与足峨盐酸反应。(已知样品中杂质不溶于水且不与酸反应,装置气密性良好)
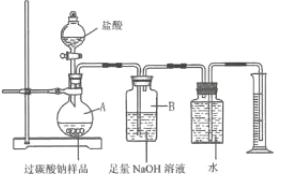
① 将盐酸慢慢滴入A中,反应一段时间,观察到_______,停止滴加盐酸。
② 装置B可吸收生成的CO2,该反应的化学方程式是________________。
③ 甲同学认为若要得出生成氧气的质量,除要记录量筒内液体的读数外,还需要知道的数据是该实验条件下的__________。
④ 将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的“活性氧”含量,写出其计算过程。
⑤ 完成上述探究后,丙同学提出:称量反应前后装置B的质量,其质量差就是反应生成CO2的质量,据此可计算出样品中“活性氧”含量。但丁同学认为该方案不合理,丁同学的理由是_____________________(填写一条即可)。
【答案】(l)碱性;(2)2H2O2 ![]() 2H2O+O2↑。(3)① 无气泡产生。②CO2+2NaOH=Na2CO3+H2O。
2H2O+O2↑。(3)① 无气泡产生。②CO2+2NaOH=Na2CO3+H2O。
③ 氧气密度。④12%。⑤ 盐酸挥发出的HCl进入B中(或生成的CO2没有完全被NaOH溶液吸收)
【解析】【查阅资料】Ⅰ.过碳酸钠在水中易离解成Na2CO3和H2O2,其水溶液具有Na2CO3和H2O2的双重性质;Ⅱ.过碳酸钠能与盐酸反应:2(2Na2CO3·3H2O2)+8HCl=8NaCl+4CO2↑+3O2↑+10H2O;Ⅲ.过碳酸钠的去污能力主要与其在反应中释放出的“活性氧”有关,“活性氧”含量越高,去污能力越强。(1)20℃时,测得1%过碳酸钠水溶液的pH为10.5,PH>7,呈碱性,PH<7,呈酸性。说明其溶液呈碱性。(2)向过碳酸钠水溶液中加入少量MnO2时产生大量气泡,发生反应的化学方程式是2H2O2 ![]() 2H2O+O2↑。(3)过碳酸钠样品中“活性氧”含量。① 将盐酸慢慢滴入A中,反应一段时间,观察到无气泡产生,停止滴加盐酸,此时碳酸钠已反应完。② 装置B可吸收生成的CO2,该反应的化学方程式是CO2+2NaOH=Na2CO3+H2O。③ 甲同学认为若要得出生成氧气的质量,除要记录量筒内液体的读数外,还需要知道的数据是该实验条件下的氧气密度。④ 将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的“活性氧”含量∶2(2Na2CO3·3H2O2)+8HCl=8NaCl+4CO2↑+3O2↑+10H2O;8NaCl→3O2
2H2O+O2↑。(3)过碳酸钠样品中“活性氧”含量。① 将盐酸慢慢滴入A中,反应一段时间,观察到无气泡产生,停止滴加盐酸,此时碳酸钠已反应完。② 装置B可吸收生成的CO2,该反应的化学方程式是CO2+2NaOH=Na2CO3+H2O。③ 甲同学认为若要得出生成氧气的质量,除要记录量筒内液体的读数外,还需要知道的数据是该实验条件下的氧气密度。④ 将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的“活性氧”含量∶2(2Na2CO3·3H2O2)+8HCl=8NaCl+4CO2↑+3O2↑+10H2O;8NaCl→3O2
![]() =
=![]() ,x=2.4g
,x=2.4g
![]() ×100%=12%。
×100%=12%。
⑤ 完成上述探究后,丙同学提出:称量反应前后装置B的质量,其质量差就是反应生成CO2的质量,据此可计算出样品中“活性氧”含量。但丁同学认为该方案不合理,丁同学的理由是盐酸挥发出的HCl进入B中(或生成的CO2没有完全被NaOH溶液吸收).


科目:初中化学 来源: 题型:
【题目】小苏打是发酵粉的主要成分之一,可用于制作发面食品.一化学兴趣小组对某小苏打样品中各成分的含量做了如下测定:将一定质量的该样品(已知杂质只含NaCl)加水全部溶解后,得到104.4g溶液,向该溶液中逐渐加入稀盐酸,产生的气体与加入稀盐酸的质量关系如图所示.试计算:
(1)m的值为 .
(2)当恰好完全反应时,所得溶液的溶质质量分数为3%,求原小苏打样品中NaHCO3与NaCl的质量比 .

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学知识有助于我们正确认识、理智选择、科学生活。下列说法不正确的是
A.共享单车为人们绿色出行提供了便利
B.常用“加铁酱油”有助于预防缺铁性贫血
C.用化学材料刚装修好的房子,会释放出甲醛等物质,不宜立即入住
D.钛合金因抗腐蚀性强,被应用于“蛟龙号”潜水器上。钛合金属于有机合成材料
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关“碳循环”的说法中,不合理的是
A.绿色植物光合作用吸收二氧化碳释放氧气
B.动物呼吸作用吸收氧气释放二氧化碳
C.用石灰水吸收空气中过量的二氧化碳,以解决温室效应
D.提倡“低碳生活 ”,大力推广风能、太阳能等能源。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋是巨大的资源宝库,从海洋中可以获得很多物质,连云港海水资源丰富。
(l)通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。实验室中除去粗盐中不溶性杂质获得精盐的步骤是:溶解→过滤→蒸发→计算产率等。
① 过滤操作中玻璃棒的末端要轻轻的斜靠在______一边。蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是______。
② 下列操作可能导致精盐产率偏高的是______(填字母)。
a.食盐没有完全溶解即过滤
b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到称量纸上
(2)海水中含量最多的氯化物是氯化钠,其次是氯化镁。下图是从海水中获得氯化镁溶液的流程。
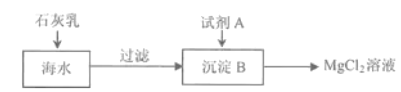
① 在海水中加人石灰乳后,发生反应的化学方程式是______________。
② 上述过程中试剂A与沉淀B 发生的是中和反应,则试剂A是(填名称)______。
(3)2017年5月18日,在中国南海海域实现可燃冰(CH4·nH2O)试采成功,这将使人类能源格局翻开新篇章。

① 可燃冰中,水分子形成一种空间笼状结构,甲烷和少虽N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于_________(选填“纯净物”或“混合物”)。
② 若某种可燃冰中CH4与H2O的质量比是1:9,则该可嫩冰中n=_______。
③ 可燃冰中甲烷完全燃烧的化学方程式是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钠和硝酸钾两种固体的溶解度曲线如右图所示。下列说法正确的是
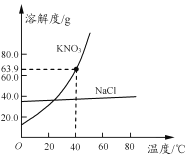
A.硝酸钾的溶解度大于氯化钠的溶解度
B.常用冷却结晶的方法从氯化钠溶液中获得其晶体
C.40℃时,将35 g硝酸钾晶体放入50 g水中,充分搅拌后,所得溶液的溶质质量分数为39.0%
D.将20℃的硝酸钾饱和溶液升温至60℃,溶液的溶质质量分数增大(忽略水分蒸发)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
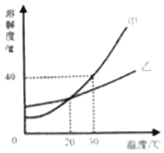
A.30℃时,甲的饱和溶液溶质质量分数为40%
B.20℃时,甲、乙的饱和溶液中所含溶质的质量一定相等
C.将等质量的甲、乙固体,分别配成30℃的饱和溶液,所需水的质量:甲>乙
D.将20℃时甲、乙的饱和溶液升温到30℃,所得甲、乙溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂以含有FeSO4和少量H2SO4的废水为原料制备FeSO4·7H2O的步骤如下:
①调节废水pH;②过滤; ③蒸发浓缩 ④结晶池中结晶 ⑤收集晶体,洗涤、干燥
(1)调节废水pH时,适宜加入 。(填序号)
A.Fe B.Cu C.Ca(OH)2
(2)实验室中,完成过滤操作需要的玻璃仪器有玻璃棒、 和 ,过滤和蒸发操作中玻璃棒的作用分别是 、 。
(3)结晶池底部有一定坡度是主要目的是 。
(4)用冰水洗涤FeSO4·7H2O晶体的目的是 ,低温干燥的目的是 。
(5)结合下图,补充完整有硫酸亚铁溶液中晶体出FeSO4·7H2O的实验方案:
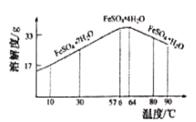
蒸发浓缩, ,过滤、洗涤、干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com