
【题目】为测定某过氧化钠样品的纯度,将2 g该样品与足量X发生如下反应(杂质不参与反应):2Na2O2+2X=4NaOH+O2↑,生成气体质量与时间的关系如图所示。回答问题:

(1)过氧化钠中钠、氧元素的质量比为_________;物质X的化学式为__________。
(2)生成氧气的质量是____________g。
(3)计算2克该样品中过氧化钠的质量________________。
科目:初中化学 来源: 题型:
【题目】借助科学的化学实验方法,我们可以从不同角度正确地认识物质。
(实验一)如图所示实验可用于测定某种化肥的组成。
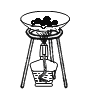
加热时,该物质会迅速分解,生成有刺激性气味的氨气(NH3)、水蒸气以及一种能使澄清石灰水变浑浊的气体。
(1)该物质是由_____组成;
(2)根据该实验,你判断该物质属于_____(填“单质”或“化合物”),这种化肥应该如何保存?_____。
(实验二)有关气体制取的研究,请根据下列装置图回答问题

(1)实验室用氯酸钾和二氧化锰制取氧气时,可选用的发生装置是(填字母代号)_____;收集装置可用C,其原因是_____,其中二氧化锰起_____作用。用化学方程式表示氯酸钾和二氧化锰发生的反应_____。
(2)实验结束拆除装置后,发现试管炸裂,试分析造成此后果的可能原因_____(要求答出两点即可)。
(3)F装置中充满水时,可作为氧气的收集装置,则氧气应从_____(填“⑥”或“⑦”)端通入。某同学用E装置收集氧气时,集气瓶只装了一半的水,则他收集到的氧气的体积分数大约是_____。
(4)已知氢气是一种难溶于水的气体,密度比空气小。实验室用金属锌和稀硫酸在常温下制得氢气。应该选择的发生和收集装置是_____。(填字母代号)
查看答案和解析>>
科目:初中化学 来源: 题型:
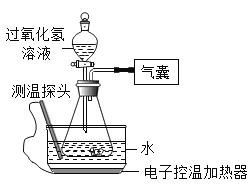
【题目】某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。
(猜想与假设)影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂种类。
(实验记录)同学们进行6组实验,实验记录如下:
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
过氧化氢溶液的浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
过氧化氢溶液的体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
锥形瓶中的物质 | 0.5g NaCl | 0.5g FeCl3 | ||||
60分内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(解释与结论)
(1)实验②中应加入过氧化氢溶液的体积x是________mL。
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定__________来比较过氧化氢的分解速率。
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是__________(填序号)。
(4)通过实验①、②、④可得出的结论是_______________。
(反思与评价)
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是____________、____________(答两点)。
(6)你认为影响过氧化氢溶液分解速率的因素还有哪些?请设计实验验证你的猜想
(猜想假设)___________________。
(实验操作)___________________。
(实验结论)___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某钙片的标签如下,且知此钙片成分中只有碳酸钙CaCO3含有钙元素。

(1)高钙片中的“钙”应理解为 ___________(填序号)
①元素 ②原子 ③分子 ④单质
(2)维生素种类较多,其中维生素D2的化学式为C28H44O,则维生素D2的相对分子质量为_________,维生素D2中C、H、O三种元素的原子个数之比为______
(3)如果一个青少年每天需要补钙0.8克,其中0.6克都来自于牛奶,其余服用钙片。请计算每天他需要补充碳酸钙多少克?(要求有计算过程)________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B.…H八种物质,有下图所示转化关系:其中D能使带火星的木条复燃,E常温下为液态,H是一种黑色固体,在①的反应前后B的质量和化学性质都不改变,试推断:
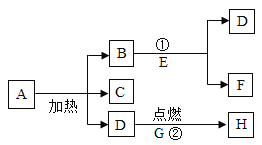
(1)写出物质的化学式:C________________,E________________;
(2)写出反应①的化学方程式:________________,写出反应②化学方程式:________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类赖以生存的物质之一,也是实验室最常用的物质之一。
(1)下列含“水”的物质属于纯净物的是_____(填字母序号)。
A 自来水 B 冰水混合物 C 河水 D 蒸馏水
(2)明矾是常用的净水剂之一,其作用是_____;用明矾净化后的水是_____(填“软水”或“硬水”);高铁酸钾(K2FeO4)也可用来净化水, K2FeO4中铁元素的化合价为_____。制备K2FeO4的化学方程式为2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6X+8H2O,则X的化学式为_____。
(3)为了防止水的污染,下列做法有利于保护水资源的是_____ (填编号)。
①抑制水中所有动、植物的生长 ②不任意排放工业废水 ③大量使用化肥农药 ④生活污水经过净化处理后再排放
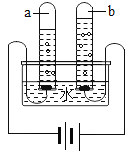
(4)如图是简易的电解水实验示意图。其中b管产生的气体为_____,反应的化学方程式为_____;晓明同学用自制电解器电解水,在水中加少许硫酸钠,目的是_____;当他在103.6g质量分数为5%的硫酸钠溶液中通电一段时间后,产生3.2 g氧气,此时另一极产生的氢气质量为_____;配制5%的硫酸钠溶液用到的玻璃仪器有烧杯、玻璃棒、_____,此时,硫酸钠的质量分数为_____(精确到0.01%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图分别盛有不同物质的容器中,所盛物质:(请用容器下的字母代号填写)
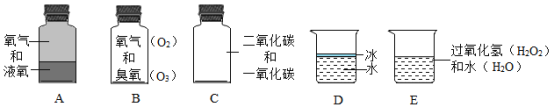
(1)属于单质的是____________;
(2)属于化合物的是____________;
(3)属于纯净物的是_____________;
(4)属于混合物的是_____________;
(5)属于氧化物的是___________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】再生水是国际公认的“第二水源”,是将生产生活等污水经过处理达标后,可以在一定范围内使用的水,生产再生水的主要流程如图.

(1)一级处理时,污水经过格栅后还需要向其中加入絮凝剂污水经过格栅起到的作用是______(填常用净水操作名称),絮凝剂可以是______;
(2)二级处理时需要使用活性炭,它的作用是______;
(3)二级处理后的水经过消毒处理,得到再生水,消毒属于______(选填“物理”或化学)变化.
(4)检验再生水是否为硬水可使用的物质是______,使硬水软化的简单方法是.______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com