
【题目】去年.我国科学家在自然界中发现金属铀,属全球首次。下图是铀元素的相关信息.其中正确的是
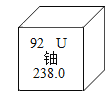
A.铀原子的中子数是92
B.铀原子的质量为238.0g
C.自然界中很长时间没发现可能是金属铀的化学性质很活泼
D.铀原子的核外电子数是146
【答案】C
【解析】
A、根据元素周期表中的一格可以知道,左上角的数字为92,表示原子序数为92;根据原子序数=核电荷数=质子数=核外电子数,则该元素原子的核内质子数和原子核外电子数均为92,而不是中子数为92,故选项说法错误。
B、根据元素周期表中的一格可以知道汉字下面的数字表示相对原子质量,该元素的相对原子质量为238.0,相对原子质量单位是“1",不是“克",故选项说法错误。
C、自然界中很长时间没发现铀,可能是金属铀的化学性质很活泼,故选项说法正确。
D、根据元素周期表中的一格可以知道,左上角的数字为92,表示原子序数为92;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为92,故选项说法错误。
故选:C。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案科目:初中化学 来源: 题型:
【题目】化学课外小组的同学想要用一氧化碳气体(含有少量杂质二氧化碳和水蒸气)测定样品中氧化铁的质量分数,装置如图所示,回答下列问题:
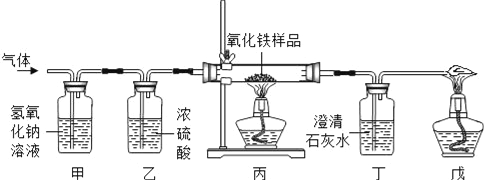
(1)乙装置的作用是____________.
(2)丙装置中反应的化学方程式是__________________.
(3)丁装置中的现象是_______________.
(4)戊装置的作用是_______________.
(5)要生产1000t含杂质3%的生铁,需要含Fe2O390%的铁矿石______t(保留整数).
查看答案和解析>>
科目:初中化学 来源: 题型:
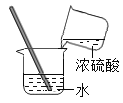
【题目】某学习小组想用锌和稀硫酸反应制取氢气,他们按照如图所示操作对浓硫酸进行稀释。某同学提出锌和浓硫酸是否也能产生氢气呢?于是他将少量浓硫酸加入到盛有锌粒的试管中,发现生成的气体具有刺激性气味。同学们对产生的气体很感兴趣,于是进行了探究。
(猜想与假设)
气体是:①H2 ②SO2 ③H2和SO2
同学们经过讨论,便直接否定了猜想①,原因是_______
(查阅资料)
(1)浓硫酸具有强氧化性,它与一些金属单质反应会产生二氧化硫气体
(2)二氧化硫能使红色品红溶液褪色
(3)氢气具有还原性
(进行实验)
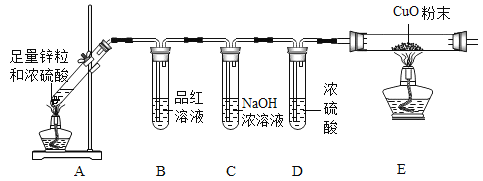
(解释与结论)
(1)同学们稀释浓硫酸时,玻璃棒的作用是_______。
(2)写出锌与稀硫酸反应的化学方程式_______。
(3)装置中氢氧化钠浓溶液的作用是_______。
(4)通过此实验,同学们证明了猜想③正确,请写出他们依据的实验现象_____。
(反思与评价)
经过讨论,小组中某个同学认为上述实验有不妥之处,他将上述实验进行改进,将足量锌粒换成少量锌粒,重复实验,得出猜想②正确。
(5)补全锌和浓硫酸反应的化学方程式:Zn+2H2SO4(浓)=ZnSO4+SO2↑+______
(6)请解释第一次实验中得到氢气的原因________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明喜欢养金鱼,他上网查阅资料得知:鱼缸中每升水的溶氧量低于0.003 g时,鱼就会死亡。过氧化钙(CaO2)是一种化学增氧剂,其反应原理是 2CaO2+2H2O=2Ca(OH)2+O2↑。小明将2 g含过氧化钙72%的固体放入盛有100 L水的鱼缸中,请你通过计算分析,当氧气完全释放后,鱼缸中水的溶氧量是否符合最低要求________(假设产生的氧气完全溶于水,其他因素忽略不计)?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列装置图,回答有关问题:
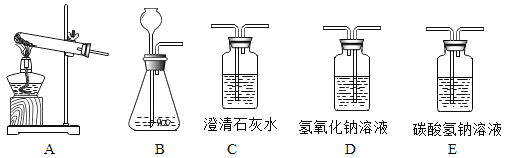
(1)实验室用锌和盐酸制取氢气,发生装置应选____(填序号),检查该装置的气密性方法是 ____。
(2)写出实验室用A制取氧气的化学方程式____。
(3)用![]() 装置来检验二氧化碳气体,发现新配制的澄清石灰水没有变浑浊,你认为可能的原因是该气体中含有____(填物质名称)气体。用图中____(填序号)除去
装置来检验二氧化碳气体,发现新配制的澄清石灰水没有变浑浊,你认为可能的原因是该气体中含有____(填物质名称)气体。用图中____(填序号)除去![]() 中含有的该气体。
中含有的该气体。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验室常用二氧化锰催化过氧化氢分解的方法制取氧气。那么,影响过氧化氢分解快慢的因素到底有哪些呢?某化学兴趣小组对此进行如下研究。
(提出问题)影响过氧化氢分解快慢的因素有哪些?
(猜想与假设)假设1:过氧化氢溶液的浓度;
假设2:催化剂的质量;
假设3:温度;
假设4:_______。
(设计实验)小明同学设计如下实验方案进行验证。
序号 | H2O2溶液的浓度 | H2O2溶液的质量 | 温度 | MnO2的质量 | 收集O2的体积 | 时间 |
① | 5% | 12 g | 20 ℃ | 0.2 g | 125 mL | 20 s |
② | 30% | 12 g | 20 ℃ | 0.2 g | 125 mL | 2 s |
③ | 30% | 12 g | 40 ℃ | 无 | 125 mL | 148 s |
(1)通过对比实验①和②可知,过氧化氢分解的快慢与_______有关。
(2)在过氧化氢分解前后,二氧化锰的质量和_______不变。
(3)请你写出用二氧化锰催化过氧化氢分解的化学方程式:_______。
(讨论交流)(4)小红同学认为在这个实验中,必须用排水法收集氧气,理由是_______。
(5)小辉同学提出小明的方案无法验证温度对过氧化氢分解快慢的影响,请你帮他说出理由:____。
(拓展延伸)同学们查阅资料得知,FeCl3溶液对过氧化氢分解也有影响。在老师的指导下设计实验继续探究,向两支试管中分别加入等质量、不同浓度的H2O2溶液,再加入等质量、等浓度的FeCl3溶液,分别用气压传感器测定两试管中气体压力的变化曲线,如图1。
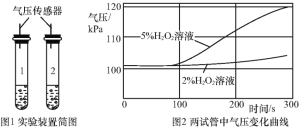
(6)为保证实验的准确性,请你设计向两试管中加入FeCl3溶液的具体方法:__。
(7)请你从图2曲线中找出FeCl3溶液对H2O2分解影响的两条规律性结论:__;____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据如图装置回答问题:
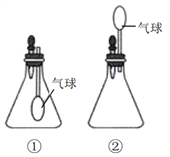
(1)使用装置①进行实验时,将滴管中的氢氧化钠溶液加入到盛有二氧化碳的锥形瓶中,可观察到的现象是__________,原因是 _________________________。
(2)使用装置②进行实验时,将滴管中的物质加入到锥形瓶中,发现气球鼓起来,请你推测锥形瓶中的物质可能是________,滴管中对应的物质可能是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用钛白渣[主要成分为 FeSO4 ,还含有少量 Fe2(SO4)3、MgSO4及 TiOSO4 ]为主要原料生产氧化铁黄(FeOOH)的一种工艺流程如下:

(背景信息)
a 在“溶解”时,TiOSO4 跟水发生反应,生成难溶于水的 H2TiO3和另一种溶于水的酸;
b 在“除杂”时,加入 NH4HF2 固体是为了使溶液显弱碱性,使 Mg 2+ 能与 OH-结合生成沉淀,从而可除去 Mg 2+ ;
c 在“氧化”中,Fe 3+与 OH-也可能结合成沉淀。
(1)操作 X 的名称是_______________。
(2)TiOSO4 与水发生反应的化学方程式为_________________________________。
(3)实验测得“氧化”时溶液的温度、pH 对氧化铁黄产率的影响如下图所示。

①氧化时反应的温度最适宜控制在_________________℃。
②氧化时最好控制 pH 在_____________左右,pH 过小或过大均会导致氧化铁黄产率偏低。请分析pH 过大会导致氧化铁黄产率偏低的可能原因:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com