
【题目】(3分)下列问题的研究中,未利用对比实验思想方法的是( )
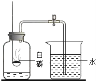
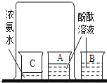
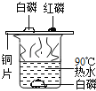
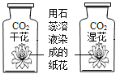
A.研究空气中氧气含量 B.研究分子运动 C.研究燃烧的条件 D.研究二氧化碳与水的反应
【答案】A
【解析】研究空气中氧气含量是利用白磷燃烧,消耗空气中氧气,使瓶内气体压强减小,水在外界大气压的作用下进入集气瓶内,所以根本不存在对照实验,故A正确;烧杯A中的酚酞试液和烧杯B中的酚酞试液属于对照试验,烧杯A置于放有浓氨水的烧杯附近;烧杯B置于空气中,在空气中没变色,说明空气不能使酚酞试液变红,烧杯A中变红说明氨分子在不断运动,进入烧杯A中,使酚酞试液变红,说明了分子在不断运动,所以利用了对比实验的原理,故B错;铜片上的白磷与铜片上的红磷属于对照实验,都与氧气接触,都属于可燃物,变量是着火点不同,白磷着火点低,红磷着火点高,热水能达到白磷的着火点,达不到红磷的着火点,从而证明可燃物燃烧温度必须达到可燃物的着火点,所以属于对比实验,故C错;纸花都是用石蕊溶液染成,都与二氧化碳接触,变量是一瓶内纸花中有水,一瓶内纸花中没有水,由实验可知没有水的纸花没变色,含有水的纸花变成红色,说明二氧化碳与水反应生成了一种酸,酸使石蕊试纸变成红色,所以属于对比实验,故D错。


科目:初中化学 来源: 题型:
【题目】铝和铝合金是一类重要的金属材料。工业上用铝土矿(含有Al2O3和SiO2,不考虑其他杂质)制取金属铝的基本流程如下:
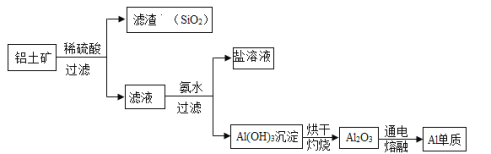
已知:①SiO2是一种难溶于水,也不与盐酸、硫酸反应的物质。
②铝盐与氨水反应,生成氢氧化铝沉淀和铵盐。
请回答下列问题:
(1)金属铝抗腐蚀性强,其原因是___________(填字母)
A.铝不易与酸反应 B.铝表面生成致密的氧化物薄膜
C.铝不易与氧气反应 D.铝是一种不活泼的金属
(2)图中盐溶液中溶质的化学式为____________.
(3)电解熔融的Al2O3,除得到金属铝之外,还可以得到另一种单质,写出其反应的化学方程式_______.
(4)工业上电解熔融Al2O3的时,为了降低Al2O3的熔点还加入了冰晶石(Na3AlF6)熔剂,冰晶石中F元素的化合价为_______,冰晶石在物质的分类中属于_____(填字母)。
A.氧化物 B.盐 C.碱 D.酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D均为无色无味的气体,D是天然气的主要成分,E和水是组成元素相同的液体,如图所示6个化学反应都有水生成,其中部分生成物已省略,请回答下列问题:
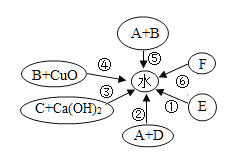
(1)写出物质的化学式:A______,B_________,D_________。
(2)写出反应①的化学方程式__________________________;若反应①和⑥的基本反应类型相同,则F可能是______(填化学式)。
(3)写出反应③的化学方程式__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)镁与NH4Cl溶液反应,不仅有一种盐生成,还有气泡产生。为确定气体的成分,进行下列实验探究。
(一)探究:气体可能是HCl、02、NH3、H2中的一种或几种。
(二)实验:
(1)甲同为确定是否含有HCl,他将气体通入酸化的硝酸银溶液中,无明显现象,则该气体中_ HCl (填“有”或“无”)。
(2)乙同学认为只有02,则可用_ 来检验。实验证明乙同学的观点不正确。
(3)丙同学为判断是否含有H2,同时确定气体成分,通过查阅资料得知:
2NH3+3CuO == 3Cu+N2+3H20于是他设计了如下图实验装置:
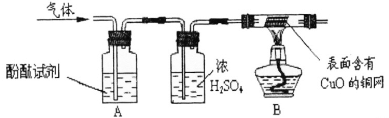
(三)实验现象与结论:A中观察到_ ,证明有NH3; B中玻璃管内观察到_ ,证明有H2。
(四)实验反思:
(4)浓硫酸的作用是_ 。
(5)大家认为丙同学在加热之前,应对气体先_ 以确保安全。
(6)写出Mg与NH4Cl溶液反应的化学方程式 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过一年的化学学习,相信你已经初步掌握了实验室制取气体的有关知识.请结合图示回答问题。
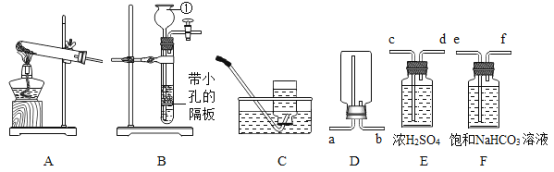
(1)图中标号①仪器的名称为:______。
(2)实验室用A装置制取氧气的化学方程式为_____。
(3)实验室用B和C装置组合可制取的气体是______。
(4)若用D装置收集二氧化碳,气体应该从_______端进入,制得的二氧化碳中往往含有氯化氢和水蒸气,若使用E、F装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→_____用端口字母表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下列实验操作可完成两个实验。甲实验为粗盐中难溶性杂质的去除,乙实验为配制溶质的质量分数为10%的氯化钠溶液。下列说法中,正确的是
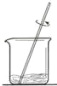
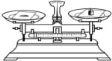

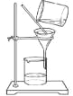
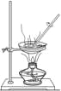
① ② ③ ④ ⑤
A.甲实验的步骤是①④⑤,其中去除杂质的关键步骤是蒸发
B.甲实验各步操作中,玻璃棒的作用都是相同的
C.乙实验若按照②③①的步骤进行操作, 则配制的溶液浓度偏大(p水=1g/cm3)
D.乙实验中,若①所用的烧杯内壁沾有水,对配制的溶液浓度无影响
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物。同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究。
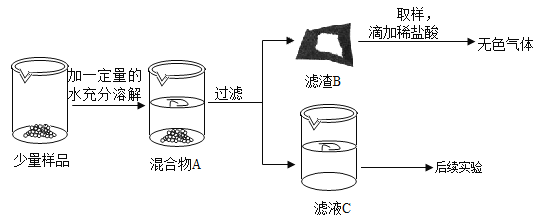
查阅资料:(1)Ca(OH)2、Na2CO3溶于水无明显的温度变化。
(2)CaCl2+Na2CO3=2NaCl+CaCO3↓。
(3)CaCl2溶液呈中性。
(1)滤渣B中一定含有_____,产生该物质的化学方程式可能是___(写出一个即可)。
(2)滤液C成分的探究。
(猜想)滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④____。
(设计方案并进行实验)甲、乙、丙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3。
乙同学:取滤液C少许放入试管中,滴加足量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH。
丙同学:取滤液C少许放入试管中,滴加Ca(OH)2溶液,有白色沉淀产生。向上层清液中滴加无色酚酞,无色酚酞变成红色,则滤液C中的溶质是NaOH和Na2CO3。
(反思与评价)
丁同学认真分析上述三位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断。他认为滤液C中的溶质一定含有________,可能含有NaOH。为进一步确认滤液C中是否含NaOH,请你帮助他设计实验进行验证。
实验操作 | 实验现象 | 实验结论及解释 |
________ | ________ | 猜想④正确 |
(3)实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是__________(填序号)。
① 样品中一定含NaOH ② 样品中一定含Na2CO3
③ 样品中含NaOH、CaO中的一种或两种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】丁酸乙酯(化学式为![]() )是一种无色、具有菠萝香味的液体,常用作食品、饮料的调香剂。请根据丁酸乙酯的化学式计算:
)是一种无色、具有菠萝香味的液体,常用作食品、饮料的调香剂。请根据丁酸乙酯的化学式计算:
(1)每个丁酸乙酯分子是由___________个原子构成的。
(2)丁酸乙酯中碳、氢两种元素的质量比是___________(填最简整数比)。
(3)___________g丁酸乙酯中含6.4g氧元素。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶保管不当的试剂(如下图),其残缺的标签中只剩下“Na”和“10%”的字样。已知它是无色液体,是初中化学常用的试剂。小欣和小芳同学很感兴趣,决定对其成分进行探究。
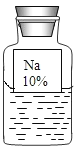
(提出猜想)
(1)这瓶试剂可能是_____溶液
①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl溶液。
(2)根据受损标签的情况判断,这瓶试剂不可能是________(填字母代号)。
A.酸 B.碱 C.盐
(收集资料)
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ.测定室温(20 ℃)时,四种物质的溶解度的数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 36 | 109 | 215 | 9.6 |
(得出结论)
(3)小欣根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是________(填物质名称)。
(设计实验)
(4)①小芳用胶头滴管吸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是____,结论正确。
②小欣为了检验该溶液是NaOH溶液还是Na2CO3溶液,她又进行了如下实验:
操作步骤 | 实验现象 | 结论及化学方程式 |
取样于试管中,滴加氢氧化钙溶液 | _______________ | 猜想②正确,相关的化学方程式:___________________ |
(5)请你选择与小欣不同类别的试剂,来鉴别NaOH溶液和Na2CO3溶液,你选择__________溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com