
【题目】溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
(1)衣服上沾有的油污,可用汽油洗去,是因为汽油能_____ (填“溶解”或“乳化”)油污。
(2)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体的溶解度与_____有关。
(3)某固体物质的溶解度曲线如图所示:
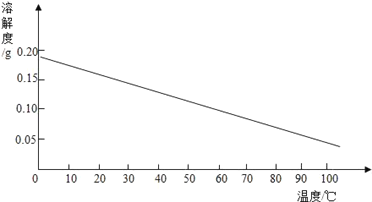
20℃时,要使接近饱和的该物质的溶液变为饱和溶液,通常可采用三种方法,它们分别是_____、_____、_____。
科目:初中化学 来源: 题型:
【题目】小宇为了测定实验室中氯酸钾样品的纯度,取10g样品与1g二氧化锰混合,依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 9.68 | 9.04 | 7.16 | 7.16 |
试计算:
(1)完全反应后产生的氧气的总质量为_____________g;
(2)样品中氯酸钾的纯度是____(写出计算过程)
(3)加热时间t1后,9.68g剩余固体中除杂质外还含有的物质为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示化学反应中溶液的颜色变化。下列叙述错误的是
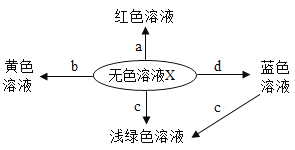
A. 若X是稀硫酸,a可能是紫色石蕊试液 B. 若X是稀硫酸,b可能是氧化物
C. 若X是稀盐酸,c不可能是单质 D. 若X是稀盐酸,d不可能是单质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,进行中和反应实验
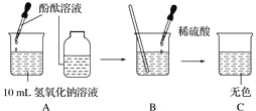
(1)B中发生中和反应的化学方程式_____。
(2)写出C的溶液(除酚酞外)溶质可能存在的几组情况_____(用化学式表示)
(3)反应过程中,不断滴入稀硫酸的话,温度会如何变化?_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题:

(1)写出指定仪器的名称:M ;
(2)下面四种途径都可以得到氧气:

丁途径得到氧气是 (填物理或化学)变化.以绿色化学的理念,你认为甲、乙、丙三种制取氧气的途径中, (填“甲”、“乙”或“丙”)途径更能体现化学实验的绿色化学追求.
(3)用高锰酸钾制取氧气的原理是 (符号表达式),反应基本类型为 .可选用的发生装置是 (填字母代号).
(4)制取氧气时可选用C装置来收集氧气,其理由是
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是a、b两种固体物质的溶解度曲线,下列说法中正确的是( )
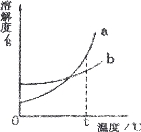
A.a中含有少量b时,一般用蒸发溶剂的方法提纯a
B.t℃时,a、b饱和溶液中含有的溶质质量a大于b
C.当温度大于t℃时,a溶液一定比b溶液浓
D.a物质的溶解度受温度变化的影响较大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量为80.5g,同时生成氢气0.4g。试计算:
(1)样品中锌的质量分数是_____;
(2)完全反应后生成溶液中溶质的质量分数是_____;
(3)所用稀硫酸的质量分数是_____(计算结果保留到0.01%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有________产生,反应的化学方程式是________________________________________________________。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
镁条长度 | 1cm | 2cm | 3cm | 4cm |
相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
[得出结论]镁条与盐酸反应产生白色沉淀与________有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是____________________(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | ________,白色沉淀________ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国著名化学家侯德榜发明的“联合制碱法”的反应原理用化学方程式可简要表示为:①NH3+CO2+H2O=NH4HCO3;
②NH4HCO3+NaCl=NaHCO3+NH4Cl;③2NaHCO3![]() Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。
(1)纯碱属于_____(填“酸”“碱”或“盐”)。
(2)有人认为“联合制碱法”有以下优点,正确的是_____。
A生产过程中部分产物可作为原料使用
B副产品是一种氮肥
C反应均不需要加热,可节约能源
(3)第②步反应中加入的是磨细的食盐粉,将食盐磨细的目的是_____。
(4)25℃时,将a g碳酸钠溶解于50g水中恰好形成饱和溶液。所得溶液的溶质质量分数为_____,此温度下碳酸钠的溶解度为_____g(用含a的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com