
【题目】选择性催化还原(SCR)技术可有效降低柴油发动机的污染物排放,主要工作原理如下图所示:

(1)在发动机内的高温条件下,氮气可以通过化合反应转化成污染物NO,请在方框中补全相应微粒的图示。

_____________;
(2)在氧化催化转化器中,化合价升高的元素是_______。
(3)尿素[CO(NH2)2]溶液热分解时的反应方程式如下:CO(NH2)2 + H2O ![]() 2NH3↑+ CO2↑
2NH3↑+ CO2↑
若消耗60 g尿素,可以产生NH3的质量为________g。
(4)从SCR催化转换器中排出的气体中有N2。下列推测合理的是_______(填字母序号)
A.SCR催化转换器可能将NH3和NO2转化为N2
B.无污染的排出气中只有N2
C.进入SCR催化转换器的气体中可能含有N2
【答案】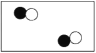 N、C 34 AC
N、C 34 AC
【解析】
本题考查了物质的相互转化和制备,微粒模型图的应用,根据化学反应方程式的计算。解答中要注重质量守恒定律的运用。
(1)氮气和氧气在高温的条件下生成一氧化氮,反应的化学方程式是N2+O2![]() 2NO,1个氮分子与1个氧分子能生成2个NO分子,所以图2方框中补全相应微粒的图示是:
2NO,1个氮分子与1个氧分子能生成2个NO分子,所以图2方框中补全相应微粒的图示是:![]() ;
;
(2)在氧化催化转化器中,一氧化氮和一氧化碳转化成了二氧化碳和二氧化氮,氮元素由+2价变成+4价,碳元素由+2变成+4价,所以化合价升高的元素是N、C;
(3)设生成氨气的质量为x
CO(NH2)2 + H2O ![]() 2NH3↑+ CO2↑
2NH3↑+ CO2↑
60 34
60g x
![]()
x=34g
(4)A、尿素热分解可能有NH3生成,经过SCR催化转换器后变成了无污染的气体,SCR催化转换器可能将NH3和NO2转化为N2,正确;B、NO2和CO2通过SCR催化转换器后,根据质量守恒定律可知,无污染的排出气中有二氧化碳和氮气,错误;C、在氧化催化转化器中通入了空气,空气存在氮气,进入SCR催化转换器的气体中可能含有N2,正确。故选AC。


科目:初中化学 来源: 题型:
【题目】某学校中午的营养餐如表所示

(1)其中富含糖类的是____________。
(2)炒菜时使用铁强化酱油,可以预防____________。
A.佝偻病 B.贫血 C.发育不良
(3)用铁锅炒菜有利人体健康,工业上用一氧化碳和赤铁矿(主要成分为Fe2O3)来炼铁,该反应的化学方程式为____________。现有含160t Fe2O3的赤铁矿,理论上可得到铁的质量为___________t。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用如图的一些装置制备气体,请回答问题:
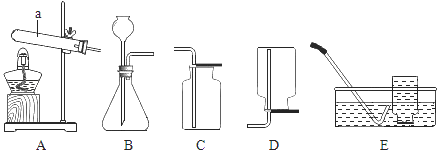
(1)写出图中仪器a的名称_____
(2)实验室制取氧气可选用____(填序号)为发生装置;写出相对应的化学方程式__
(3)实验室收集CO2应选用_____(填序号)装置,理由是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A | B |
(1)电解水实验揭示了水的组成。下图实验中得到氧气的试管是_______(填“1”或“2”)。 (2)电解水的化学方程式为_________。
| (1)潜水时需要氧气,说明氧气能________。 (2)用高锰酸钾制取氧气的化学方程式为_________。
|
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下图所示实验回答问题:
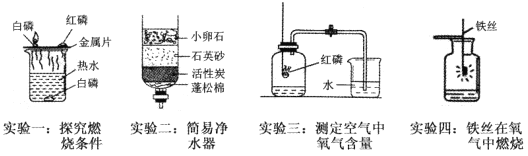
(1)实验一中金属片上的白磷燃烧而热水中的白磷不燃烧,说明燃烧的条件之一是_______________________________________;
(2)实验二中活性炭具有________性,因而可除去水中的色素和异味;
(3)实验三中若测得空气中O2含量小于![]() ,可能的原因是_____________;(答一点即可)。
,可能的原因是_____________;(答一点即可)。
(4)实验四中集气瓶里水的作用是______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以如图(1)和图(2)是两个设计证明分子运动的实验.在图(2)的锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过.
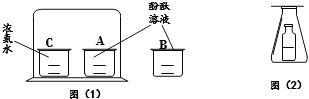
(1)图(2)中观察到的现象是 .
(2)图(1)中观察到的现象是 ,可以得到的结论是 .
(3)在图(1)中的大烧杯外放一杯酚酞溶液的目的是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组做“滴水生火”实验,向包裹过氧化钠(Na2O2)的棉花上滴水,观察到棉花燃烧。
资料:Na2O2与H2O反应生成O2和NaOH
(实验1)验证反应的生成物
步骤 | 操作 | 现象 |
① | 取0.5 g Na2O2固体于锥形瓶中,加入50 mL蒸馏水,得溶液A | 固体全部消失,产生大量气泡 |
② | 将带火星的木条伸入锥形瓶 | _____ |
③ | 取5 mL溶液A于试管中,滴加1滴酚酞溶液 | 溶液变红 |
(1)证明②中有O2生成的现象是_____。
(2)依据③的现象,判断溶液A呈_____(填“酸性”、“碱性”或“中性”)。
(发现问题)③中溶液变红后,约2分钟褪为无色。
(查阅资料)(1)Na2O2与H2O反应分为两步:
①Na2O2与H2O反应生成H2O2和NaOH ②H2O2分解
(2)通常条件下,NaOH溶液与MnO2不反应
(3)H2O2有漂白性,能使变红的酚酞溶液褪色
(4)向5 mL 不同浓度的NaOH溶液中滴加1滴酚酞溶液,现象如下表:
NaOH溶液的浓度 | 30% | 10% | 1% |
现象 | 变红,15 s后褪色 | 变红,40 s后褪色 | 变红,10分钟内 不褪色 |
(猜想与假设)本实验中,溶液褪色的原因可能是:
a.生成的O2
b.溶液中的H2O2
c.溶液中NaOH的浓度
(实验2)验证猜想
编号 | 实验 |
I |
|
II | 取10 mL 溶液A于试管中,加入适量MnO2,将带火星的木条伸入试管。产生无色气体,带火星的木条复燃 |
III | i. 取10 mL 溶液A于试管中,……,过滤 |
ii. 取5 mL滤液于试管中,滴加1滴酚酞溶液。溶液变红,10分钟内不褪色 |
(实验结论)猜想a不成立,猜想b成立,猜想c不成立
综合以上信息,回答下列问题:
(3)实验I的现象是_____。
(4)实验II的目的是_____。产生无色气体的原因是_____(用化学方程式表示)。
(5)补全实验i:取10 mL 溶液A于试管中,_____,过滤。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如下表。下列说法不正确的是( )
温度/℃ | 20 | 40 | 60 | 80 |
溶解度/g | 1.68 | 3.73 | 7.3 | 13.4 |
A. 高氯酸钾的溶解度随温度降低而减小
B. 80℃的高氯酸钾饱和溶液冷却至40℃一定有晶体析出
C. 60℃时,高氯酸钾饱和溶液中溶质的质量分数小于7.3%
D. 20℃时,向2g高氯酸钾中加入98g水,所得溶液的溶质质量分数为2%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com